BIJSLUITER
Inhoud van deze bijsluiter
- 1. NAAM VAN HET DIERGENEESMIDDEL
- 2. SAMENSTELLING
- 3. DOELDIERSOORT(EN)
- 4. INDICATIES VOOR GEBRUIK
- 5. CONTRA-INDICATIES
- 6. SPECIALE WAARSCHUWINGEN
- 7. BIJWERKINGEN
- 8. DOSERING VOOR ELKE DIERSOORT, TOEDIENINGSWIJZEN EN TOEDIENINGSWEGEN
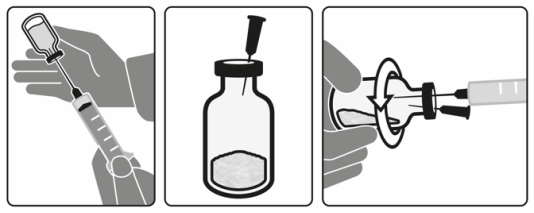
- 9. AANWIJZINGEN VOOR EEN JUISTE TOEDIENING
- 10. WACHTTIJD(EN)
- 11. BIJZONDERE BEWAARVOORSCHRIFTEN
- 12. SPECIALE VOORZORGSMAATREGELEN VOOR HET VERWIJDEREN
- 13. INDELING VAN HET DIERGENEESMIDDEL
- 14. NUMMERS VAN DE VERGUNNINGEN VOOR HET IN DE HANDEL BRENGEN EN VERPAKKINGSGROOTTEN
- 15. DATUM WAAROP DE BIJSLUITER VOOR HET LAATST IS HERZIEN
- 16. CONTACTGEGEVENS
- 17. OVERIGE INFORMATIE