![]() Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
1. NAAM VAN HET GENEESMIDDEL
Wegovy 0,25 mg oplossing voor injectie in een voorgevulde pen
Wegovy 0,5 mg oplossing voor injectie in een voorgevulde pen
Wegovy 1 mg oplossing voor injectie in een voorgevulde pen
Wegovy 1,7 mg oplossing voor injectie in een voorgevulde pen
Wegovy 2,4 mg oplossing voor injectie in een voorgevulde pen
Wegovy 0,25 mg FlexTouch oplossing voor injectie in een voorgevulde pen
Wegovy 0,5 mg FlexTouch oplossing voor injectie in een voorgevulde pen
Wegovy 1 mg FlexTouch oplossing voor injectie in een voorgevulde pen
Wegovy 1,7 mg FlexTouch oplossing voor injectie in een voorgevulde pen
Wegovy 2,4 mg FlexTouch oplossing voor injectie in een voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Voorgevulde pen, één dosis
Wegovy 0,25 mg oplossing voor injectie
Elke met één dosis voorgevulde pen bevat 0,25 mg semaglutide* in 0,5 ml oplossing. Eén ml oplossing bevat 0,5 mg semaglutide*.
Wegovy 0,5 mg oplossing voor injectie
Elke met één dosis voorgevulde pen bevat 0,5 mg semaglutide* in 0,5 ml oplossing. Eén ml oplossing bevat 1 mg semaglutide*.
Wegovy 1 mg oplossing voor injectie
Elke met één dosis voorgevulde pen bevat 1 mg semaglutide* in 0,5 ml oplossing. Eén ml oplossing bevat 2 mg semaglutide*.
Wegovy 1,7 mg oplossing voor injectie
Elke met één dosis voorgevulde pen bevat 1,7 mg semaglutide* in 0,75 ml oplossing. Eén ml oplossing bevat 2,27 mg semaglutide*.
Wegovy 2,4 mg oplossing voor injectie
Elke met één dosis voorgevulde pen bevat 2,4 mg semaglutide* in 0,75 ml oplossing. Eén ml oplossing bevat 3,2 mg semaglutide*.
Voorgevulde pen, FlexTouch
Wegovy 0,25 mg FlexTouch oplossing voor injectie voorgevulde pen
Elke voorgevulde pen bevat 1 mg semaglutide* in 1,5 ml oplossing. Eén ml oplossing bevat 0,68 mg semaglutide*. Een voorgevulde pen bevat 4 doses van 0,25 mg.
Wegovy 0,5 mg FlexTouch oplossing voor injectie voorgevulde pen
1,5 ml: Elke voorgevulde pen bevat 2 mg semaglutide* in 1,5 ml oplossing. Eén ml oplossing bevat 1,34 mg semaglutide*. Een voorgevulde pen bevat 4 doses van 0,5 mg.
3 ml: Elke voorgevulde pen bevat 2 mg semaglutide* in 3 ml oplossing. Eén ml oplossing bevat 0,68 mg semaglutide*. Een voorgevulde pen bevat 4 doses van 0,5 mg.
Wegovy 1 mg FlexTouch oplossing voor injectie voorgevulde pen
Elke voorgevulde pen bevat 4 mg semaglutide* in 3 ml oplossing. Eén ml oplossing bevat 1,34 mg semaglutide*. Een voorgevulde pen bevat 4 doses van 1 mg.
Wegovy 1,7 mg FlexTouch oplossing voor injectie voorgevulde pen
Elke voorgevulde pen bevat 6,8 mg semaglutide* in 3 ml oplossing. Eén ml oplossing bevat 2,27 mg semaglutide*. Een voorgevulde pen bevat 4 doses van 1,7 mg.
Wegovy 2,4 mg FlexTouch oplossing voor injectie voorgevulde pen
Elke voorgevulde pen bevat 9,6 mg semaglutide* in 3 ml oplossing. Eén ml oplossing bevat 3,2 mg semaglutide*. Een voorgevulde pen bevat 4 doses van 2,4 mg.
*humaan ‘glucagon-like peptide-1’-analoog (GLP-1-analoog), geproduceerd met behulp van recombinant- DNA-techniek in Saccharomyces cerevisiae-cellen.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie (injectie)
Heldere en kleurloze isotone oplossing, pH = 7,4.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Volwassenen
Wegovy is geïndiceerd als aanvulling op een caloriearm dieet en meer lichaamsbeweging ten behoeve van gewichtsbeheersing, waaronder gewichtsverlies en op gewicht blijven, bij volwassenen met een aanvankelijke Body Mass Index (BMI) van
• ≥ 30 kg/m2 (obesitas), of
• ≥ 27 kg/m2 tot < 30 kg/m2 (overgewicht) die ten minste één gewichtsgerelateerde comorbiditeit hebben, zoals dysglykemie (prediabetes of diabetes mellitus type 2), hypertensie, dyslipidemie, obstructieve slaapapneu of hart- en vaatziekte.
Voor onderzoeksresultaten met betrekking tot cardiovasculaire risicoreductie, aan obesitas gerelateerd hartfalen en de onderzochte populatie, zie rubriek 5.1.
Adolescenten (≥ 12 jaar)
Wegovy is geïndiceerd als aanvulling op een caloriearm dieet en meer lichaamsbeweging ten behoeve van gewichtsbeheersing bij adolescenten van 12 jaar en ouder met
• obesitas* en
• lichaamsgewicht boven 60 kg.
Behandeling met Wegovy moet worden gestaakt en heroverwogen als adolescente patiënten na 12 weken op de 2,4 mg of maximaal verdraagbare dosis niet ten minste 5% van hun BMI verlaagd hebben.
*Obesitas (BMI ≥ 95e percentiel) zoals gedefinieerd in geslachts- en leeftijdsspecifieke BMI-groeigrafieken (CDC.gov) (zie tabel 1).
Tabel 1 BMI-grenswaarden voor obesitas (≥ 95e percentiel) naar geslacht en leeftijd voor pediatrische patiënten van 12 jaar en ouder (CDC criteria)
Leeftijd (jaren) | BMI (kg/m2) bij 95e percentiel | |
Mannen | Vrouwen | |
12 | 24,2 | 25,2 |
12,5 | 24,7 | 25,7 |
13 | 25,1 | 26,3 |
13,5 | 25,6 | 26,8 |
14 | 26,0 | 27,2 |
14,5 | 26,4 | 27,7 |
15 | 26,8 | 28,1 |
15,5 | 27,2 | 28,5 |
16 | 27,5 | 28,9 |
16,5 | 27,9 | 29,3 |
17 | 28,2 | 29,6 |
17,5 | 28,6 | 30,0 |
4.2 Dosering en wijze van toediening
Dosering
Volwassenen
De onderhoudsdosis van semaglutide 2,4 mg eenmaal per week wordt bereikt door te beginnen met een dosis van 0,25 mg. Om de kans op gastro-intestinale symptomen te verkleinen, moet de dosis over een periode van 16 weken worden verhoogd naar een onderhoudsdosis van 2,4 mg eenmaal per week (zie tabel 2).
Indien nodig kan de dosis worden verhoogd naar 7,2 mg eenmaal per week na ten minste 4 weken behandeling met de 2,4 mg dosis, bij volwassenen met een BMI van ≥ 30 kg/m2 bij aanvang van de behandeling.
Als met 7,2 mg geen verdere klinische verbetering in lichaamsgewicht wordt waargenomen, verlaag dan de dosis naar 2,4 mg eenmaal per week.
Overweeg uitstel van dosisverhoging of overweeg verlaging naar de vorige dosis in geval van significante gastro-intestinale symptomen totdat de symptomen zijn verminderd.
Tabel 2 Schema voor dosisverhoging
Dosisverhoging | Wekelijkse dosis |
Week 1–4 | 0,25 mg |
Week 5–8 | 0,5 mg |
Week 9–12 | 1 mg |
Week 13–16 | 1,7 mg |
Onderhoudsdosis | 2,4 mg |
Onderhoudsdosis | 7,2 mg |
Adolescenten
Voor adolescenten van 12 jaar en ouder dient hetzelfde schema voor dosisverhoging te worden toegepast als voor volwassenen (zie tabel 2). De dosis moet worden verhoogd tot 2,4 mg (onderhoudsdosis) of tot de maximaal verdraagbare dosis is bereikt. Doses hoger dan 2,4 mg per week worden niet aanbevolen.
Patiënten met diabetes type 2
Overweeg bij patiënten met diabetes type 2 bij het initiëren van behandeling met semaglutide een dosisverlaging van gelijktijdig gebruikte insuline of insuline-secretagogen (zoals sulfonylureumderivaten) om het risico op hypoglykemie te verlagen, zie rubriek 4.4.
Gemiste dosis
Als een dosis is gemist, dient deze zo snel mogelijk en binnen 5 dagen na de gemiste dosis alsnog te worden toegediend. Als er meer dan 5 dagen verstreken zijn, moet de gemiste dosis worden overgeslagen en moet de volgende dosis op de gebruikelijke geplande dag worden toegediend. In beide gevallen kunnen patiënten vervolgens hun gebruikelijke wekelijkse doseringsschema hervatten. Als er meer doses gemist worden, moet het verlagen van de aanvangsdosis voor het herstarten worden overwogen.
Specifieke patiëntgroepen
Ouderen (≥ 65 jaar)
Er is geen dosisaanpassing nodig op basis van leeftijd. De therapeutische ervaring bij patiënten ≥ 85 jaar is beperkt.
Patiënten met nierinsufficiëntie
Er is geen dosisaanpassing nodig voor patiënten met lichte of matig ernstige nierinsufficiëntie. Er is beperkte ervaring met het gebruik van semaglutide bij patiënten met ernstige nierinsufficiëntie. Semaglutide wordt niet aanbevolen voor gebruik bij patiënten met ernstige nierinsufficiëntie (eGFR < 30 ml/min/1,73 m2) waaronder patiënten met terminale nierinsufficiëntie (zie rubriek 4.4, 4.8 en 5.2).
Patiënten met leverinsufficiëntie
Er is geen dosisaanpassing nodig voor patiënten met lichte of matig ernstige leverinsufficiëntie. Er is beperkte ervaring met het gebruik van semaglutide bij patiënten met ernstige leverinsufficiëntie. Semaglutide wordt niet aanbevolen voor gebruik bij patiënten met ernstige leverinsufficiëntie en moet met voorzichtigheid gebruikt worden bij patiënten met lichte of matig ernstige leverinsufficiëntie (zie rubriek 4.4 en 5.2).
Pediatrische patiënten
Er is geen dosisaanpassing nodig voor adolescenten van 12 jaar en ouder. Doses hoger dan 2,4 mg worden niet aanbevolen.
De veiligheid en werkzaamheid van semaglutide bij kinderen onder de 12 jaar zijn niet vastgesteld.
Wijze van toediening
Subcutaan gebruik.
Wegovy moet eenmaal per week worden toegediend op een gewenst moment van de dag, onafhankelijk van de maaltijden.
Het wordt subcutaan geïnjecteerd in de buik, in de dij of in de bovenarm. De injectieplaats kan worden afgewisseld. Het mag niet intraveneus of intramusculair worden toegediend.
Voor de 7,2 mg dosis: injecteer opeenvolgend drie doses van 2,4 mg. De injecties kunnen in hetzelfde lichaamsgebied worden toegediend maar moeten ten minste 5 cm uit elkaar zitten.
De dag van de wekelijkse toediening kan indien nodig worden gewijzigd zolang de tijd tussen doses ten minste 3 dagen (> 72 uur) bedraagt. Na selectie van een nieuwe toedieningsdag, moet de toediening eenmaal per week worden voortgezet.
Bij het toedienen van Wegovy met één dosis voorgevulde pen dient de pen stevig tegen de huid te worden gehouden totdat de gele balk tot stilstand is gekomen. De injectie duurt ongeveer 5–10 seconden.
Patiënten moeten worden geadviseerd de instructies voor het gebruik in de bijsluiter zorgvuldig door te lezen vóór toediening van het geneesmiddel.
Zie rubriek 6.6 voor verdere informatie vóór de toediening.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
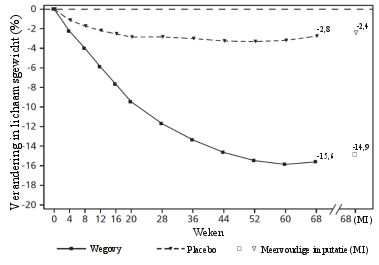
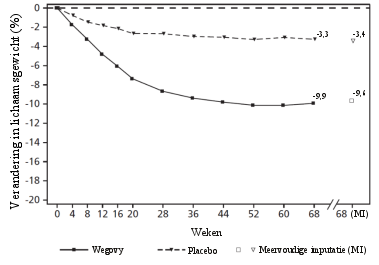
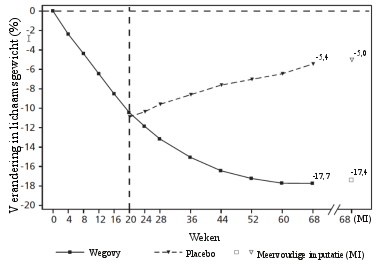
In vier fase 3a-studies werden 2.650 volwassen patiënten blootgesteld aan Wegovy. De duur van de studies was 68 weken. De meest gemelde bijwerkingen waren gastro-intestinale aandoeningen, zoals nausea, diarree, constipatie en braken.
Tabel met lijst van de bijwerkingen
In tabel 3 staan bijwerkingen die zijn gemeld tijdens klinische studies bij volwassenen en in postmarketingmeldingen. De frequenties zijn gebaseerd op een verzameling van de fase 3a-studies.
De bijwerkingen die worden geassocieerd met Wegovy zijn onderverdeeld naar systeem/orgaanklasse en frequentie. De frequenties zijn gedefinieerd als: zeer vaak (≥ 1/10); vaak (≥ 1/100, < 1/10); soms (≥ 1/1.000, < 1/100); zelden (≥ 1/10.000, < 1/1.000); zeer zelden (< 1/10.000) en niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Tabel 3 Frequentie van bijwerkingen van semaglutide
MedDRA | Zeer vaak | Vaak | Soms | Zelden | Zeer zelden | Niet bekend |
Immuunsysteem-aandoeningen |
|
|
| Anafylacti-sche reactie |
|
|
Voedings- en stofwisselings-stoornissen |
| Hypo-glykemie bij patiënten met type 2 diabetesa |
|
|
|
|
Zenuwstelsel-aandoeningen | Hoofdpijnb | Duizeligheidb |
|
|
|
|
Oogaandoeningen |
| Diabetische retinopathie bij patiënten met diabetes type 2a |
|
| Niet-arteritische anterieure ischemische opticusneuropathie (NAION) |
|
Hartaandoeningen |
|
| Hypotensie |
|
|
|
Maagdarmstelsel-aandoeningen | Brakena,b | Gastritisb,c | Acute pan-creatitisa |
|
| Ingewanden-obstructie |
Lever- en galaandoeningen |
| Cholelithiasea |
|
|
|
|
Huid- en onderhuid-aandoeningen |
| Haaruitvala |
| Angio-oedeem |
|
|
Algemene aandoeningen en toedieningsplaats-stoornissen | Vermoeid-heidb,c | Reacties op de injectieplaatsc |
|
|
|
|
Onderzoeken |
|
| Verhoogde amylasec |
|
|
|
a) zie hieronder voor een beschrijving van geselecteerde bijwerkingen
b) hoofdzakelijk waargenomen in de periode van dosisverhoging
c) gegroepeerde voorkeurstermen
d) frequentie is gebaseerd op het 3a-programma. Een toegenomen frequentie is waargenomen bij de dosis van 7,2 mg. Zie de rubriek “Dysesthesie” hieronder voor meer informatie.
Beschrijving van een geselecteerd aantal bijwerkingen
De onderstaande informatie over specifieke bijwerkingen heeft, tenzij anders aangegeven, betrekking op de fase 3a-studies
Gastro-intestinale bijwerkingen
Gedurende de studieduur van 68 weken kwam nausea voor bij 43,9% van patiënten die behandeld werden met semaglutide (16,1% bij placebo), diarree bij 29,7% (15,9% bij placebo) en braken bij 24,5% (6,3% bij placebo). De meeste bijwerkingen waren mild tot matig van aard en van korte duur. Constipatie kwam voor bij 24,2% van patiënten behandeld met semaglutide (11,1% bij placebo) en was mild tot matig in ernst en van langere duur. Bij patiënten die werden behandeld met semaglutide was de mediane duur van nausea 8 dagen, braken 2 dagen, diarree 3 dagen en constipatie 47 dagen.
Patiënten met matig ernstige nierinsufficiëntie (eGFR ≥ 30 tot < 60 ml/min/1,73 m2) ervaren mogelijk meer gastro-intestinale bijwerkingen bij de behandeling met semaglutide.
De gastro-intestinale voorvallen leidden bij 4,3% van de patiënten tot definitieve stopzetting van de behandeling.
Patiënten met gastroparese die worden behandeld met semaglutide kunnen ernstigere of hevigere gastro-intestinale bijwerkingen ervaren.
Acute pancreatitis
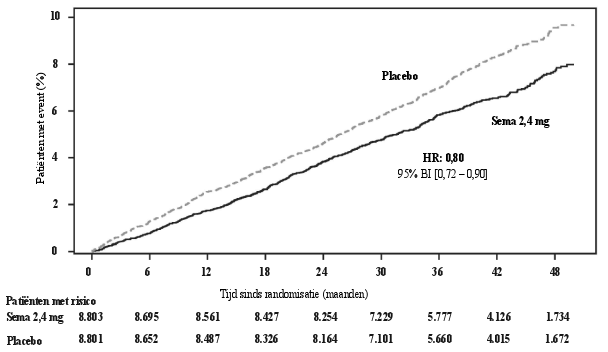
De frequentie van na beoordeling bevestigde, acute pancreatitis gemeld in klinische fase 3a-studies was respectievelijk 0,2% voor semaglutide en < 0,1% voor placebo. In SELECT, het onderzoek naar cardiovasculaire uitkomsten, was de frequentie van na beoordeling bevestigde acute pancreatitis 0,2% voor semaglutide en 0,3% voor placebo.
Acute galsteenziekte/cholelithiase
Cholelithiase werd gemeld bij 1,6% en leidde tot cholecystitis bij 0,6% van patiënten behandeld met semaglutide. Cholelithiase en cholecystitis werden gemeld bij respectievelijk 1,1% en 0,3% van de patiënten die placebo kregen.
Haaruitval
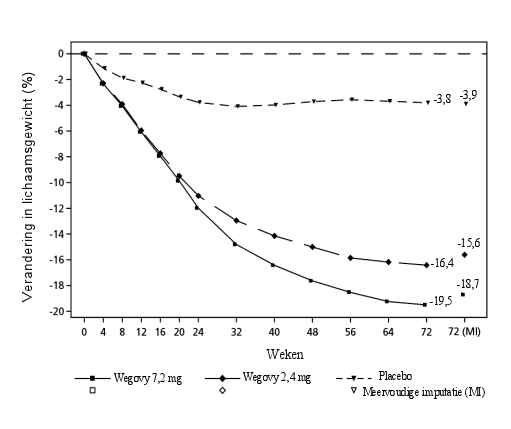
Haaruitval werd gemeld bij 2,5% van patiënten behandeld met semaglutide en bij 1,0% van de patiënten die placebo kregen. In de STEP UP‑studies werd haaruitval gerapporteerd bij 5,3% van de patiënten behandeld met semaglutide 7,2 mg en bij 1,0% van de patiënten behandeld met placebo. De voorvallen waren voornamelijk mild van aard en de meeste patiënten herstelden tijdens de voortgezette behandeling. Haaruitval werd vaker gemeld bij patiënten met een groter gewichtsverlies (≥ 20%).
Verhoogde hartslag
In de fase 3a-studies werd een gemiddelde stijging van 3 slagen per minuut (bpm) ten opzichte van een uitgangswaarde van 72 bpm waargenomen bij patiënten behandeld met semaglutide. Het aandeel patiënten met een toename in hartslag ten opzichte van de uitgangswaarde van ≥ 10 bpm op elk moment gedurende de behandeling betrof 67,0% in de semaglutidegroep versus 50,1% in de placebogroep.
Immunogeniciteit
In overeenstemming met de mogelijk immunogene eigenschappen van geneesmiddelen die eiwitten of peptiden bevatten, kunnen patiënten na behandeling met semaglutide antilichamen ontwikkelen. Het aandeel van patiënten dat positief testte op antilichamen tegen semaglutide op een willekeurig tijdstip na aanvang van de studie was 2,9 – 10,9% voor semaglutide 2,4 mg en 15,3% voor semaglutide 7,2 mg. Geen van de patiënten had neutraliserende antilichamen tegen semaglutide of antilichamen tegen semaglutide met endogeen GLP-1-neutraliserend effect. Het is mogelijk dat tijdens de behandeling hoge semaglutideconcentraties de gevoeligheid van de assays hebben verminderd; het risico van fout-negatieve uitslagen kan dus niet worden uitgesloten. Bij patiënten met een positieve testuitslag voor antilichamen tijdens en na de behandeling was de aanwezigheid van antilichamen echter van voorbijgaande aard en had deze geen waarneembaar effect op werkzaamheid en veiligheid.
Hypoglykemie bij patiënten met diabetes type 2
In STEP 2 werd klinisch significante hypoglykemie waargenomen bij 6,2% (0,1 voorvallen/patiëntjaar) van de patiënten behandeld met semaglutide, in vergelijking met 2,5% (0,03 voorvallen/patiëntjaar) bij patiënten behandeld met placebo. Hypoglykemie bij gebruik van semaglutide werd zowel met als zonder gelijktijdig gebruik van sulfonylureumderivaten waargenomen. Eén episode (0,2% van de patiënten, 0,002 voorvallen/patiëntjaar) werd gemeld als ernstig bij een patiënt die niet gelijktijdig werd behandeld met een sulfonylureumderivaat. Het risico op hypoglykemie werd verhoogd als semaglutide werd gebruikt met een sulfonylureumderivaat.
In STEP-HFpEF-DM werd klinisch significante hypoglykemie waargenomen bij 4,2% van de patiënten zowel in de semaglutide- als in de placebogroep bij gelijktijdig gebruik met sulfonylureumderivaten en/of insuline (0,065 voorvallen/patiëntjaar met semaglutide en 0,098 voorvallen/patiëntjaar met placebo).
Diabetische retinopathie bij patiënten met diabetes type 2
Een 2 jaar durende klinische studie onderzocht 3.297 patiënten met diabetes type 2, met een hoog cardiovasculair risico, lange duur van de diabetes en onvoldoende gecontroleerde bloedglucose. In deze studie kwamen meer beoordeelde gevallen van complicaties van diabetische retinopathie voor bij patiënten behandeld met semaglutide (3,0%) in vergelijking tot placebo (1,8%). Dit werd waargenomen bij met insuline behandelde patiënten die bekend waren met diabetische retinopathie. Het behandelverschil werd reeds in een vroeg stadium duidelijk en hield gedurende de studie aan. In STEP 2 werden retinale aandoeningen gemeld bij 6,9% van de patiënten behandeld met Wegovy, 6,2% van de patiënten behandeld met semaglutide 1 mg en 4,2% van de patiënten behandeld met placebo. De meeste voorvallen werden gemeld als diabetische retinopathie (respectievelijk 4,0%, 2,7% en 2,7%) en niet-proliferatieve retinopathie (respectievelijk 0,7%, 0% en 0%).
Dysesthesie
Voorvallen gerelateerd aan een klinisch beeld van veranderd huidgevoel zoals dysesthesie, paresthesie, hyperesthesie, branderig gevoel van de huid, allodynie en gevoelige huid werden gemeld bij 2,1% van de patiënten behandeld met Wegovy injectie en bij 1,2% van de patiënten behandeld met placebo. De voorvallen waren mild tot matig van aard en de meeste patiënten herstelden terwijl ze de behandeling voortzetten.
In STEP‑UP werden dysesthesie-gerelateerde verschijnselen gemeld bij 21,6% van de patiënten behandeld met semaglutide 7,2 mg en 0,3% bij patiënten behandeld met placebo. De meeste voorvallen in de 7,2 mg‑groep waren mild tot matig van aard en 85% (368 van 434 voorvallen) herstelde tijdens de behandeling. In de semaglutide 7,2 mg s.c.‑groep herstelde 28% (123 van alle 434 voorvallen) na aanpassingen in de dosis van het studieproduct.
Niet-arteritische anterieure ischemische opticusneuropathie (NAION)
Resultaten uit verschillende grote epidemiologische studies geven aan dat blootstelling aan semaglutide bij volwassenen met diabetes type 2 geassocieerd wordt met een ongeveer tweevoudige toename van het relatieve risico op het ontwikkelen van NAION, wat overeenkomt met ongeveer 1 bijkomend geval per 10.000 patiëntjaren behandeling.
Pediatrische patiënten
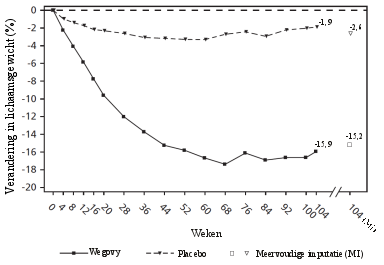
In een klinische studie uitgevoerd bij adolescenten van 12 tot 18 jaar, met obesitas of overgewicht met ten minste één gewichtsgerelateerde comorbiditeit, werden 133 patiënten blootgesteld aan Wegovy. De studieduur was 68 weken.
Over het algemeen waren de frequentie, het type en de ernst van de bijwerkingen bij de adolescenten vergelijkbaar met die waargenomen bij de volwassen populatie. Cholelithiase werd gemeld bij 3,8% van de patiënten behandeld met Wegovy en bij 0% van de patiënten behandeld met placebo.
Na 68 weken behandeling werden geen effecten op de groei of puberale ontwikkeling gevonden.
Andere speciale populaties
In de SELECT- en SUSTAIN 6-studies was het bijwerkingenprofiel bij volwassenen met vastgestelde cardiovasculaire ziekte, vergelijkbaar met dat bij fase 3a-studies voor gewichtsbeheersing.
In de HFpEF-studies, bij volwassenen met aan obesitas gerelateerd hartfalen met behouden ejectiefractie (HFpEF), was het bijwerkingenprofiel vergelijkbaar met dat bij fase 3a-studies voor gewichtsbeheersing.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie
Website: www.eenbijwerkingmelden.be
E-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Novo Nordisk A/S
Novo Allé
DK-2880 Bagsværd
Denemarken
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/21/1608/001
EU/1/21/1608/002
EU/1/21/1608/003
EU/1/21/1608/004
EU/1/21/1608/005
EU/1/21/1608/006
EU/1/21/1608/007
EU/1/21/1608/008
EU/1/21/1608/009
EU/1/21/1608/010
EU/1/21/1608/011
EU/1/21/1608/012
10. DATUM VAN HERZIENING VAN DE TEKST
03/2026
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau http://www.ema.europa.eu
1
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4924130 | WEGOVY 1,7MG FLEXTOUCH OPL INJ VOORGEV.PEN | € 211,6 | - | Ja | - | - | |
| 4924239 | WEGOVY 0,25MG FLEXTOUCH OPL INJ VOORGEV.PEN 1,5ML | € 144,82 | - | Ja | - | - | |
| 4924247 | WEGOVY 0,5MG FLEXTOUCH OPL INJ VOORGEV.PEN 1,5ML | € 144,82 | - | Ja | - | - | |
| 4924262 | WEGOVY 1MG FLEXTOUCH OPL INJ VOORGEV.PEN 3ML | € 144,82 | - | Ja | - | - | |
| 4924254 | WEGOVY 0,5MG FLEXTOUCH OPL INJ VOORGEV.PEN 3ML | € 144,82 | - | Ja | - | - | |
| 4924270 | WEGOVY 2,4MG FLEXTOUCH OPL INJ VOORGEV.PEN 3ML | € 232,8 | - | Ja | - | - |