1. NAAM VAN HET GENEESMIDDEL
Norditropin FlexPro 5 mg/1,5 ml, oplossing voor injectie in een voorgevulde pen
Norditropin FlexPro 10 mg/1,5 ml, oplossing voor injectie in een voorgevulde pen
Norditropin FlexPro 15 mg/1,5 ml, oplossing voor injectie in een voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Norditropin FlexPro: 5 mg/1,5 ml
Eén ml oplossing bevat 3,3 mg somatropine
Norditropin FlexPro: 10 mg/1,5 ml
Eén ml oplossing bevat 6,7 mg somatropine
Norditropin FlexPro: 15 mg/1,5 ml
Eén ml oplossing bevat 10 mg somatropine
somatropine (in E. coli geproduceerd via recombinant DNA)
1 mg somatropine komt overeen met 3 IE (Internationale Eenheden) somatropine
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1
3. FARMACEUTISCHE VORM
Oplossing voor injectie in een voorgevulde pen
Heldere, kleurloze oplossing
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Kinderen:
Groeiachterstand door groeihormoondeficiëntie (GHD)
Groeiachterstand bij meisjes ten gevolge van dysgenesie van de gonaden (Turner-syndroom)
Groeiachterstand bij prepuberale kinderen ten gevolge van chronische nierinsufficiëntie
Groeistoornis (huidige lengte SDS < -2,5 en met een voor ouderlengte gecorrigeerde lengte SDS < -1) bij kinderen die klein geboren zijn in functie van de duur van de zwangerschap, met een geboortegewicht en/of lengte kleiner dan -2 Standaarddeviaties (SD), bij wie geen inhaalgroei (groeisnelheid SDS < 0 gedurende het laatste jaar) is opgetreden tegen de leeftijd van 4 jaar of later.
Groeiachterstand ten gevolge van het Noonan-syndroom.
Volwassenen:
Groeihormoondeficiëntie vanaf de kindertijd:
Patiënten met groeihormoondeficiëntie tijdens de kindertijd moeten na voltooiing van de groei opnieuw geëvalueerd worden op de secretiecapaciteit voor groeihormoon. Onderzoek is niet nodig voor diegenen met meer dan drie hypofysaire hormoondeficiënties, met ernstige GHD ten gevolge van een gekende genetische oorzaak, ten gevolge van structurele hypothalamo-hypofysaire abnormaliteiten, ten gevolge van een tumor van het centraal zenuwstelsel of ten gevolge van een hoge dosis craniale bestraling, of bij GHD ten gevolge van een hypofysaire/hypothalamische ziekte of trauma, indien de IGF-1-serumwaarden (Insulin-like Growth Factor-1) < -2 SDS zijn na ten minste 4 weken stoppen van groeihormoonbehandeling.
Bij alle andere patiënten is een IGF-1-evaluatie en één groeihormoon dynamische test vereist.
Groeihormoondeficïentie vanaf de volwassen leeftijd:
Ernstige GHD ten gevolge van een bekende hypothalamo-hypofysaire aandoening, craniale bestraling en hersenschade ten gevolge van een trauma. GHD dient samen te gaan met één ander hormoontekort met uitzondering van prolactine. GHD dient te worden aangetoond door een dynamische test nadat adequate substitutietherapie van elke andere deficiëntie werd ingesteld.
Bij volwassenen wordt de insulinetolerantietest als dynamische test aanbevolen. Indien de insulinetolerantietest gecontra-indiceerd is, dient men alternatieve dynamische testen uit te voeren. De gecombineerde arginine-GHRH-test wordt aanbevolen. Een arginine- of glucagontest kan ook overwogen worden. Deze testen bezitten evenwel een minder gestaafde diagnostische waarde dan de insulinetolerantietest.
4.2 Dosering en wijze van toediening
Norditropin mag enkel worden voorgeschreven door artsen met een specialistische kennis van de therapeutische indicatie.
Dosering
De dosering is individueel en moet steeds worden aangepast in overeenstemming met de individuele klinische en biochemische respons op de behandeling.
De algemeen aanbevolen doseringen zijn:
Pediatrische patiënten:
Groeihormoontekort
0,025-0,035 mg/kg/dag of 0,7-1,0 mg/m2/dag
Bij blijvende GHD na voltooiing van de groei, dient de groeihormoonbehandeling voortgezet te worden om een volledige somatische volwassen ontwikkeling te bereiken met inbegrip van de vetvrije massa en de minerale botontwikkeling (voor meer informatie betreffende de dosering, zie Substitutietherapie bij volwassenen).
Turner-syndroom
0,045-0,067 mg/kg/dag of 1,3-2,0 mg/m2/dag
Chronische nierinsufficiëntie
0,050 mg/kg/dag of 1,4 mg/m2/dag (zie rubriek 4.4)
Kinderen die klein geboren zijn in functie van de duur van de zwangerschap
0,035 mg/kg/dag of 1,0 mg/m2/dag
Een dosis van 0,035 mg/kg/dag wordt gewoonlijk aanbevolen tot de eindlengte is bereikt (zie rubriek 5.1).
De behandeling dient na het eerste jaar behandeling te worden gestaakt als de groeisnelheid SDS kleiner is dan + 1.
De behandeling dient te worden gestaakt als de groeisnelheid < 2 cm/jaar is en, als bevestiging noodzakelijk is, de botleeftijd > 14 jaar (meisjes) of > 16 jaar (jongens) is, wat overeenstemt met het sluiten van de epifysairschijven.
Noonan-syndroom:
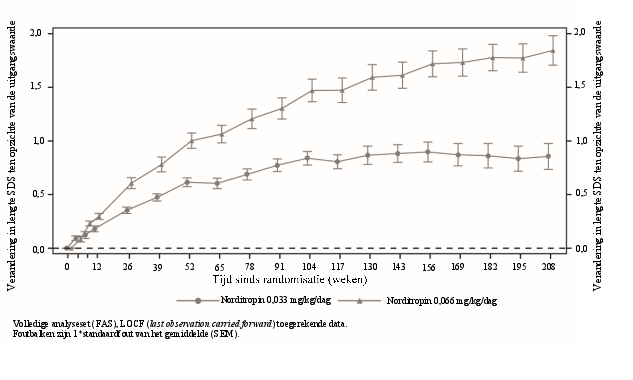
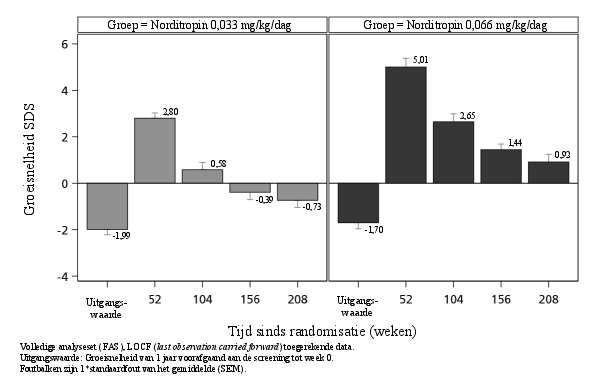
0,066 mg/kg/dag is de aanbevolen dosis, hoewel in sommige gevallen 0,033 mg/kg/dag voldoende kan zijn (zie rubriek 5.1).
De behandeling dient te worden gestaakt op het moment van de sluiting van de epifysairschijven (zie rubriek 4.4).
Volwassen patiënten:
Substitutietherapie bij volwassenen
De dosering moet aangepast worden aan de behoeften van de individuele patiënt.
Bij patiënten met GHD vanaf de kindertijd is de aanbevolen dosis voor het heropstarten van de behandeling 0,2-0,5 mg/dag met erop volgend dosisaanpassing op basis van de IGF-1-concentratiebepaling.
Bij patiënten met GHD vanaf de volwassen leeftijd, wordt het aanbevolen de behandeling te starten met een lage dosis: 0,1-0,3 mg/dag. Het wordt aanbevolen de dosering geleidelijk maandelijks te verhogen in functie van de klinische respons en de ongewenste effecten bij de patiënt. De IGF-1 serumspiegel kan gebruikt worden als richtlijn om de dosering aan te passen. Vrouwen kunnen hogere doses nodig hebben dan mannen, terwijl mannen in de loop van de tijd een toenemende IGF-1-gevoeligheid vertonen. Dit betekent dat er een risico bestaat dat vrouwen, vooral diegenen onder orale oestrogenenbehandeling, onderbehandeld worden, terwijl mannen overbehandeld worden.
De vereiste dosis vermindert met de leeftijd. De onderhoudsdosering varieert sterk van persoon tot persoon, maar bedraagt zelden meer dan 1,0 mg/dag.
Wijze van toediening
In het algemeen wordt aanbevolen het product dagelijks ’s avonds subcutaan toe te dienen. Om het optreden van lipoatrofie te voorkomen, moet men regelmatig de injectieplaats afwisselen.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
Somatropine dient niet gebruikt te worden wanneer er enige aanwijzing is van activiteit van een tumor. Intracraniale tumoren moeten inactief zijn en de kankerbehandeling dient voltooid te zijn alvorens een therapie met groeihormoon (GH) te starten. De behandeling dient te worden gestaakt als er aanwijzingen zijn van groei van tumoren.
Somatropine dient niet gebruikt te worden voor de stimulatie van de longitudinale groei bij kinderen met gesloten epifysairschijven.
Patiënten met een acute kritische aandoening die lijden aan complicaties na een openhartoperatie, abdominale chirurgie, meervoudig trauma ten gevolge van een ongeval, acute ademhalingsinsufficiëntie of vergelijkbare aandoeningen dienen niet te worden behandeld met somatropine (zie rubriek 4.4).
Bij kinderen met chronische nierinsufficiëntie dient de behandeling met Norditropin FlexPro te worden gestaakt bij niertransplantatie.
4.8 Bijwerkingen
Patiënten met een groeihormoondeficiëntie worden gekenmerkt door een tekort aan extracellulair volume. Wanneer de behandeling met somatropine wordt gestart, wordt dit tekort gecorrigeerd. Vochtretentie met perifeer oedeem kan optreden, vooral bij volwassenen. Soms kan bij volwassenen het carpaal-tunnelsyndroom optreden. De symptomen zijn doorgaans tijdelijk en dosisafhankelijk, waardoor het soms nodig is de dosis tijdelijk te verminderen.
Lichte gewrichtspijn, spierpijn en paresthesieën kunnen eveneens optreden, maar deze symptomen verdwijnen gewoonlijk spontaan.
Bij kinderen treden soms of zelden bijwerkingen op.
Ervaring verkregen tijdens klinische studies:
Systeem/orgaanklassen | Zeer vaak | Vaak | Soms | Zelden |
Voedings- en stofwisselings-stoornissen |
|
| Diabetes mellitus type 2 bij volwassenen |
|
Zenuwstelsel- |
| Hoofdpijn en paresthesie bij volwassenen | Carpaal-tunnelsyndroom bij volwassenen. Hoofdpijn bij kinderen |
|
Huid- en onderhuid-aandoeningen |
|
| Pruritus bij volwassenen | Rash bij kinderen |
Skeletspierstelsel-, bindweefselaandoeningen |
| Artralgie, gewrichtsstijfheid en myalgie bij volwassenen | Spierstijfheid bij volwassenen | Artralgie en myalgie bij kinderen |
Voortplantingsstelsel- en borstaandoeningen |
|
| Bij volwassenen en kinderen, gynaecomastie |
|
Algemene aandoeningen en toedieningsplaats-stoornissen | Perifeer oedeem bij volwassenen (zie tekst hierboven) |
| Pijn ter hoogte van de injectieplaats bij volwassenen en kinderen. Reactie op de injectieplaats bij kinderen | Perifeer oedeem bij kinderen |
Bij kinderen met Turner-syndroom werd een toegenomen groei van handen en voeten gedurende de behandeling met somatropine gemeld.
Een open, gerandomiseerde, klinische studie bij patiënten met Turner-syndroom behandeld met hoge doses Norditropin, heeft een tendens tot een verhoogde incidentie van otitis media aangetoond. De toename van oorinfecties gaf echter geen aanleiding tot meer ooroperaties/trommelvliesbuisjes vergeleken met de lager gedoseerde groep in de studie.
Postmarketingervaring:
Naast de bijwerkingen die hierboven werden vermeld, werden de bijwerkingen die hieronder opgelijst staan spontaan gerapporteerd en in het algemeen beschouwd als mogelijk gerelateerd aan een behandeling met Norditropin. De frequenties van deze bijwerkingen kunnen niet bepaald worden met de beschikbare gegevens:
– Neoplasmata, benigne en maligne (inclusief cysten en poliepen): Leukemie werd gemeld bij een klein aantal patiënten met een groeihormoondeficiëntie (zie rubriek 4.4.)
– Immuunsysteemaandoeningen: Overgevoeligheid (zie rubriek 4.3). Aanmaak van antilichamen gericht tegen somatropine. De titers en bindingscapaciteiten van deze antilichamen waren zeer laag en beïnvloedden de groei ten gevolge van behandeling met Norditropin niet
– Endocriene aandoeningen: Hypothyroïdie. Daling van de serumthyroxinespiegel (zie rubriek 4.4)
– Voedings- en stofwisselingsstoornissen: Hyperglykemie (zie rubriek 4.4)
– Zenuwstelselaandoeningen: Benigne intracraniale hypertensie (zie rubriek 4.4)
– Skeletspierstelsel- en bindweefselaandoeningen: Ziekte van Legg-Calvé-Perthes. De ziekte van Legg-Calvé-Perthes zou frequenter kunnen voorkomen bij patiënten met een klein gestalte
– Onderzoeken: Toename van het alkalisch fosfatase in bloed.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem:
Federaal agentschap voor geneesmiddelen en gezondheidsproducten
www.fagg.be
Afdeling Vigilantie
Website: www.eenbijwerkingmelden.be
E-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Novo Nordisk Pharma
Alfons Gossetlaan 32E/202
1702 Groot-Bijgaarden
België
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Norditropin FlexPro 5 mg/1,5 ml: BE381184
Norditropin FlexPro 10 mg/1,5 ml: BE381193
Norditropin FlexPro 15 mg/1,5 ml: BE381202
10. DATUM VAN HERZIENING VAN DE TEKST
04/2025
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4726451 | NORDITROPIN FLEXPRO 10MG/1,5ML OPL INJ VOORG.PEN 5 | € 952,22 | - | Ja | € 12,8 | € 8,5 | |
| 4726469 | NORDITROPIN FLEXPRO 5MG/1,5ML OPL INJ VOORGEV.PEN5 | € 481,59 | - | Ja | € 12,8 | € 8,5 | |
| 4726477 | NORDITROPIN FLEXPRO 15MG/1,5ML OPL INJ VOORG.PEN 5 | € 1422,64 | - | Ja | € 12,8 | € 8,5 | |
| 4856761 | NORDITROPIN FLEXPRO 5MG/1,5ML OPL INJ VOORGEV.PEN1 | € 105,1 | - | Ja | € 12,8 | € 8,5 | |
| 4856779 | NORDITROPIN FLEXPRO 15MG/1,5ML OPL INJ VOORG.PEN 1 | € 293,3 | - | Ja | € 12,8 | € 8,5 | |
| 4856787 | NORDITROPIN FLEXPRO 10MG/1,5ML OPL INJ VOORG.PEN 1 | € 199,22 | - | Ja | € 12,8 | € 8,5 |