SAMENVATTING VAN DE PRODUCTKENMERKEN ![]() Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
1. NAAM VAN HET GENEESMIDDEL
Mounjaro 2,5 mg oplossing voor injectie in voorgevulde pen
Mounjaro 5 mg oplossing voor injectie in voorgevulde pen
Mounjaro 7,5 mg oplossing voor injectie in voorgevulde pen
Mounjaro 10 mg oplossing voor injectie in voorgevulde pen
Mounjaro 12,5 mg oplossing voor injectie in voorgevulde pen
Mounjaro 15 mg oplossing voor injectie in voorgevulde pen
Mounjaro 2,5 mg oplossing voor injectie in injectieflacon
Mounjaro 5 mg oplossing voor injectie in injectieflacon
Mounjaro 7,5 mg oplossing voor injectie in injectieflacon
Mounjaro 10 mg oplossing voor injectie in injectieflacon
Mounjaro 12,5 mg oplossing voor injectie in injectieflacon
Mounjaro 15 mg oplossing voor injectie in injectieflacon
Mounjaro 2,5 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Mounjaro 5 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Mounjaro 7,5 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Mounjaro 10 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Mounjaro 12,5 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Mounjaro 15 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Voorgevulde pen, eenmalige dosis
Mounjaro 2,5 mg oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 2,5 mg tirzepatide in 0,5 ml oplossing (5 mg/ml).
Mounjaro 5 mg oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 5 mg tirzepatide in 0,5 ml oplossing (10 mg/ml).
Mounjaro 7,5 mg oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 7,5 mg tirzepatide in 0,5 ml oplossing (15 mg/ml).
Mounjaro 10 mg oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 10 mg tirzepatide in 0,5 ml oplossing (20 mg/ml).
Mounjaro 12,5 mg oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 12,5 mg tirzepatide in 0,5 ml oplossing (25 mg/ml).
Mounjaro 15 mg oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 15 mg tirzepatide in 0,5 ml oplossing (30 mg/ml).
Injectieflacon, eenmalige dosis
Mounjaro 2,5 mg oplossing voor injectie in injectieflacon
Elke injectieflacon bevat 2,5 mg tirzepatide in 0,5 ml oplossing (5 mg/ml).
Mounjaro 5 mg oplossing voor injectie in injectieflacon
Elke injectieflacon bevat 5 mg tirzepatide in 0,5 ml oplossing (10 mg/ml).
Mounjaro 7,5 mg oplossing voor injectie in injectieflacon
Elke injectieflacon bevat 7,5 mg tirzepatide in 0,5 ml oplossing (15 mg/ml).
Mounjaro 10 mg oplossing voor injectie in injectieflacon
Elke injectieflacon bevat 10 mg tirzepatide in 0,5 ml oplossing (20 mg/ml).
Mounjaro 12,5 mg oplossing voor injectie in injectieflacon
Elke injectieflacon bevat 12,5 mg tirzepatide in 0,5 ml oplossing (25 mg/ml).
Mounjaro 15 mg oplossing voor injectie in injectieflacon
Elke injectieflacon bevat 15 mg tirzepatide in 0,5 ml oplossing (30 mg/ml).
Voorgevulde pen (KwikPen), meerdere doses
Mounjaro 2,5 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Elke dosis bevat 2,5 mg tirzepatide in 0,6 ml oplossing. Elke voorgevulde pen met meerdere doses bevat 10 mg tirzepatide in 2,4 ml (4,17 mg/ml). Elke pen levert 4 doses van 2,5 mg.
Mounjaro 5 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Elke dosis bevat 5 mg tirzepatide in 0,6 ml oplossing. Elke voorgevulde pen met meerdere doses bevat 20 mg tirzepatide in 2,4 ml (8,33 mg/ml). Elke pen levert 4 doses van 5 mg.
Mounjaro 7,5 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Elke dosis bevat 7,5 mg tirzepatide in 0,6 ml oplossing. Elke voorgevulde pen met meerdere doses bevat 30 mg tirzepatide in 2,4 ml (12,5 mg/ml). Elke pen levert 4 doses van 7,5 mg.
Mounjaro 10 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Elke dosis bevat 10 mg tirzepatide in 0,6 ml oplossing. Elke voorgevulde pen voor meerdere doses bevat 40 mg tirzepatide in 2,4 ml (16,7 mg/ml). Elke pen levert 4 doses van 10 mg.
Mounjaro 12,5 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Elke dosis bevat 12,5 mg tirzepatide in 0,6 ml oplossing. Elke voorgevulde pen voor meerdere doses bevat 50 mg tirzepatide in 2,4 ml (20,8 mg/ml). Elke pen levert 4 doses van 12,5 mg.
Mounjaro 15 mg/dosis KwikPen oplossing voor injectie in voorgevulde pen
Elke dosis bevat 15 mg tirzepatide in 0,6 ml oplossing. Elke voorgevulde pen met meerdere doses bevat 60 mg tirzepatide in 2,4 ml (25 mg/ml). Elke pen levert 4 doses van 15 mg.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie (injectie).
Heldere, kleurloze tot lichtgele oplossing.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Diabetes mellitus type 2
Mounjaro is geïndiceerd voor de behandeling van volwassenen, adolescenten en kinderen van 10 jaar en ouder met onvoldoende gereguleerde diabetes mellitus type 2, als aanvulling op dieet en lichaamsbeweging
- als monotherapie wanneer metformine ongeschikt wordt geacht vanwege intolerantie of contra-indicaties
- in aanvulling op andere geneesmiddelen voor de behandeling van diabetes.
Voor studieresultaten met betrekking tot combinaties, effecten op glykemische controle en de onderzochte populaties, zie rubriek 4.4, 4.5 en 5.1.
Gewichtsbeheersing
Mounjaro is geïndiceerd als aanvulling op een caloriearm dieet en verhoogde lichamelijke activiteit ten
behoeve van gewichtsbeheersing, inclusief gewichtsverlies en gewichtsbehoud, bij volwassenen met een aanvankelijke Body Mass Index (BMI) van
- ≥ 30 kg/m2 (obesitas) of
- ≥ 27 kg/m2 tot < 30 kg/m2 (overgewicht) die ten minste één gewichtsgerelateerde comorbide aandoening hebben (bijv. hypertensie, dyslipidemie, obstructieve slaapapneu, hart- en vaatziekten, prediabetes of diabetes mellitus type 2).
Voor onderzoeksresultaten met betrekking tot obstructieve slaapapneu (OSA) en hartfalen met behouden ejectiefractie (HFpEF), zie rubriek 5.1.
4.2 Dosering en wijze van toediening
Dosering
De startdosering van tirzepatide is 2,5 mg eenmaal per week. Na 4 weken moet de dosis worden verhoogd tot 5 mg eenmaal per week. Indien nodig kan de dosis worden verhoogd in stappen van 2,5 mg na minimaal 4 weken op de huidige dosering.
Volwassenen
De aanbevolen onderhoudsdoses zijn 5 mg, 10 mg en 15 mg.
De maximale dosering is 15 mg eenmaal per week.
Pediatrische patiënten van 10 jaar en ouder (behandeling van diabetes mellitus type 2)
De aanbevolen onderhoudsdoses zijn 5 mg en 10 mg.
De maximale dosering is 10 mg eenmaal per week.
Combinatietherapie
Wanneer tirzepatide wordt toegevoegd aan een bestaande behandeling met metformine en/of natrium-glucose-cotransporter (SGLT)-2-remmer, kan de huidige dosis metformine en/of SGLT-2-remmer worden voortgezet.
Wanneer tirzepatide wordt toegevoegd aan een bestaande therapie van een sulfonylureumderivaat en/of insuline, kan een verlaging van de dosis van het sulfonylureumderivaat of insuline worden overwogen om het risico op hypoglykemie te verlagen. Zelfcontrole van bloedglucose is noodzakelijk om de dosis van het sulfonylureumderivaat en insuline aan te passen. Een stapsgewijze dosisverlaging van insuline wordt aanbevolen (zie rubriek 4.4 en 4.8).
Gemiste doses
Als een dosis is vergeten, moet deze zo snel mogelijk binnen 4 dagen na de vergeten dosis worden toegediend. Als er meer dan 4 dagen zijn verstreken, sla dan de gemiste dosis over en dien de volgende dosis toe op de dag volgens het normale schema. In beide gevallen kunnen patiënten vervolgens hun normale doseringsschema van eenmaal per week hervatten.
Het doseringsschema wijzigen
De dag waarop de wekelijkse toediening plaatsvindt, kan indien nodig worden gewijzigd, zolang de tijd tussen twee doses ten minste 3 dagen is.
Speciale patiëntengroepen
Ouderen, geslacht, ras, etniciteit of lichaamsgewicht
Er is geen dosisaanpassing nodig op basis van leeftijd, geslacht, ras, etniciteit of lichaamsgewicht (zie rubriek 5.1 en 5.2). Er zijn slechts zeer beperkte gegevens beschikbaar van patiënten ≥ 85 jaar.
Nierfunctiestoornis
Er is geen dosisaanpassing nodig voor patiënten met een nierfunctiestoornis, waaronder eindstadium nierziekte (ESRD). Ervaring met het gebruik van tirzepatide bij patiënten met een ernstige nierfunctiestoornis en ESRD is beperkt. Voorzichtigheid is geboden bij de behandeling van deze patiënten met tirzepatide (zie rubriek 5.2).
Leverfunctiestoornis
Er is geen dosisaanpassing nodig voor patiënten met leverfunctiestoornis. Ervaring met het gebruik van tirzepatide bij patiënten met een ernstige leverfunctiestoornis is beperkt. Voorzichtigheid is geboden bij de behandeling van deze patiënten met tirzepatide (zie rubriek 5.2).
Pediatrische patiënten
Er is geen dosisaanpassing nodig op basis van leeftijd, geslacht, ras, etniciteit of lichaamsgewicht bij kinderen en adolescenten van 10 tot 18 jaar, die worden behandeld voor diabetes mellitus type 2. Er zijn geen gegevens beschikbaar voor kinderen en adolescenten met diabetes mellitus type 2 met een lichaamsgewicht < 50 kg of een BMI onder het 85e percentiel bij aanvang van de behandeling. Bij kinderen die < 60 kg wegen, is voorzichtigheid geboden bij het verhogen van de dosis naar 10 mg, omdat de veiligheidsgegevens beperkt zijn.
De veiligheid en werkzaamheid van tirzepatide zijn niet vastgesteld bij kinderen jonger dan 10 jaar voor de behandeling van diabetes mellitus type 2 en bij kinderen en adolescenten jonger dan 18 jaar voor gewichtsbeheersing.
Wijze van toediening
Mounjaro moet subcutaan in de buik of het bovenbeen worden geïnjecteerd, of iemand anders moet het in de achterkant van de bovenarm injecteren.
De dosis kan op elk moment van de dag worden toegediend, met of zonder maaltijden.
Injectieplaatsen moeten bij elke dosis worden gewisseld. Als een patiënt ook insuline injecteert, moet de patiënt Mounjaro op een andere injectieplaats injecteren.
Patiënten en hun verzorgers moet worden geadviseerd om de gebruikershandleiding, die bijgesloten is in de bijsluiter, zorgvuldig te lezen voordat het geneesmiddel wordt toegediend. Bij pediatrische patiënten mag een verzorger de injecties toedienen of de patiënt mag zichzelf injecteren als een zorgverlener vaststelt dat dit mogelijk is.
Voordat de Mounjaro KwikPen gebruikt wordt moet de gebruikershandleiding zorgvuldig gelezen worden.
Injectieflacon
Patiënten en hun verzorgers moeten instructie krijgen in de subcutane injectietechniek voor toediening van Mounjaro.
Voor meer informatie voorafgaand aan toediening, zie rubriek 6.6.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof(fen) of voor een van de in rubriek 6.1 vermelde hulpstof(fen).
4.8 Bijwerkingen
Samenvatting van veiligheidsprofiel
In 13 voltooide fase 3-studies werden 8.522 volwassen patiënten blootgesteld aan tirzepatide alleen of in combinatie met andere glucoseverlagende geneesmiddelen. De meest frequent gemelde bijwerkingen waren maagdarmstelselaandoeningen en deze reacties waren meestal licht of matig van ernst. De incidenties van nausea, diarree en braken waren hoger tijdens de dosisverhogingsperiode en namen in de loop van de tijd af (zie rubriek 4.2 en 4.4).
Lijst met bijwerkingen in tabelvorm
De volgende gerelateerde bijwerkingen uit klinische studies staan hieronder weergegeven volgens systeem/orgaanklasse en in volgorde van afnemende frequentie (zeer vaak: ≥ 1/10; vaak: ≥ 1/100 tot < 1/10; soms: ≥ 1/1.000 tot < 1/100; zelden: ≥ 1/10.000 tot < 1/1.000; zeer zelden: < 1/10.000). Binnen elke frequentiegroep worden de bijwerkingen weergegeven in volgorde van afnemende frequentie.
Tabel 1. Bijwerkingen
Systeem/ | Zeer vaak | Vaak | Soms | Zelden |
Immuunsysteem-aandoeningen |
| Overgevoeligheids-reacties |
| Anafylactische reactie#, Angio-oedeem# |
Voedings- en stofwisselings-stoornissen | Hypoglykemie1* bij gebruik met sulfonylureum‑ | Hypoglykemie1* bij gebruik met metformine en SGLT-2-remmer, Verminderde eetlust1 | Hypoglykemie1* bij gebruik met metformine6, Gewichtsverlies1 |
|
Zenuwstelsel- |
| Duizeligheid2 | Dysgeusie, |
|
Bloedvat-aandoeningen |
| Hypotensie2 |
|
|
Maagdarmstelsel-aandoeningen | Nausea, Diarree, Braken3, Abdominale pijn3, Constipatie4 | Dyspepsie, Opgezette buik, Oprispingen, Flatulentie, Gastro-oesofageale refluxziekte | Cholelithiasis, Cholecystitis, Acute pancreatitis, Vertraagde maaglediging |
|
Huid- en |
| Haaruitval2 |
|
|
Algemene aandoeningen en toedieningsplaats-stoornissen |
| Vermoeidheid†, Injectieplaatsreacties | Injectieplaatspijn |
|
Onderzoeken |
| Verhoogde hartslag, Verhoogde lipase, Verhoogde amylase, Bloed calcitonine verhoogd5 |
|
|
#Van post-marketing rapportages
*Hypoglykemie hieronder gedefinieerd.
†Vermoeidheid omvat de termen vermoeidheid, asthenie, malaise en lethargie.
1 Bijwerking die alleen van toepassing is op patiënten met diabetes mellitus type 2 (T2DM).
2 Bijwerking die voornamelijk van toepassing is op patiënten met overgewicht of obesitas, met of zonder T2DM.
3 Frequentie was zeer vaak in gewichtsbeheersings-, OSA- en HFpEF-studies en de T2DM-studie bij pediatrische patiënten en vaak in T2DM-studies bij volwassenen.
4 Frequentie was zeer vaak in gewichtsbeheersings-, OSA- en HFpEF-studies en vaak in T2DM-studies bij volwassenen en pediatrische patiënten.
5 Frequentie was vaak in gewichtsbeheersings- en HFpEF-studies, soms in T2DM- en OSA-studies bij volwassenen en zeer zelden in de T2DM-studie bij pediatrische patiënten.
6 Frequentie was vaak in de T2DM-studie bij pediatrische patiënten.
Beschrijving van geselecteerde bijwerkingen
Overgevoeligheidsreacties
Overgevoeligheidsreacties zijn gemeld met tirzepatide in gepoolde placebogecontroleerde T2DM-studies bij volwassenen, gepoolde placebogecontroleerde gewichtsbeheersingsstudies, gepoolde placebogecontroleerde OSA-studies en in de placebogecontroleerde HFpEF-studie. Soms waren deze ernstig (bijv. urticaria, eczeem, uitslag, dermatitis). Overgevoeligheidsreacties werden gemeld bij respectievelijk 3,2%, 5,0%, 3,0% en 4,7% van de met tirzepatide behandelde patiënten, vergeleken met respectievelijk 1,7%, 3,8%, 2,1% en 3,5% van de met placebo behandelde patiënten.
Gevallen van anafylactische reactie en angio-oedeem zijn zelden gemeld bij gebruik van tirzepatide in de markt.
Hypoglykemie bij patiënten met diabetes mellitus type 2
Diabetes type 2-studies bij volwassenen
Klinisch significante hypoglykemie (bloedglucose < 3,0 mmol/l (< 54 mg/dl)) of ernstige hypoglykemie (waarbij de hulp van een andere persoon nodig is) trad op bij 10 tot 14% (0,14 tot 0,16 voorvallen/patiëntjaar) van de patiënten wanneer tirzepatide werd toegevoegd aan een sulfonylureumderivaat en bij 14 tot 19% (0,43 tot 0,64 voorvallen/patiëntjaar) van de patiënten wanneer tirzepatide werd toegevoegd aan basale insuline.
De mate van klinisch significante hypoglykemie bij gebruik van tirzepatide als monotherapie of bij toevoeging aan andere orale bloedglucoseverlagende geneesmiddelen was maximaal 0,04 voorvallen/patiëntjaar (zie tabel 1 en rubriek 4.2, 4.4 en 5.1).
In klinische fase 3-studies rapporteerden 10 (0,2%) patiënten 12 episoden van ernstige hypoglykemie. Van deze 10 patiënten gebruikten 5 (0,1%) gelijktijdig insuline glargine of een sulfonylureumderivaat, die ieder 1 episode rapporteerden.
Gewichtsbeheersingsstudie
In een placebogecontroleerde fase 3-gewichtsbeheersingsstudie bij patiënten met T2DM werd hypoglykemie (bloedglucose < 3,0 mmol/l (< 54 mg/dl)) gemeld bij 4,2% van de met tirzepatide behandelde patiënten versus 1,3% van de met placebo behandelde patiënten. In deze studie hadden patiënten die tirzepatide gebruikten in combinatie met een insulinesecretagoog (bijv. sulfonylureumderivaat) een hogere incidentie van hypoglykemie (10,3%) in vergelijking met de met tirzepatide behandelde patiënten die geen sulfonylureumderivaat gebruikten (2,1%). Er werden geen episodes van ernstige hypoglykemie gemeld.
Gastro-intestinale bijwerkingen
In gepoolde placebogecontroleerde fase 3-T2DM-studies bij volwassenen waren gastro-intestinale aandoeningen dosisafhankelijk verhoogd voor tirzepatide 5 mg (37,1%), 10 mg (39,6%) en 15 mg (43,6%) vergeleken met placebo (20,4%). Nausea trad op bij 12,2%, 15,4% en 18,3% versus 4,3% en diarree trad op bij 11,8%, 13,3% en 16,2% versus 8,9% voor tirzepatide 5 mg, 10 mg en 15 mg versus placebo. Gastro-intestinale bijwerkingen waren meestal licht (74%) of matig (23,3%) van ernst. De frequentie van nausea, braken en diarree was hoger tijdens de dosisescalatieperiode en nam in de loop van de tijd af.
Er waren meer patiënten in de groepen met tirzepatide 5 mg (3,0%), 10 mg (5,4%) en 15 mg (6,6%) die permanent de behandeling staakten vanwege het gastro-intestinale voorval dan in de placebogroep (0,4%).
In een placebogecontroleerde fase 3-gewichtsbeheersingsstudie bij patiënten zonder T2DM, waren gastro-intestinale aandoeningen verhoogd voor tirzepatide 5 mg (55,6%), 10 mg (60,8%) en 15 mg (59,2%) vergeleken met placebo (30,3%). Nausea trad op bij 24,6%, 33,3% en 31,0% versus 9,5% en diarree trad op bij 18,7%, 21,2% en 23,0% versus 7,3% voor respectievelijk tirzepatide 5 mg, 10 mg en 15 mg versus placebo. Gastro-intestinale bijwerkingen waren meestal licht (60,8%) of matig (34,6%) van ernst. De frequentie van nausea, braken en diarree was hoger tijdens de dosisescalatieperiode en nam in de loop van de tijd af.
Er waren meer patiënten in de groepen met tirzepatide 5 mg (1,9%), 10 mg (4,4%) en 15 mg (4,1%) die permanent de studiebehandeling staakten vanwege het gastro-intestinale voorval dan in de placebogroep (0,5%).
Galblaasgerelateerde gebeurtenissen
In gepoolde placebogecontroleerde fase 3-gewichtsbeheersingsstudies was de totale incidentie van cholecystitis en acute cholecystitis respectievelijk 0,6% en 0,2% voor met tirzepatide en placebo behandelde patiënten.
In gepoolde placebogecontroleerde fase 3-gewichtsbeheersingsstudies, in gepoolde placebogecontroleerde fase 3-OSA-studies en in een placebogecontroleerde fase 3-HFpEF-studie, werd acute galblaasziekte gemeld bij respectievelijk 2,0%, 0,9% en 4,4% van de met tirzepatide behandelde patiënten en bij respectievelijk 1,6%, 0,9% en 2,7% van de met placebo behandelde patiënten.
In de fase 3-gewichtsbeheersingsstudies waren acute galblaasgerelateerde gebeurtenissen positief geassocieerd met gewichtsvermindering.
Immunogeniciteit
In klinische fase 3-studies werden in totaal 9.094 met tirzepatide behandelde patiënten beoordeeld op anti-drug antilichamen (ADA). In deze studies ontwikkelde 45,1-65,1% van de patiënten ADA tijdens de behandelperiode (treatment-emergent ADA- TE ADA). Bij 29,8-51,3% van de beoordeelde patiënten bleven TE ADA aanwezig gedurende een periode van 16 weken of langer. Van deze patiënten had maximaal 3% neutraliserende antilichamen tegen tirzepatide-activiteit op de receptoren voor glucose-afhankelijke insulinotrope polypeptide (GIP) en 2,3% op de receptoren voor glucagon-achtige peptide-1 (GLP‑1). Daarnaast had maximaal 1,2% van de patiënten neutraliserende antilichamen tegen lichaamseigen GIP en 0,4% tegen lichaamseigen GLP-1.
Er was geen bewijs voor een veranderd farmacokinetisch profiel of een invloed op de werkzaamheid van tirzepatide gerelateerd aan de ontwikkeling van ADA of neutraliserende antilichamen.
Hartslag
In gepoolde placebogecontroleerde fase 3-T2DM-studies bij volwassen patiënten, resulteerde behandeling met tirzepatide in een maximaal gemiddelde verhoging van de hartslag van 3 tot 5 slagen per minuut (spm) over de verschillende doseringen. De maximaal gemiddelde verhoging van de hartslag bij met placebo behandelde patiënten was 1 slag per minuut.
Het percentage patiënten dat een verandering van de hartslagfrequentie bij baseline van > 20 spm bij 2 of meer opeenvolgende bezoeken had, was respectievelijk 2,1%, 3,8% en 2,9% voor tirzepatide 5 mg, 10 mg en 15 mg, vergeleken met 2,1% voor placebo.
Er werden kleine gemiddelde verhogingen van het PR-interval waargenomen bij behandeling met tirzepatide in vergelijking met placebo (respectievelijk gemiddelde verhoging van 1,4 tot 3,2 msec en gemiddelde daling van 1,4 msec). Er werd geen verschil in aritmie en tijdens de behandeling optredende cardiale geleidingsstoornissen waargenomen tussen tirzepatide 5 mg, 10 mg, 15 mg en placebo (respectievelijk 3,8%, 2,1%, 3,7% en 3%).
In gepoolde placebogecontroleerde fase 3-gewichtsbeheersingsstudies, in gepoolde placebogecontroleerde fase 3-OSA-studies en in een placebogecontroleerde fase 3-HFpEF-studie, resulteerde behandeling met tirzepatide in een gemiddelde verhoging van de hartslag van respectievelijk 3, 2 en 3 slagen per minuut. Er was een gemiddelde verhoging van de hartslag van respectievelijk < 1, < 1 en 1 slag per minuut bij met placebo behandelde patiënten.
In een placebogecontroleerde gewichtsbeheersingsstudie bij patiënten zonder T2DM was het percentage patiënten, dat een verandering van de hartslagfrequentie ten opzichte van baseline van > 20 spm bij 2 of meer opeenvolgende bezoeken had, respectievelijk 2,4%, 4,9% en 6,3% voor tirzepatide 5 mg, 10 mg en 15 mg, vergeleken met 1,2% voor placebo. Er werden kleine gemiddelde verhogingen van het PR-interval waargenomen bij behandeling met tirzepatide en placebo (gemiddelde verhoging van respectievelijk 0,3 tot 1,4 msec en van 0,5 msec). Er werd geen verschil in aritmie en tijdens de behandeling optredende cardiale geleidingsstoornis waargenomen tussen tirzepatide 5 mg, 10 mg, 15 mg en placebo (respectievelijk 3,7%, 3,3%, 3,3% en 3,6%).
Injectieplaatsreacties
In gepoolde placebogecontroleerde fase 3-T2DM-studies bij volwassen patiënten, in gepoolde placebogecontroleerde fase 3-gewichtsbeheersingsstudies, in gepoolde placebogecontroleerde fase 3-OSA-studies en in een placebogecontroleerde fase 3-HFpEF-studie, waren de injectieplaatsreacties verhoogd voor tirzepatide (respectievelijk 3,2%, 8,0%, 8,2% en 6,0%) vergeleken met placebo (respectievelijk 0,4%, 1,8%, 2,6% en 1,6%).
Over het algemeen waren in fase 3-studies de meest voorkomende tekenen en symptomen van de injectieplaatsreacties erytheem en pruritus. De maximale ernst van de injectieplaatsreacties voor patiënten was licht (91%) of matig (9%). Er waren geen ernstige injectieplaatsreacties.
Pancreasenzymen
In gepoolde placebogecontroleerde fase 3-T2DM-studies resulteerde behandeling met tirzepatide bij volwassen patiënten in gemiddelde verhogingen ten opzichte van baseline van 33% tot 38% in pancreasamylase en van 31% tot 42% in lipase over de verschillende doseringen. Met placebo behandelde patiënten hadden een stijging in amylase van 4% ten opzichte van baseline en er werden geen veranderingen waargenomen in lipase.
In gepoolde placebogecontroleerde fase 3-gewichtsbeheersingsstudies, in gepoolde placebogecontroleerde fase 3-OSA-studies en in een placebogecontroleerde fase 3-HFpEF-studie, resulteerde behandeling met tirzepatide in gemiddelde verhogingen ten opzichte van baseline van respectievelijk 23%, 25% en 28% in pancreasamylase en van respectievelijk 34%, 39% en 32% in lipase. Met placebo behandelde patiënten hadden een stijging in amylase van respectievelijk 2%, 1% en 4% ten opzichte van baseline en van respectievelijk 6%, 4% en 1% in lipase.
Pediatrische patiënten
De veiligheids- en immunogeniciteitsprofielen bij kinderen en adolescenten van 10 tot 18 jaar met T2DM die eenmaal per week werden behandeld met 5 mg en 10 mg tirzepatide, waren consistent met die hierboven beschreven voor volwassen patiënten met T2DM, met uitzondering van een hogere frequentie van braken, buikpijn en hypoglykemie in combinatie met alleen metformine.
Tijdens de T2DM-studie bij pediatrische patiënten traden geen ernstige hypoglykemische episodes op. Tijdens de placebogecontroleerde fase trad klinisch significante hypoglykemie (bloedglucose < 3,0 mmol/l (< 54 mg/dl)) op bij 28,6% (1,98 voorvallen/patiëntjaar) van de patiënten behandeld met tirzepatide en bij 10,0% (0,35 voorvallen/patiëntjaar) van de met placebo behandelde patiënten, wanneer toegevoegd aan basale insuline met of zonder metformine. Het percentage was respectievelijk 9,1% (0,28 voorvallen/patiëntjaar) en 4,2% (0,07 voorvallen/patiëntjaar) voor met tirzepatide en met placebo behandelde patiënten, in combinatie met alleen metformine.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten, www.fagg.be, Afdeling Vigilantie: Website: www.eenbijwerkingmelden.be, e-mail: adr@fagg-afmps.be.
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Eli Lilly Nederland B.V., Orteliuslaan 1000, 3528 BD Utrecht, Nederland.
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/22/1685/001
EU/1/22/1685/002
EU/1/22/1685/003
EU/1/22/1685/004
EU/1/22/1685/005
EU/1/22/1685/006
EU/1/22/1685/007
EU/1/22/1685/008
EU/1/22/1685/009
EU/1/22/1685/010
EU/1/22/1685/011
EU/1/22/1685/012
EU/1/22/1685/013
EU/1/22/1685/014
EU/1/22/1685/015
EU/1/22/1685/016
EU/1/22/1685/017
EU/1/22/1685/018
EU/1/22/1685/019
EU/1/22/1685/020
EU/1/22/1685/021
EU/1/22/1685/022
EU/1/22/1685/023
EU/1/22/1685/024
EU/1/22/1685/025
EU/1/22/1685/026
EU/1/22/1685/027
EU/1/22/1685/028
EU/1/22/1685/029
EU/1/22/1685/030
EU/1/22/1685/031
EU/1/22/1685/032
EU/1/22/1685/033
EU/1/22/1685/034
EU/1/22/1685/035
EU/1/22/1685/036
EU/1/22/1685/037
EU/1/22/1685/038
EU/1/22/1685/039
EU/1/22/1685/040
EU/1/22/1685/041
EU/1/22/1685/042
EU/1/22/1685/043
EU/1/22/1685/044
EU/1/22/1685/045
EU/1/22/1685/046
EU/1/22/1685/047
EU/1/22/1685/048
EU/1/22/1685/049
EU/1/22/1685/050
EU/1/22/1685/051
EU/1/22/1685/052
EU/1/22/1685/053
EU/1/22/1685/054
EU/1/22/1685/055
EU/1/22/1685/056
EU/1/22/1685/057
EU/1/22/1685/058
EU/1/22/1685/059
EU/1/22/1685/060
10. DATUM VAN HERZIENING VAN DE TEKST 29 JANUARI 2026.
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
AFLEVERINGSWIJZE Geneesmiddel op medisch voorschrift.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4862058 | MOUNJARO 2,5MG KWIKPEN OPL INJ VOORGEV.PEN 0,6ML | € 179,78 | - | Ja | € 2 | € 1 | |
| 4862066 | MOUNJARO 5,0MG KWIKPEN OPL INJ VOORGEV.PEN 0,6ML | € 241,16 | - | Ja | € 2 | € 1 | |
| 4862074 | MOUNJARO 7,5MG KWIKPEN OPL INJ VOORGEV.PEN 0,6ML | € 333,23 | - | Ja | € 2 | € 1 | |
| 4862082 | MOUNJARO 10,0MG KWIKPEN OPL INJ VOORGEV.PEN 0,6ML | € 333,23 | - | Ja | € 2 | € 1 | |
| 4862090 | MOUNJARO 12,5MG KWIKPEN OPL INJ VOORGEV.PEN 0,6ML | € 410,88 | - | Ja | - | - | |
| 4862108 | MOUNJARO 15,0MG KWIKPEN OPL INJ VOORGEV.PEN 0,6ML | € 410,88 | - | Ja | - | - |
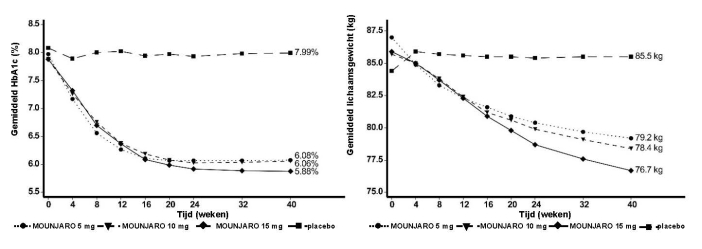
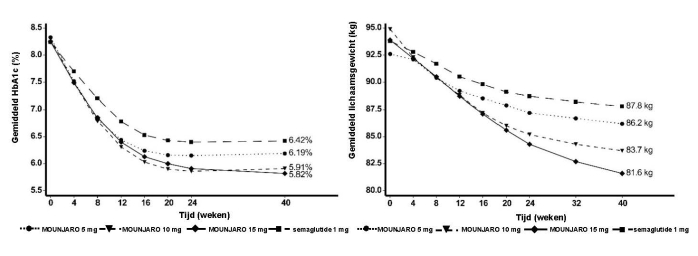
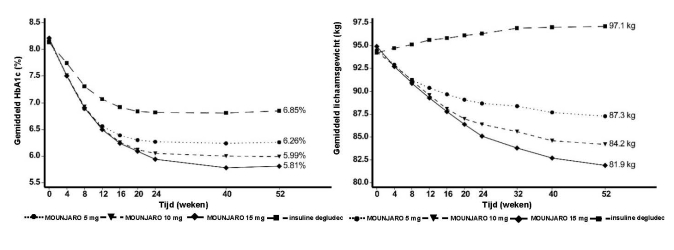
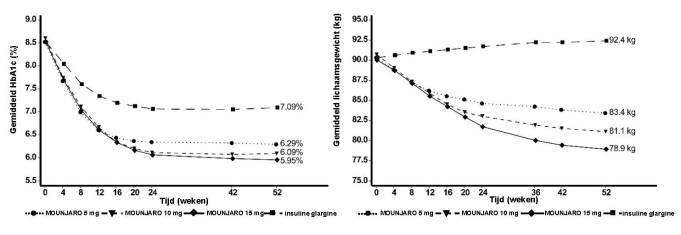
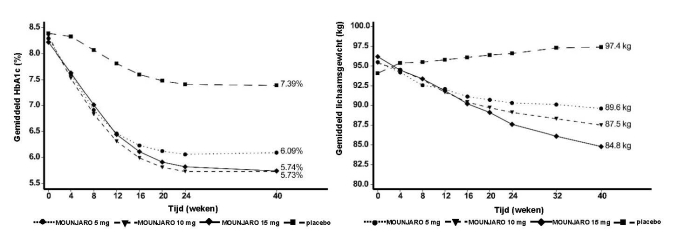
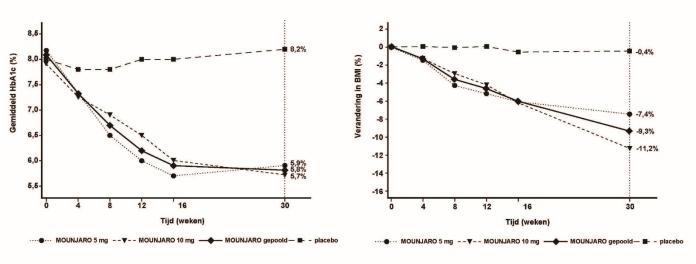 Figuur 6. Gemiddeld HbA1c (%) en verandering in BMI (%) ten opzichte van baseline tot week 30
Figuur 6. Gemiddeld HbA1c (%) en verandering in BMI (%) ten opzichte van baseline tot week 30