![]() Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
1. NAAM VAN HET GENEESMIDDEL
SOTYKTU 6 mg filmomhulde tabletten
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke filmomhulde tablet bevat 6 mg deucravacitinib.
Hulpstoffen met bekend effect
Elke filmomhulde tablet bevat 44 mg lactose (zie rubriek 4.4).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Filmomhulde tablet (tablet)
Roze, ronde, biconvexe, filmomhulde tablet met een diameter van 8 mm, bedrukt met ‘BMS 895’ en ‘6 mg’ aan één kant op twee regels, effen aan de andere kant.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
SOTYKTU is geïndiceerd voor de behandeling van matige tot ernstige plaque‑psoriasis bij volwassenen die in aanmerking komen voor systemische behandeling.
4.2 Dosering en wijze van toediening
Behandeling moet worden gestart onder de begeleiding en het toezicht van een arts die ervaring heeft met het diagnosticeren en behandelen van psoriasis.
Dosering
De aanbevolen dosis is 6 mg, eenmaal daags oraal ingenomen.
Als een patiënt na 24 weken behandeling geen verbetering vertoont, moet beëindiging van de behandeling worden overwogen. De respons van de patiënt op de behandeling moet regelmatig beoordeeld worden.
Bijzondere populaties
Ouderen
Er is geen dosisaanpassing nodig voor oudere patiënten van 65 jaar en ouder (zie rubriek 5.2). Er is zeer beperkte klinische ervaring met patiënten ≥ 75 jaar en deucravacitinib moet met voorzichtigheid worden gebruikt bij deze groep patiënten.
Nierfunctiestoornissen
Er is geen dosisaanpassing nodig voor patiënten met een nierfunctiestoornis, inclusief patiënten met eindstadium nierfalen (ESRD) die dialyseren (zie rubriek 5.2).
Leverfunctiestoornissen
Er is geen dosisaanpassing nodig voor patiënten met een lichte tot matige leverfunctiestoornis. Gebruik van deucravacitinib wordt niet aanbevolen bij patiënten met een ernstige leverfunctiestoornis (zie rubriek 5.2).
Pediatrische patiënten
De veiligheid en werkzaamheid van deucravacitinib bij kinderen en jongeren onder de 18 jaar zijn nog niet vastgesteld. Er zijn geen gegevens beschikbaar.
Wijze van toediening
Voor oraal gebruik.
Tabletten kunnen met of zonder voedsel worden ingenomen. Tabletten moeten heel worden doorgeslikt en mogen niet worden vermalen, gesneden of gekauwd.
4.3 Contra‑indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
Klinisch belangrijke, actieve infecties (bijv. actieve tuberculose, zie rubriek 4.4).
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De vaakst gemelde bijwerking is bovensteluchtweginfectie (18,9%), in de meeste gevallen nasofaryngitis. Het veiligheidsprofiel van deucravacitinib op de lange termijn was vergelijkbaar en in overeenstemming met eerdere ervaring.
Lijst met bijwerkingen in tabelvorm
De volgende lijst met bijwerkingen van deucravacitinib is afkomstig van klinische onderzoeken bij plaque‑psoriasis (tabel 1). Deze bijwerkingen worden weergegeven volgens de MedDRA systeem/orgaanklassen en per frequentie.
Frequenties worden gedefinieerd als: zeer vaak (≥ 1/10); vaak (≥ 1/100, < 1/10); soms (≥ 1/1.000, < 1/100); zelden (≥ 1/10.000, < 1/1.000); zeer zelden (< 1/10.000); niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Tabel 1: Lijst met bijwerkingen
Systeem/orgaanklasse | Frequentie | Bijwerking |
Infecties en parasitaire aandoeningen | Zeer vaak | Bovensteluchtweginfectiesa |
Vaak | Herpes-simplexinfectiesb | |
Soms | Herpes zoster | |
Maagdarmstelselaandoeningen | Vaak | Orale ulceratiec |
Huid- en onderhuidaandoeningen | Vaak | Acneïforme rashd |
Onderzoeken | Vaak | Verhoogd creatinefosfokinase in het bloed |
a Bovensteluchtweginfecties omvatten nasofaryngitis, bovensteluchtweginfectie, virale bovensteluchtweginfectie, faryngitis, sinusitis, acute sinusitis, rhinitis, tonsillitis, peritonsillair abces, laryngitis, tracheïtis en rhinotracheïtis. | ||
Beschrijving van geselecteerde bijwerkingen
Infecties
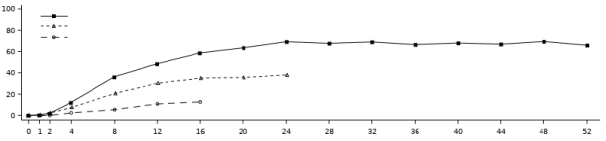
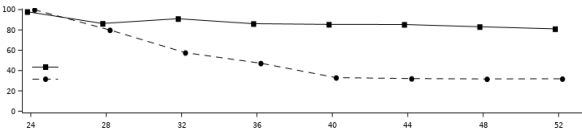
In de onderzoeken POETYK PSO‑1 en POETYK PSO‑2 (zie rubriek 5.1), kwamen infecties voor bij 29,1% van de patiënten in de deucravacitinibgroep (116,0 voorvallen per 100 persoonjaren) vergeleken met 21,5% van de patiënten in de placebogroep (83,7 voorvallen per 100 persoonjaren) tijdens de eerste 16 weken. De meerderheid van de infecties was niet ernstig en licht tot matig in ernst en heeft niet geleid tot het staken van deucravacitinib. De incidentie van ernstige infecties was 0,6% in de deucravacitinibgroep (2,0 voorvallen per 100 persoonjaren) en 0,5% in de placebogroep (1,6 voorvallen per 100 persoonjaren).
Het percentage infecties in de deucravacitinibgroep nam tot en met week 52 niet toe (95,4 voorvallen per 100 persoonjaren). Het percentage ernstige infecties in de deucravacitinibgroep nam tot en met week 52 niet toe (1,7 voorvallen per 100 persoonjaren).
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem zoals vermeld in aanhangsel V.
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Bristol-Myers Squibb Pharma EEIG
Plaza 254
Blanchardstown Corporate Park 2
Dublin 15, D15 T867
Ierland
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/23/1718/001
EU/1/23/1718/002
EU/1/23/1718/003
EU/1/23/1718/004
EU/1/23/1718/005
EU/1/23/1718/006
EU/1/23/1718/007
EU/1/23/1718/008
10. DATUM VAN HERZIENING VAN DE TEKST
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau http://www.ema.europa.eu.
.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4697421 | SOTYKTU 6 mg 28 filmomhulde tabletten | € 723,51 | - | Ja | € 12,8 | € 8,5 |