SAMENVATTING VAN DE PRODUCTKENMERKEN
![]() Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
1. NAAM VAN HET GENEESMIDDEL
Qdenga poeder en oplosmiddel voor oplossing voor injectie
Qdenga poeder en oplosmiddel voor oplossing voor injectie in een voorgevulde spuit
Tetravalent vaccin (levend, verzwakt) tegen dengue
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Na reconstitutie bevat 1 dosis (0,5 ml):
Denguevirus serotype 1 (levend, verzwakt)*: ≥ 3,3 log10 PFU**/dosis
Denguevirus serotype 2 (levend, verzwakt)#: ≥ 2,7 log10 PFU**/dosis
Denguevirus serotype 3 (levend, verzwakt)*: ≥ 4,0 log10 PFU**/dosis
Denguevirus serotype 4 (levend, verzwakt)*: ≥ 4,5 log10 PFU**/dosis
*Geproduceerd in Vero-cellen met behulp van recombinant-DNA-technologie. Genen van serotype-specifieke oppervlakte-eiwitten, ontworpen in dengue type-2 basis. Dit product bevat genetisch gemodificeerde organismen (GMO’s, genetically modified organisms).
#Geproduceerd in Vero-cellen met behulp van recombinant-DNA-technologie
**PFU = Plaquevormende eenheden
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Poeder en oplosmiddel voor oplossing voor injectie.
Voorafgaand aan reconstitutie is het vaccin een wit tot gebroken wit gevriesdroogd poeder (compacte cake).
Het oplosmiddel is een heldere, kleurloze oplossing.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Qdenga is geïndiceerd voor de preventie van dengue bij personen vanaf 4 jaar.
Qdenga dient te worden gebruikt in overeenstemming met de officiële aanbevelingen.
4.2 Dosering en wijze van toediening
Dosering
Personen vanaf 4 jaar
Qdenga moet worden toegediend als een 0,5 ml dosis met een schema van twee doses (0 en 3 maanden).
De noodzaak voor een herhalingsdosis is niet vastgesteld.
Andere pediatrische patiënten (kinderen < 4 jaar)
De veiligheid en werkzaamheid van Qdenga bij kinderen jonger dan 4 jaar zijn nog niet vastgesteld.
De momenteel beschikbare gegevens worden beschreven in rubriek 4.8, maar er kan geen doseringsadvies worden gegeven.
Ouderen
Dosisaanpassing is niet vereist bij personen van 60 jaar of ouder. Zie rubriek 4.4.
Wijze van toediening
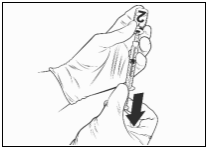
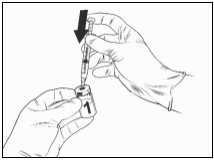
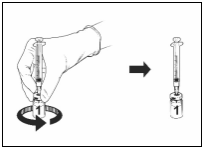
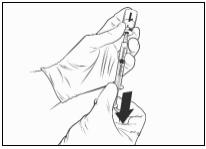
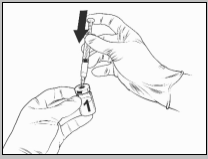
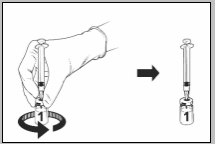
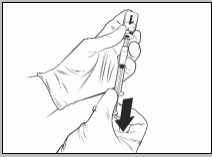
Na volledige reconstitutie van het gelyofiliseerde vaccin met het oplosmiddel moet Qdenga worden toegediend door subcutane injectie, bij voorkeur in de bovenarm nabij de deltaspier.
Qdenga niet toedienen via intravasculaire, intradermale of intramusculaire injectie.
Het vaccin mag niet met andere vaccins of andere parenterale geneesmiddelen in dezelfde spuit worden gemengd.
Voor instructies over reconstitutie van Qdenga voorafgaand aan toediening, zie rubriek 6.6.
4.3 Contra-indicaties
- Overgevoeligheid voor de werkzame stoffen of voor een van de in rubriek 6.1 vermelde hulpstoffen of overgevoeligheid voor een eerdere dosis Qdenga.
- Personen met aangeboren of verworven immuundeficiëntie, met inbegrip van personen die immunosuppressieve therapieën ontvangen zoals hoge doses systemische corticosteroïden (bijv. 20 mg/dag of 2 mg/kg lichaamsgewicht/dag prednison gedurende 2 weken of meer) binnen 4 weken vóór vaccinatie, of andere geneesmiddelen met bekende immunosuppressieve eigenschappen, waaronder chemotherapie. Er moet per persoon worden bekeken wanneer vaccinatie na immunosuppresieve behandeling moet worden vermeden.
- Personen met een symptomatische hiv-infectie of met een asymptomatische hiv-infectie met daarbij bewijs van een verstoord immuunsysteem.
- Zwangere vrouwen (zie rubriek 4.6).
- Vrouwen die borstvoeding geven (zie rubriek 4.6).
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
In klinische onderzoeken waren de meest gemelde bijwerkingen bij proefpersonen van 4 tot 60 jaar oud pijn op de injectieplaats (50%), hoofdpijn (35%), myalgie (31%), erytheem op de injectieplaats (27%), malaise (24%), asthenie (20%) en koorts (11%).
Deze bijwerkingen traden gewoonlijk op binnen 2 dagen na de injectie, waren licht tot matig in intensiteit, van korte duur (1 tot 3 dagen) en kwamen minder frequent voor na de tweede injectie van Qdenga dan na de eerste injectie.
Vaccinviremie
In klinisch onderzoek DEN-205 werd voorbijgaande vaccinviremie na vaccinatie met Qdenga waargenomen bij 49% van de onderzoeksdeelnemers die nog niet eerder waren besmet met dengue en bij 16% van de onderzoeksdeelnemers die eerder besmet waren geweest met dengue. Vaccinviremie begon meestal in de tweede week na de eerste injectie en had een gemiddelde duur van 4 dagen. Vaccinviremie ging bij sommige proefpersonen gepaard met voorbijgaande, lichte tot matige symptomen, zoals hoofdpijn, artralgie, myalgie en huiduitslag, die ook kunnen voorkomen bij dengue. Vaccinviremie werd zelden waargenomen na de tweede dosis.
Diagnostische tests voor dengue zijn mogelijk positief tijdens vaccinviremie en kunnen niet worden gebruikt om vaccinviremie te onderscheiden van een infectie met wildtype dengue.
Tabel met lijst van bijwerkingen
Bijwerkingen in verband met Qdenga verkregen uit klinisch onderzoek en ervaring na toekenning van de handelsvergunning worden opgesomd in de tabel hieronder (Tabel 1).
Het veiligheidsprofiel dat hieronder staat weergegeven, is gebaseerd op gegevens die zijn verkregen uit placebogecontroleerde klinische onderzoeken en ervaring na toekenning van de handelsvergunning. De gepoolde analyse van klinische onderzoeken omvatte gegevens van 14.627 onderzoeksdeelnemers in de leeftijd van 4 tot 60 jaar (13.839 kinderen en 788 volwassenen) die zijn gevaccineerd met Qdenga. Dit omvatte een reactogeniciteitsubgroep van 3.830 deelnemers (3.042 kinderen en 788 volwassenen).
De bijwerkingen worden vermeld in overeenstemming met de volgende frequentiecategorieën:
Zeer vaak: 1/10
Vaak: 1/100, <1/10
Soms: 1/1.000, <1/100
Zelden: 1/10.000, <1/1.000
Zeer zelden: <1/10.000
Niet bekend: kan met de beschikbare gegevens niet worden bepaald
Tabel 1: Bijwerkingen tijdens klinische onderzoeken (leeftijd 4 tot 60 jaar) en ervaring na toekenning van de handelsvergunning (leeftijd 4 jaar en ouder)
Systeem/orgaanklasse volgens MedDRA | Frequentie | Bijwerkingen |
Infecties en parasitaire aandoeningen | Zeer vaak | Infectie van de bovenste luchtwegena |
Vaak | Nasofaryngitis | |
Soms | Bronchitis | |
Bloed- en lymfestelselaandoeningen | Zeer zelden | Trombocytopeniec |
Immuunsysteemaandoeningen | Niet bekend | Anafylactische reactie, waaronder anafylactische shockc |
Voedings- en stofwisselingsstoornissen | Zeer vaak | Verminderde eetlustd |
Psychische stoornissen | Zeer vaak | Prikkelbaarheidd |
Zenuwstelselaandoeningen | Zeer vaak | Hoofdpijn |
Soms | Duizeligheid | |
Oogaandoeningen | Niet bekend | Oogpijnc |
Maagdarmstelselaandoeningen | Soms | Diarree |
Huid- en onderhuidaandoeningen | Soms | Uitslage |
Zelden | Petechiaec | |
Zeer zelden | Angio-oedeem | |
Skeletspierstelsel- en bindweefselaandoeningen | Zeer vaak | Myalgie |
Vaak | Artralgie | |
Algemene aandoeningen en toedieningsplaatsstoornissen | Zeer vaak | Pijn op de injectieplaats |
Vaak | Zwelling op de injectieplaats | |
Soms | Bloeding op de injectieplaatsf |
a Inclusief infectie van de bovenste luchtwegen en virusinfectie van de bovenste luchtwegen
b Inclusief faryngotonsillitis en tonsillitis
c Bijwerkingen waargenomen na toekenning van de handelsvergunning
d In klinische onderzoeken waargenomen bij kinderen jonger dan 6 jaar
e Inclusief huiduitslag, virale huiduitslag, maculopapulaire uitslag, pruritische huiduitslag
f Bij volwassenen gemeld in klinische onderzoeken
Pediatrische patiënten
Pediatrische gegevens van proefpersonen van 4 tot 17 jaar
Samengevoegde veiligheidsgegevens uit klinische onderzoeken zijn beschikbaar voor 13.839 kinderen (9.210 in de leeftijd van 4 tot 11 jaar en 4.629 tussen de 12 en 17 jaar). Dit omvat reactogeniciteitsgegevens verzameld bij 3.042 kinderen (1.865 in de leeftijd van 4 tot 11 jaar en 1.177 tussen de 12 en 17 jaar).
Frequentie, type en ernst van bijwerkingen bij kinderen kwamen grotendeels overeen met die voor volwassenen. Bijwerkingen die vaker werden gemeld bij kinderen dan bij volwassenen waren koorts (11% tegenover 3%), infectie van de bovenste luchtwegen (11% tegenover 3%), nasofaryngitis (6% tegenover 0,6%), faryngotonsillitis (2% tegenover 0,3%) en griepachtige ziekte (1% tegenover 0,1%). Bijwerkingen die minder vaak werden gemeld bij kinderen dan bij volwassenen waren erytheem op de injectieplaats (2% tegenover 27%), misselijkheid (0,03% tegenover 0,8%) en artralgie (0,03% tegenover 1%).
De volgende reacties werden waargenomen bij 357 kinderen jonger dan 6 jaar die werden gevaccineerd met Qdenga:
verminderde eetlust (17%), somnolentie (13%) en prikkelbaarheid (12%).
Pediatrische gegevens van proefpersonen jonger dan 4 jaar, d.w.z. buiten de leeftijdsindicatie
Reactogeniciteit bij proefpersonen jonger dan 4 jaar werd beoordeeld bij 78 proefpersonen die ten minste één dosis Qdenga hadden ontvangen, van wie 13 proefpersonen het geïndiceerde regime van twee doses hadden ontvangen. De zeer vaak gemelde reacties waren prikkelbaarheid (25%), koorts (17%), pijn op de injectieplaats (17%) en verlies van eetlust (15%). Somnolentie (8%) en erytheem op de injectieplaats (3%) werden vaak gemeld. Zwelling op de injectieplaats werd niet waargenomen bij patiënten jonger dan 4 jaar.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Takeda Pharmaceuticals International AG Ireland Branch
Block 2 Miesian Plaza
50-58 Baggot Street Lower
Dublin 2
D02 HW68
Ierland
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/22/1699/001
EU/1/22/1699/002
EU/1/22/1699/003
EU/1/22/1699/004
EU/1/22/1699/005
EU/1/22/1699/006
10. DATUM VAN HERZIENING VAN DE TEKST
12/2025
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4642039 | QDENGA PDR&SOLV.1VOORGEV.SP.+2AIG+OPL INJ 1FL0,5ML | € 89,7 | - | Ja | - | - |