SAMENVATTING VAN DE PRODUCTKENMERKEN
![]() Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
Dit geneesmiddel is onderworpen aan aanvullende monitoring. Daardoor kan snel nieuwe veiligheidsinformatie worden vastgesteld. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden. Zie rubriek 4.8 voor het rapporteren van bijwerkingen.
1. NAAM VAN HET GENEESMIDDEL
Tezspire 210 mg oplossing voor injectie in een voorgevulde spuit
Tezspire 210 mg oplossing voor injectie in een voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Voorgevulde spuit
Elke voorgevulde spuit bevat 210 mg tezepelumab in 1,91 ml oplossing (110 mg/ml).
Voorgevulde pen
Elke voorgevulde pen bevat 210 mg tezepelumab in 1,91 ml oplossing (110 mg/ml).
Tezepelumab is een humaan monoklonaal antilichaam dat geproduceerd wordt in ovariumcellen van de Chinese hamster (Chinese hamster ovary, CHO) met behulp van recombinant-DNA-technologie.
Hulpstoffen met bekend effect
Dit geneesmiddel bevat 48 mg L-proline en 0,19 mg polysorbaat 80 in elke dosis van 210 mg (1,91 ml).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie (injectie)
Heldere tot opalescente, kleurloze tot lichtgele oplossing.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Astma
Tezspire is geïndiceerd als aanvullende onderhoudsbehandeling bij volwassen en adolescente patiënten van 12 jaar en ouder met ernstig astma dat onvoldoende onder controle is, ondanks hoog gedoseerde inhalatiecorticosteroïden in combinatie met een ander geneesmiddel als onderhoudsbehandeling.
Chronische rinosinusitis met neuspoliepen (CRSwNP)
Tezspire is geïndiceerd als aanvullende behandeling op intranasale corticosteroïden bij volwassen patiënten met ernstige chronische rinosinusitis met neuspoliepen (CRSwNP) bij wie behandeling met systemische corticosteroïden en/of chirurgie onvoldoende controle van de ziekte geeft.
4.2 Dosering en wijze van toediening
De behandeling moet worden gestart door een arts die ervaring heeft met de diagnose en behandeling van aandoeningen waarvoor Tezspire is geïndiceerd (zie rubriek 4.1).
Dosering
Tezspire is bestemd voor langdurige behandeling. Er dient minstens jaarlijks beslist te worden of de
therapie dient te worden voortgezet op basis van de mate waarin de ziekte onder controle is.
Astma
Volwassen en adolescente patiënten (van 12 jaar en ouder)
De aanbevolen dosering van tezepelumab is 210 mg via subcutane injectie elke 4 weken.
CRSwNP
De aanbevolen dosering van tezepelumab voor volwassenen is 210 mg via subcutane injectie elke 4 weken.
Gemiste dosis
Als een dosis werd gemist, moet deze zo snel mogelijk alsnog worden toegediend. Daarna kan de patiënt de dosering hervatten op de geplande dag van toediening. Als het al tijd is voor de volgende dosis, dien dan toe zoals gepland. Er mag geen dubbele dosis worden toegediend.
Speciale populaties
Ouderen (van 65 jaar en ouder)
Er is geen dosisaanpassing nodig bij oudere patiënten (zie rubriek 5.2).
Nier- en leverinsufficiëntie
Er is geen dosisaanpassing nodig voor patiënten met nier- of leverinsufficiëntie (zie rubriek 5.2).
Pediatrische patiënten
De veiligheid en werkzaamheid van Tezspire voor de behandeling van astma bij kinderen jonger dan 12 jaar zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
De veiligheid en werkzaamheid van Tezspire voor de behandeling van CRSwNP bij kinderen jonger dan 18 jaar zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
Wijze van toediening
Tezspire wordt toegediend als een subcutane injectie.
Een patiënt kan dit geneesmiddel zelf injecteren of de verzorger van de patiënt mag dit geneesmiddel toedienen na getraind te zijn in de subcutane injectietechniek. Patiënten en/of verzorgers moeten vóór gebruik een goede training krijgen over de bereiding en toediening van Tezspire volgens de ‘Gebruiksaanwijzing’.
Tezspire moet worden geïnjecteerd in de dij of buik, behalve in de 5 cm rond de navel. Als een beroepsbeoefenaar in de gezondheidszorg of verzorger de injectie toedient, kan de bovenarm ook worden gebruikt. Een patiënt mag niet zelf in de arm injecteren. Het mag niet worden geïnjecteerd in gebieden waar de huid gevoelig is, blauwe plekken heeft, of erythemateus of verhard is. Het wordt aanbevolen om bij elke injectie de injectieplaats af te wisselen.
Uitgebreide instructies voor toediening met de voorgevulde spuit of met de voorgevulde pen zijn te vinden in de ‘Gebruiksaanwijzing’.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
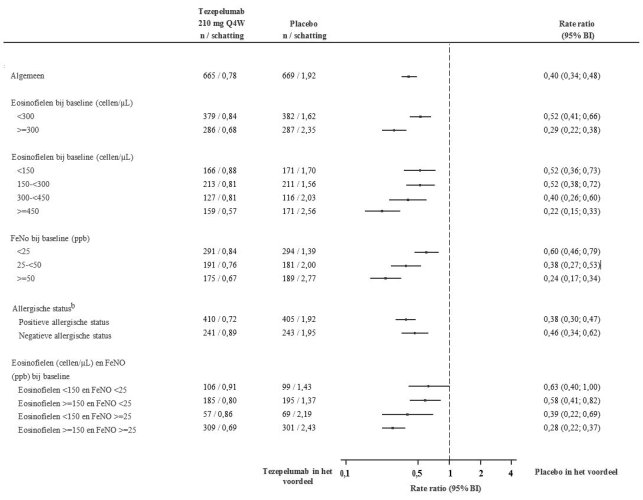
De meest gemelde bijwerkingen tijdens de behandeling van astma zijn artralgie (3,8%) en faryngitis (4,1%) en de meest gemelde bijwerking tijdens de behandeling van CRSwNP is faryngitis (5,4%).
Tabel met lijst van bijwerkingen
Tabel 1 geeft de bijwerkingen weer uit klinische studies bij patiënten met ernstig astma en CRSwNP, die ten minste één dosis Tezspire toegediend kregen tijdens studies die 52 weken duurden, en uit postmarketingervaring.
De frequentie van bijwerkingen wordt gedefinieerd als: zeer vaak (≥1/10); vaak (≥1/100, <1/10); soms (≥1/1.000, <1/100); zelden (≥1/10.000, <1/1.000); zeer zelden (<1/10.000); en niet bekend (kan met de beschikbare gegevens niet worden bepaald). Binnen elke frequentiegroep worden bijwerkingen gerangschikt naar afnemende ernst.
Tabel 1 Lijst van bijwerkingen | ||
Systeem/orgaanklasse | Bijwerking | Frequentie |
Infecties en parasitaire aandoeningen | Faryngitisa | Vaak |
Immuunsysteemaandoeningen | Overgevoeligheid (waaronder anafylactische reactie) | Niet bekend |
Huid- en onderhuidaandoeningen | Rashb | Vaak |
Skeletspierstelsel- en bindweefselaandoeningen | Artralgie | Vaak |
Algemene aandoeningen en toedieningsplaatsstoornissen | Reactie op de injectieplaatsc | Vaak |
a Faryngitis is gedefinieerd door de volgende gegroepeerde voorkeurstermen: faryngitis, faryngitis bacterieel, streptokokkenfaryngitis en virale faryngitis.
b Rash is gedefinieerd door de volgende gegroepeerde voorkeurstermen: rash, rash pruritus, rash erythemateus, rash maculo-papulair, rash vlekkerig.
c Zie ‘Beschrijving van geselecteerde bijwerkingen’.
Beschrijving van geselecteerde bijwerkingen
Reacties op de injectieplaats
In de samengevoegde veiligheidsgegevens van PATHWAY en NAVIGATOR traden reacties op de injectieplaats op (bijv. erytheem, zwelling en/of pijn op de injectieplaats) bij 3,8% van de patiënten die werden behandeld met 210 mg tezepelumab, subcutaan elke 4 weken (Q4W).
Pediatrische patiënten
Een totaal van 82 adolescenten in de leeftijd van 12 tot 17 jaar met ernstig, ongecontroleerd astma nam deel aan de 52 weken durende fase 3-studie NAVIGATOR (zie rubriek 5.1). Het veiligheidsprofiel bij adolescenten was over het algemeen vergelijkbaar met de totale studiepopulatie.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
AstraZeneca AB
SE 151 85 Södertälje
Zweden
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/22/1677/001 1 voorgevulde spuit
EU/1/22/1677/002 Meerstuksverpakking: 3 (3 verpakkingen van 1) voorgevulde spuiten
EU/1/22/1677/003 1 voorgevulde pen
EU/1/22/1677/004 Meerstuksverpakking: 3 (3 verpakkingen van 1) voorgevulde pennen
10. DATUM VAN HERZIENING VAN DE TEKST
10/2025
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4636767 | TEZSPIRE 210MG OPL INJ SER VOORGEVULDE FL 1,91ML | € 1216,73 | - | Ja | € 12,8 | € 8,5 | |
| 4652350 | TEZSPIRE 210MG OPLOSSING VOOR INJECTIE IN VOORGEVULDE SPUIT | € 3628,25 | - | Ja | € 12,8 | € 8,5 |