1. NAAM VAN HET GENEESMIDDEL
Enbrel 25 mg oplossing voor injectie in een patroon voor dosisdispenser
Enbrel 50 mg oplossing voor injectie in een patroon voor dosisdispenser
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Enbrel 25 mg oplossing voor injectie in een patroon voor dosisdispenser
Elke patroon voor dosisdispenser bevat 25 mg etanercept.
Enbrel 50 mg oplossing voor injectie in een patroon voor dosisdispenser
Elke patroon voor dosisdispenser bevat 50 mg etanercept.
Etanercept is een humaan tumornecrosefactorreceptor-p75 Fc-fusie-eiwit geproduceerd met recombinant-DNA-techniek in een zoogdierexpressiesysteem van het Chinese hamsterovarium.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie.
De oplossing is helder, en kleurloos tot lichtgeel of lichtbruin.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Reumatoïde artritis
Enbrel in combinatie met methotrexaat is geïndiceerd voor de behandeling van volwassenen met matige tot ernstige actieve reumatoïde artritis, waarbij de respons op ‘disease-modifying antirheumatic drugs’, waaronder methotrexaat (tenzij gecontra-indiceerd), ontoereikend is gebleken.
Enbrel kan als monotherapie verstrekt worden wanneer er sprake is van een intolerantie ten opzichte van methotrexaat of wanneer verdere behandeling met methotrexaat als ongepast wordt ervaren.
Enbrel is tevens geïndiceerd voor de behandeling van ernstige, actieve en progressieve reumatoïde artritis bij volwassenen die niet eerder behandeld zijn met methotrexaat.
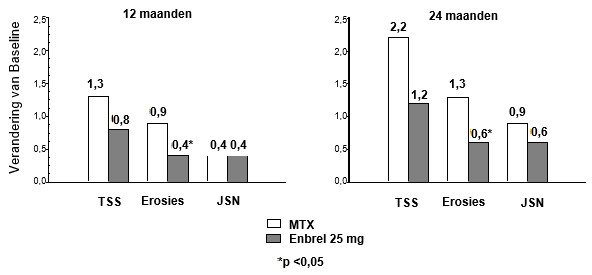
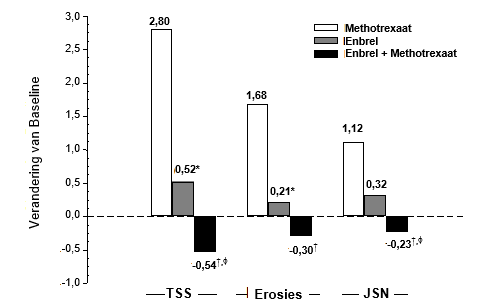
Het is gebleken dat Enbrel, zowel op zichzelf gebruikt als in combinatie met methotrexaat, de progressiesnelheid van gewrichtsschade, zoals deze door middel van röntgenonderzoek gemeten wordt, reduceert en het lichamelijk functioneren verbetert.
Juveniele idiopathische artritis
Behandeling van polyartritis (reumafactor positief of negatief) en uitgebreide oligoartritis bij kinderen en adolescenten vanaf 2 jaar die een ontoereikende respons hebben gehad op methotrexaat of methotrexaat niet verdroegen.
Behandeling van arthritis psoriatica bij adolescenten vanaf 12 jaar die een ontoereikende respons hebben gehad op methotrexaat of die methotrexaat niet verdroegen.
Behandeling van enthesitis-gerelateerde artritis bij adolescenten vanaf 12 jaar die een ontoereikende respons hebben gehad op conventionele therapie of die conventionele therapie niet verdroegen.
Arthritis psoriatica
Behandeling van actieve en progressieve arthritis psoriatica bij volwassenen bij wie de respons op eerdere ‘disease-modifying antirheumatic drug’-therapie onvoldoende is gebleken. Enbrel heeft laten zien dat het het lichamelijk functioneren van patiënten met arthritis psoriatica verbetert en de snelheid van progressie van perifere gewrichtsschade, gemeten door middel van röntgenonderzoek, vermindert bij patiënten met polyarticulaire symmetrische subtypen van de aandoening.
Axiale spondyloartritis
Spondylitis ankylopoetica (SA)
Behandeling van ernstige actieve spondylitis ankylopoetica bij volwassenen bij wie de respons op conventionele therapie ontoereikend was.
Niet-radiografische axiale spondyloartritis
Behandeling van volwassenen met ernstige niet-radiografische axiale spondyloartritis met objectieve verschijnselen van ontsteking zoals aangegeven door een verhoogd C-reactief proteïne (CRP) en/of met magnetische kernspinresonantie (MRI), die een ontoereikende respons hebben gehad op niet-steroïdale ontstekingsremmers (non-steroidal anti-inflammatory drugs - NSAID’s).
Plaque psoriasis
Behandeling van matige tot ernstige plaque psoriasis bij volwassenen met onvoldoende respons op, of een intolerantie of een contra-indicatie voor, andere systemische therapie waaronder ciclosporine, methotrexaat of psoralenen en ultraviolet A-licht (PUVA) (zie rubriek 5.1).
Plaque psoriasis bij kinderen
Behandeling van chronische ernstige plaque psoriasis bij kinderen en adolescenten vanaf 6 jaar met onvoldoende controle door, of intolerantie voor, andere systemische therapieën of fototherapieën.
4.2 Dosering en wijze van toediening
Behandeling met Enbrel dient te worden begonnen door en onder de begeleiding te blijven van artsen, gespecialiseerd in de diagnose en behandeling van reumatoïde artritis, juveniele idiopathische artritis, arthritis psoriatica, spondylitis ankylopoetica, niet-radiografische axiale spondyloartritis, plaque psoriasis of plaque psoriasis bij kinderen. Aan met Enbrel behandelde patiënten dient een ‘Patiëntenkaart’ te worden gegeven.
De Enbrel-patroon voor dosisdispenser is beschikbaar in sterktes van 25 mg en 50 mg. Andere toedieningsvormen van Enbrel zijn beschikbaar in sterktes van 10 mg, 25 mg en 50 mg.
Dosering
Reumatoïde artritis
De aanbevolen dosering is 25 mg Enbrel, tweemaal per week toegediend. Ook 50 mg Enbrel, eenmaal per week toegediend, is veilig en effectief gebleken (zie rubriek 5.1).
Arthritis psoriatica, spondylitis ankylopoetica en niet-radiografische axiale spondyloartritis
De aanbevolen dosering is 25 mg Enbrel, tweemaal per week toegediend, of 50 mg Enbrel eenmaal per week toegediend.
Beschikbare gegevens suggereren dat voor alle bovengenoemde indicaties een klinische respons gewoonlijk binnen 12 behandelweken wordt bereikt. Indien een patiënt niet reageert binnen dit tijdsbestek dient een vervolgbehandeling zorgvuldig te worden overwogen.
Plaque psoriasis
De aanbevolen dosering is 25 mg Enbrel, tweemaal per week toegediend, of 50 mg, eenmaal per week toegediend. Als alternatief kan voor maximaal 12 weken tweemaal per week 50 mg gebruikt worden, indien nodig gevolgd door een dosering van 25 mg tweemaal per week of 50 mg eenmaal per week. De behandeling met Enbrel dient te worden voortgezet tot remissie wordt bereikt, tot maximaal 24 weken. Voortdurende behandeling na 24 weken kan geschikt zijn voor sommige volwassen patiënten (zie rubriek 5.1). De behandeling dient gestaakt te worden bij patiënten die na 12 weken geen respons vertonen. Als herhalingsbehandeling met Enbrel geïndiceerd is, dient bovenstaande richtlijn over de behandelduur gevolgd te worden. De dosis dient 25 mg tweemaal per week of 50 mg eenmaal per week te zijn.
Bijzondere patiëntgroepen
Nier- en leverfunctiestoornissen
Aanpassing van de dosis is niet noodzakelijk.
Ouderen
Aanpassing van de dosering is niet noodzakelijk. Dosering en wijze van toediening zijn hetzelfde als voor volwassenen in de leeftijd van 18‑64 jaar.
Pediatrische patiënten
De dosering van Enbrel voor kinderen is gebaseerd op het lichaamsgewicht. Patiënten die minder dan 62,5 kg wegen, moeten nauwkeurig gedoseerd worden op basis van mg/kg gebruikmakend van het poeder en oplosmiddel voor oplossing voor injectie of het poeder voor oplossing voor injectie (zie hieronder de dosering voor specifieke indicaties). Patiënten die 62,5 kg of meer wegen kunnen gedoseerd worden met een vaste dosis in een voorgevulde spuit, een voorgevulde pen of een patroon voor dosisdispenser.
De veiligheid en werkzaamheid van Enbrel bij kinderen jonger dan 2 jaar zijn niet vastgesteld.
Er zijn geen gegevens beschikbaar.
Juveniele idiopathische artritis (JIA)
De aanbevolen dosering is 0,4 mg/kg (tot een maximum van 25 mg per dosis) tweemaal per week gegeven als subcutane injectie met een interval van 3‑4 dagen tussen twee doses, of 0,8 mg/kg (tot een maximum van 50 mg per dosis) eenmaal per week gegeven. Het stoppen van de behandeling dient overwogen te worden bij patiënten die geen respons laten zien na 4 maanden.
De injectieflacon met 10 mg kan geschikter zijn voor toediening aan kinderen met JIA die een lichaamsgewicht van minder dan 25 kg hebben.
Er zijn geen formele klinische onderzoeken uitgevoerd bij kinderen van 2 en 3 jaar oud. Beperkte veiligheidsdata uit een patiëntenregister suggereren echter dat het veiligheidsprofiel bij kinderen van 2 en 3 jaar oud, die eenmaal per week 0,8 mg/kg subcutaan toegediend krijgen, vergelijkbaar is met dat bij volwassenen en kinderen van 4 jaar en ouder (zie rubriek 5.1).
Er is in het algemeen geen geëigend gebruik van Enbrel bij kinderen jonger dan 2 jaar voor de indicatie juveniele idiopathische artritis.
Plaque psoriasis bij kinderen (leeftijd 6 jaar en ouder)
De aanbevolen dosering is 0,8 mg/kg (tot een maximum van 50 mg per dosis) eenmaal per week gedurende maximaal 24 weken. De behandeling dient gestaakt te worden bij patiënten die na 12 weken geen respons vertonen.
Wanneer een herhalingsbehandeling met Enbrel geïndiceerd wordt, dient bovenstaande richtlijn voor de duur van de behandeling opgevolgd te worden. De dosering dient 0,8 mg/kg (tot een maximum van 50 mg per dosis) eenmaal per week te zijn.
Er is in het algemeen geen geëigend gebruik van Enbrel bij kinderen jonger dan 6 jaar voor de indicatie plaque psoriasis.
Wijze van toediening
Subcutaan gebruik
De totale inhoud (0,5 ml voor de 25 mg dosissterkte of 1 ml voor de 50 mg dosissterkte) van de patroon voor dosisdispenser dient uitsluitend te worden toegediend met behulp van het SMARTCLIC-injecteerapparaat voor een subcutane injectie. Geschikte plaatsen voor injectie zijn de buik, het bovenste deel van de dijen, of wanneer toegediend door een zorgverlener, aan de buitenkant van de bovenarmen.
Enbrel oplossing voor injectie in een patroon voor dosisdispenser is bedoeld voor eenmalig gebruik in combinatie met het SMARTCLIC-apparaat. Na de juiste training van de injecteertechniek kunnen patiënten zichzelf injecteren met behulp van het SMARTCLIC-apparaat met de patroon voor dosisdispenser voor eenmalig gebruik, als hun arts bepaalt dat dit kan. De patiënten krijgen indien nodig een medische opvolging. De arts dient met de patiënt te bespreken welke toedieningsvorm voor injectie het meest geschikt is.
Bij de toediening dienen de instructies voor gebruik aan het eind van de bijsluiter en in de gebruikershandleiding die bij het SMARTCLIC-apparaat wordt geleverd, te worden gevolgd (zie rubriek 6.6). Gedetailleerde instructies over onbedoelde afwijkingen van het doseringsschema, inclusief gemiste doses, zijn vermeld in rubriek 3 van de bijsluiter.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
Sepsis of een risico op sepsis.
Behandeling met Enbrel mag niet worden begonnen bij patiënten met actieve infecties, waaronder chronische of gelokaliseerde infecties.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De meest gerapporteerde bijwerkingen zijn reacties op de injectieplaats (waaronder pijn, zwelling, jeuk, rood worden en bloeding op de punctieplaats), infecties (waaronder bovensteluchtweginfecties, bronchitis, blaasontsteking en huidinfecties), hoofdpijn, allergische reacties, vorming van auto-antilichamen, jeuk en koorts.
Ernstige bijwerkingen zijn ook gerapporteerd voor Enbrel. TNF‑antagonisten, zoals Enbrel, hebben effect op het immuunsysteem en hun gebruik kan de afweer van het lichaam tegen infecties en kanker beïnvloeden. Ernstige infecties komen voor bij minder dan 1 op 100 patiënten behandeld met Enbrel. Meldingen betroffen ook fatale en levensbedreigende infecties en sepsis. Verschillende maligniteiten zijn ook gerapporteerd tijdens het gebruik van Enbrel, waaronder borstkanker, longkanker, huidkanker en lymfeklierkanker (lymfoom).
Ernstige hematologische, neurologische en auto-immuunreacties zijn ook gerapporteerd. Deze omvatten zeldzame meldingen van pancytopenie en zeer zeldzame meldingen van aplastische anemie. Centrale en perifere demyeliniserende aandoeningen zijn zelden, respectievelijk zeer zelden waargenomen tijdens het gebruik van Enbrel. Er zijn zeldzame meldingen geweest van lupus, lupus-gerelateerde aandoeningen en vasculitis.
Overzicht van bijwerkingen in tabelvorm
De lijst met bijwerkingen die hieronder is weergegeven is gebaseerd op ervaring uit klinische onderzoeken en op post-marketingervaring.
Binnen de systeem/orgaanklassen zijn bijwerkingen gerangschikt naar frequentie (aantal patiënten dat wordt verwacht de bijwerking te ervaren), waarbij gebruik is gemaakt van de volgende categorieën: zeer vaak (≥1/10); vaak (≥1/100, <1/10); soms (≥1/1.000, <1/100); zelden (≥1/10.000, <1/1.000); zeer zelden (<1/10.000); niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Systeem/orgaanklasse | Zeer vaak | Vaak | Soms | Zelden | Zeer zelden | Niet bekend (kan met de beschikbare gegevens niet worden bepaald) | |
Infecties en parasitaire aandoeningen | Infectie (waaronder bovensteluchtweginfectie, bronchitis, cystitis, huidinfectie)* |
| Ernstige infecties (waaronder pneumonie, cellulitis, artritis bacterieel, sepsis en parasitaire infectie)* | Tuberculose, opportunistische infectie (waaronder invasieve schimmel-, Protozoa-, bacteriële, atypische mycobacteriële, virale infecties en Legionella)* |
| Hepatitis B-reactivering, listeria | |
Neoplasmata, benigne, maligne en niet-gespecificeerd (inclusief cysten en poliepen) |
|
| Niet-melanome huidkankers* (zie rubriek 4.4) | Maligne melanoom (zie rubriek 4.4), lymfoom, leukemie |
| Merkelcelcarcinoom (zie rubriek 4.4), Kaposi-sarcoom | |
Bloed- en lymfestelselaandoeningen |
|
| Trombocytopenie, anemie, leukopenie, neutropenie | Pancytopenie* | Aplastische anemie* | Histiocytose hematofaag (macrofaagactivatiesyndroom)* | |
Immuunsysteemaandoeningen |
| Allergische reacties (zie Huid- en onderhuidaandoeningen), auto-antilichaamvorming* | Vasculitis (waaronder antineutrofielen-cytoplasma-antilichaamgeassocieerde vasculitis) | Ernstige allergische/anafylactische reacties (waaronder angio-oedeem, bronchospasme), sarcoïdose |
| Verergering van symptomen van dermatomyositis | |
Zenuwstelselaandoeningen | Hoofdpijn |
|
| Demyelinisatie van het CZS wijzend op multipele sclerose of gelokaliseerde demyeliniserende aandoeningen, zoals neuritis optica en myelitis transversa (zie rubriek 4.4), perifere demyelinisatie, waaronder Guillain-Barré-syndroom, chronische inflammatoire demyeliniserende polyneuropathie, demyeliniserende polyneuropathie en multifocale motorische neuropathie (zie rubriek 4.4), epileptische aanval |
|
| |
Oogaandoeningen |
|
| Uveïtis, scleritis |
|
|
| |
Hartaandoeningen |
|
| Verergering van congestief hartfalen (zie rubriek 4.4) | Nieuw ontstaan van congestief hartfalen (zie rubriek 4.4) |
|
| |
Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen |
|
|
| Interstitiële longaandoening (waaronder pneumonitis en longfibrose)* |
|
| |
Maagdarmstelselaandoeningen |
|
| Inflammatoire darmziekte |
|
|
| |
Lever- en galaandoeningen |
|
| Verhoogde leverenzymen* | Auto-immuunhepatitis* |
|
| |
Huid- en onderhuidaandoeningen |
| Pruritus, uitslag | Angio-oedeem, psoriasis (waaronder nieuwe of erger wordende pustuleuze, voornamelijk op de handpalmen en de voetzolen), urticaria, psoriasiforme huiduitslag | Stevens-Johnson-syndroom, cutane vasculitis (waaronder overgevoeligheidsvasculitis), erythema multiforme, lichenoïde reacties | Toxische epidermale necrolyse |
| |
Skeletspierstelsel- en bindweefselaandoeningen |
|
|
| Cutane lupus erythematosus, subacute cutane lupus erythematosus, lupusachtig syndroom |
|
| |
Nier- en urinewegaandoeningen |
|
|
| Glomerulonefritis |
|
| |
Algemene aandoeningen en toedieningsplaatsstoornissen | Reacties op de injectieplaats (waaronder bloeding, blauwe plekken, erytheem, jeuk, pijn, zwelling)* | Pyrexie |
|
|
|
| |
*Zie Beschrijving van geselecteerde bijwerkingen hieronder. |
| ||||||
Beschrijving van geselecteerde bijwerkingen
Maligniteiten en lymfoproliferatieve aandoeningen
Honderdnegenentwintig (129) nieuwe maligniteiten van verschillende types werden geobserveerd bij 4.114 patiënten met reumatoïde artritis die in klinisch onderzoek behandeld werden met Enbrel gedurende maximaal ongeveer 6 jaar, waaronder 231 patiënten die behandeld werden met Enbrel in combinatie met methotrexaat tijdens het 2 jaar durend actief-gecontroleerd onderzoek. De waargenomen frequentie en incidenties in deze klinische trials waren overeenkomstig de verwachting voor de bestudeerde populatie. Een totaal aantal van 2 maligniteiten werd gemeld in klinische onderzoeken die ongeveer 2 jaar duurden en die 240 met Enbrel-behandelde patiënten met arthritis psoriatica omvatten. In klinische onderzoeken die gedurende meer dan 2 jaar werden uitgevoerd met 351 patiënten met spondylitis ankylopoetica, werden 6 maligniteiten gemeld onder de met Enbrel behandelde patiënten. In een groep van 2.711 patiënten met plaque psoriasis die met Enbrel behandeld werden in dubbelblinde en open-labelonderzoeken van maximaal 2,5 jaar werden 30 maligniteiten en 43 niet-melanome huidkankers gemeld.
In een groep van 7.416 met Enbrel behandelde patiënten in klinische trials voor reumatoïde artritis, arthritis psoriatica, spondylitis ankylopoetica en psoriasis werden 18 lymfomen gemeld.
Tijdens de postmarketingperiode werden ook meldingen ontvangen van verscheidene maligniteiten (waaronder borst- en longcarcinoom en lymfoom) (zie rubriek 4.4).
Reacties op de plaats van injectie
Vergeleken met placebo hadden patiënten met reumatische aandoeningen die met Enbrel werden behandeld een significant hogere incidentie van reacties op de plaats van injectie (36% vs. 9%). Reacties op de plaats van injectie vonden gewoonlijk plaats in de eerste maand. De gemiddelde duur was ongeveer 3 tot 5 dagen. Voor de meerderheid van de reacties op de plaats van injectie in de met Enbrel behandelde groep werd geen behandeling gegeven en de meerderheid van de patiënten die wel behandeld werden, kregen lokale preparaten zoals corticosteroïden of orale antihistaminica. Daarnaast ontwikkelden zich bij sommige patiënten geheugenreacties op de plaats van injectie, die werden gekarakteriseerd door een huidreactie op de meest recente plaats van injectie, tezamen met een simultane verschijning van reacties op de plaats van de vorige injecties. Deze reacties waren in het algemeen van voorbijgaande aard en keerden niet terug in de loop van de behandeling.
In gecontroleerde onderzoeken bij patiënten met plaque psoriasis ontwikkelde ongeveer 13,6% van de met Enbrel behandelde patiënten reacties op de plaats van injectie vergeleken met 3,4% van de met placebo behandelde patiënten gedurende de eerste 12 weken van behandeling.
Ernstige infecties
In placebogecontroleerd onderzoek werd geen verhoging van de incidentie van ernstige infecties (fataal, levensbedreigend, of met de noodzaak tot ziekenhuisopnames of intraveneuze antibiotica) waargenomen. Ernstige infecties traden op in 6,3% van de patiënten met reumatoïde artritis die met Enbrel behandeld werden gedurende maximaal 48 maanden. Deze bestonden uit abces (op verschillende plaatsen), bacteriëmie, bronchitis, bursitis, cellulitis, cholecystitis, diarree, diverticulitis, endocarditis (verdenking), gastro-enteritis, hepatitis B, herpes zoster, beenzweer, mondinfectie, osteomyelitis, otitis, peritonitis, pneumonie, pyelonefritis, sepsis, septische artritis, sinusitis, huidinfectie, huidulcus, urineweginfectie, vasculitis en wondinfectie. In het twee jaar durend actief-gecontroleerd onderzoek waarin patiënten werden behandeld met alleen Enbrel, of alleen methotrexaat of met Enbrel in combinatie met methotrexaat, waren de aantallen ernstige infecties gelijk in de verschillende behandelingsgroepen. Het kan echter niet worden uitgesloten dat de combinatie van Enbrel en methotrexaat verband zou kunnen houden met een verhoogd percentage infecties.
Er waren geen verschillen in de infectiepercentages tussen patiënten die behandeld werden met Enbrel en die behandeld werden met placebo voor plaque psoriasis in placebogecontroleerde onderzoeken die tot 24 weken duurden. Ernstige infecties die de met Enbrel behandelde patiënten ondervonden waren, cellulitis, gastro-enteritis, pneumonie, cholecystitis, osteomyelitis, gastritis, appendicitis, streptokokkenfasciitis, myositis, septische shock, diverticulitis en abces. In de dubbelblinde en open-label arthritis psoriatica-onderzoeken meldde 1 patiënt een ernstige infectie (pneumonie).
Ernstige en fatale infecties zijn gerapporteerd tijdens het gebruik van Enbrel; gemelde pathogenen waren onder andere bacteriën, mycobacteriën (waaronder M. tuberculosis), virussen en schimmels. Sommige hebben plaatsgevonden binnen enkele weken na het starten van de behandeling met Enbrel bij patiënten met onderliggende ziektes (bijv. diabetes, congestief hartfalen, een voorgeschiedenis van actieve of chronische infectie) in aanvulling op hun reumatoïde artritis (zie rubriek 4.4). Behandeling met Enbrel zou de mortaliteit kunnen verhogen bij patiënten met vastgestelde sepsis.
Opportunistische infecties zijn gemeld in associatie met Enbrel, inclusief invasieve schimmel-, parasitaire (inclusief protozoale), virale (waaronder herpes zoster), bacteriële (inclusief Listeria en Legionella) en atypische mycobacteriële infecties. In een gepoolde dataset van klinische onderzoeken was de totale incidentie van opportunistische infecties 0,09% voor de 15.402 patiënten die Enbrel kregen. De incidentie aangepast aan de duur van blootstelling was 0,06 gebeurtenissen per 100 patiëntjaren. In postmarketingervaring bestond ongeveer de helft van alle wereldwijde case reports van opportunistische infecties uit invasieve schimmelinfecties. De meest voorkomende gerapporteerde invasieve schimmelinfecties omvatten Candida, Pneumocystis, Aspergillus en Histoplasma. Invasieve schimmelinfecties veroorzaakten meer dan de helft van de overlijdensgevallen onder patiënten die opportunistische infecties ontwikkelden. De meerderheid van de meldingen met een fatale uitkomst was bij patiënten met Pneumocystis pneumonie, ongespecificeerde systemische schimmelinfecties en aspergillose (zie rubriek 4.4).
Auto-antilichamen
Van volwassen patiënten werd op meerdere tijdstippen serum getest op auto-antilichamen. Van de patiënten met reumatoïde artritis die geëvalueerd werden op antinucleaire antilichamen (ANA) was het percentage patiënten dat nieuwe positieve ANA ontwikkelde (1:40) hoger bij de met Enbrel behandelde patiënten (11%) dan bij de met placebo behandelde patiënten (5%). Het percentage patiënten dat nieuwe positieve anti-ds-DNA-antilichamen ontwikkelde was ook groter met radio-immuunbepaling (15% van de patiënten die behandeld werden met Enbrel vergeleken met 4% van de met placebo behandelde patiënten) en met de Crithidia lucida-test (3% van de met Enbrel behandelde patiënten vergeleken met geen van de met placebo behandelde patiënten). Van de patiënten die behandeld werden met Enbrel was de proportie die anti-cardiolipineantilichamen ontwikkelde, vergelijkbaar verhoogd vergeleken met de met placebo behandelde patiënten. De invloed van langdurige behandeling met Enbrel op de ontwikkeling van auto-immuunziekten is onbekend.
Er zijn zeldzame meldingen geweest van patiënten, inclusief reumafactorpositieve patiënten, die andere auto-antilichamen hebben ontwikkeld in samenhang met een lupusachtig syndroom of uitslag welke qua klinische presentatie en biopsie vergelijkbaar is met subactieve huidlupus of discoïde lupus.
Pancytopenie en aplastische anemie
Er waren postmarketingmeldingen van pancytopenie en aplastische anemie waarvan sommige een fatale afloop hadden (zie rubriek 4.4).
Interstitiële longaandoening
In gecontroleerde klinische onderzoeken met etanercept bij alle indicaties bedroeg de frequentie (incidentie als proportie) van interstitiële longaandoening bij patiënten die etanercept kregen, zonder dat ze gelijktijdig ook methotrexaat kregen 0,06% (frequentie zelden). In de gecontroleerde klinische onderzoeken die gelijktijdige behandeling met etanercept en methotrexaat toestonden, bedroeg de frequentie (incidentie als proportie) van interstitiële longaandoening 0,47% (frequentie soms). Er waren postmarketingmeldingen van interstitiële longaandoening (inclusief pneumonitis en longfibrose) waarvan sommige een fatale afloop hadden.
Gelijktijdige behandeling met anakinra
In onderzoeken waarin volwassen patiënten gelijktijdig behandeld werden met Enbrel en anakinra, werd een hoger percentage ernstige infecties gevonden dan bij patiënten die alleen met Enbrel behandeld werden en bij 2% van de patiënten (3/139) ontwikkelde zich neutropenie (absoluut aantal neutrofielen 1.000/mm3). Eén neutropenische patiënt ontwikkelde cellulitis die na ziekenhuisopname vanzelf verdween (zie rubrieken 4.4 en 4.5).
Verhoogde leverenzymen
In de dubbelblinde periodes van gecontroleerde klinische onderzoeken met etanercept bij alle indicaties, bedroeg de frequentie (incidentie als proportie) van de bijwerking verhoogde leverenzymen bij patiënten die etanercept kregen, zonder dat ze gelijktijdig ook methotrexaat kregen 0,54% (frequentie soms). In de dubbelblinde periodes van gecontroleerde klinische onderzoeken die gelijktijdige behandeling met etanercept en methotrexaat toestonden, bedroeg de frequentie (incidentie als proportie) van de bijwerking verhoogde leverenzymen 4,18% (frequentie vaak).
Auto-immuunhepatitis
In gecontroleerde klinische onderzoeken met etanercept bij alle indicaties bedroeg de frequentie (incidentie als proportie) van auto-immuunhepatitis bij patiënten die etanercept kregen, zonder dat ze gelijktijdig ook methotrexaat kregen 0,02% (frequentie zelden). In de gecontroleerde klinische onderzoeken die gelijktijdige behandeling met etanercept en methotrexaat toestonden, bedroeg de frequentie (incidentie als proportie) van auto-immuunhepatitis 0,24% (frequentie soms).
Pediatrische patiënten
Bijwerkingen bij pediatrische patiënten met juveniele idiopathische artritis
In het algemeen waren de bijwerkingen bij kinderen met juveniele idiopathische artritis overeenkomstig in frequentie en type met de bijwerkingen die gezien werden bij volwassenen. Verschillen met volwassenen en andere speciale overwegingen staan beschreven in de volgende paragrafen.
De typen infecties die werden gezien in klinisch onderzoek met patiënten van 2 tot 18 jaar met juveniele idiopathische artritis waren meestal licht tot matig en kwamen overeen met de typen infecties die vaak gezien worden bij poliklinische pediatrische patiënten. Ernstige bijwerkingen die werden gerapporteerd, omvatten varicella met verschijnselen en symptomen van aseptische meningitis die zonder sequela verdwenen (zie ook rubriek 4.4), appendicitis, gastro-enteritis, depressie/persoonlijkheidsstoornis, huidulcus, oesofagitis/gastritis, septische shock door groep A‑streptokokken, diabetes mellitus type I en infectie van weke delen en postoperatieve wonden.
In één onderzoek met kinderen van 4 tot 17 jaar met juveniele idiopathische artritis liepen 43 van de 69 (62%) kinderen een infectie op terwijl ze Enbrel kregen gedurende 3 maanden van het onderzoek (deel 1, open-label). De frequentie en ernst van de infecties was vergelijkbaar bij 58 patiënten die de 12 maanden durende open-label extensietherapie afgerond hadden. De typen en proportie van bijwerkingen bij patiënten met juveniele idiopathische artritis waren gelijk aan die gezien werden in onderzoeken met Enbrel bij volwassen patiënten met reumatoïde artritis en waren merendeels licht. Verschillende bijwerkingen werden meer gerapporteerd bij 69 patiënten met juveniele idiopathische artritis die gedurende 3 maanden Enbrel kregen dan bij de 349 volwassen patiënten met reumatoïde artritis. Deze omvatten hoofdpijn (19% van de patiënten, 1,7 gebeurtenissen per patiëntjaar), misselijkheid (9%, 1,0 gebeurtenis per patiëntjaar), buikpijn (19%, 0,74 gebeurtenissen per patiëntjaar) en braken (13%, 0,74 gebeurtenissen per patiëntjaar).
In klinisch onderzoek naar juveniele idiopathische artritis werden 4 gevallen van macrofaagactivatiesyndroom gemeld.
Bijwerkingen bij kinderen met plaque psoriasis
In een 48 weken durend onderzoek met 211 kinderen in de leeftijd van 4 tot 17 jaar met plaque psoriasis waren de gemelde bijwerkingen vergelijkbaar met de bijwerkingen die in eerdere onderzoeken met volwassenen met plaque psoriasis werden gezien.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België: Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie
Website: www.eenbijwerkingmelden.be
E-mail: adr@fagg-afmps.be
Nederland: Nederlands Bijwerkingen Centrum Lareb
Website: www.lareb.nl
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Pfizer Europe MA EEIG
Boulevard de la Plaine 17
1050 Brussel
België
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Enbrel 25 mg oplossing voor injectie in een patroon voor dosisdispenser
EU/1/99/126/027
EU/1/99/126/028
EU/1/99/126/029
Enbrel 50 mg oplossing voor injectie in een patroon voor dosisdispenser
EU/1/99/126/030
EU/1/99/126/031
EU/1/99/126/032
10. DATUM VAN HERZIENING VAN DE TEKST
07/2025
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
25G10
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4521068 | Enbrel 25 mg oplossing voor injectie in een patroon voor dosisdispenser – 4 x 0,5 ml | € 235,18 | - | Ja | € 12,8 | € 8,5 | |
| 4521050 | Enbrel 50 mg oplossing voor injectie in een patroon voor dosisdispenser – 4 x 1 ml | € 463,46 | - | Ja | € 12,8 | € 8,5 | |
| 4521043 | Enbrel 50 mg oplossing voor injectie in een patroon voor dosisdispenser – 12 x 1 ml | € 1311,9 | - | Ja | € 12,8 | € 8,5 |