1. NAAM VAN HET GENEESMIDDEL
Bimzelx 160 mg oplossing voor injectie in een voorgevulde spuit
Bimzelx 320 mg oplossing voor injectie in een voorgevulde spuit
Bimzelx 160 mg oplossing voor injectie in een voorgevulde pen
Bimzelx 320 mg oplossing voor injectie in een voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Bimzelx 160 mg, oplossing voor injectie in voorgevulde spuit
Elke voorgevulde spuit bevat 160 mg bimekizumab in 1 ml.
Bimzelx 320 mg, oplossing voor injectie in voorgevulde spuit
Elke voorgevulde spuit bevat 320 mg bimekizumab in 2 ml.
Bimzelx 160 mg, oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 160 mg bimekizumab in 1 ml.
Bimzelx 320 mg, oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 320 mg bimekizumab in 2 ml.
Bimekizumab is een gehumaniseerd monoklonaal IgG1-antilichaam, geproduceerd met behulp van recombinant-DNA-technologie in een genetisch gemodificeerde ovariumcellijn van de Chinese hamster (CHO).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie (injectie).
De oplossing is helder tot licht opalescent, en kleurloos tot licht bruinachtig-geel.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Plaque-psoriasis
Bimzelx is geïndiceerd voor de behandeling van matige tot ernstige plaque-psoriasis bij volwassenen die in aanmerking komen voor systemische therapie.
Artritis psoriatica
Bimzelx, alleen of in combinatie met methotrexaat, is geïndiceerd voor de behandeling van actieve artritis psoriatica bij volwassenen die ontoereikend reageerden op een of meer ziektemodificerende antireumatica (‘disease-modifying antirheumatic drugs’, DMARD’s) of deze niet verdragen.
Axiale spondyloartritis
Niet-radiografische axiale spondyloartritis (nr-axSpA)
Bimzelx is geïndiceerd voor de behandeling van volwassenen met actieve niet-radiografische axiale spondyloartritis met objectieve tekenen van ontsteking zoals aangetoond door een verhoogde C‑reactieve proteïne (CRP) en/of magnetische resonantiebeeldvorming (MRI), die ontoereikend reageerden op niet-steroïdale ontstekingsremmers (NSAID’s) of deze niet verdragen.
Spondylitis ankylopoetica (AS, radiografische axiale spondyloartritis)
Bimzelx is geïndiceerd voor de behandeling van volwassenen met actieve spondylitis ankylopoetica die ontoereikend reageerden op conventionele therapie of deze niet verdragen.
Hidradenitis suppurativa (HS)
Bimzelx is geïndiceerd voor de behandeling van actieve matige tot ernstige hidradenitis suppurativa (acne inversa) bij volwassenen met een ontoereikende respons op conventionele systemische HS-therapie (zie rubriek 5.1).
4.2 Dosering en wijze van toediening
Dit geneesmiddel is bedoeld voor gebruik onder begeleiding en toezicht van een arts die ervaring heeft met het diagnosticeren en behandelen van aandoeningen waarvoor het is geïndiceerd.
Dosering
Plaque-psoriasis
De aanbevolen dosis voor volwassen patiënten met plaque-psoriasis bedraagt 320 mg (toegediend als 2 subcutane injecties van 160 mg of 1 subcutane injectie van 320 mg) in week 0, 4, 8, 12, 16 en daarna elke 8 weken.
Artritis psoriatica
De aanbevolen dosis voor volwassen patiënten met actieve artritis psoriatica is 160 mg (toegediend als 1 subcutane injectie van 160 mg) om de 4 weken.
Voor patiënten met artritis psoriatica met gelijktijdige matige tot ernstige plaque-psoriasis is de aanbevolen dosis gelijk aan die voor plaque-psoriasis [320 mg (toegediend als 2 subcutane injecties van 160 mg of 1 subcutane injectie van 320 mg) in week 0, 4, 8, 12, 16 en daarna elke 8 weken]. Na 16 weken is een reguliere beoordeling van de werkzaamheid aanbevolen, en als een toereikende klinische respons in gewrichten niet kan worden gehandhaafd, kan overschakeling op 160 mg om de 4 weken worden overwogen.
Axiale spondyloartritis (nr-axSpA en AS)
De aanbevolen dosis voor volwassen patiënten met axiale spondyloartritis is 160 mg (gegeven als 1 subcutane injectie van 160 mg) om de 4 weken.
Hidradenitis suppurativa
De aanbevolen dosis voor volwassen patiënten met hidradenitis suppurativa is 320 mg (gegeven als 2 subcutane injecties van 160 mg of 1 subcutane injectie van 320 mg) elke 2 weken tot week 16 en elke 4 weken daarna.
Voor bovenstaande indicaties moet overwogen worden om de behandeling stop te zetten bij patiënten die na 16 weken behandeling geen respons hebben laten zien.
Speciale populaties
Patiënten met plaque-psoriasis met overgewicht
Voor sommige patiënten met plaque-psoriasis (inclusief artritis psoriatica met gelijktijdige matige tot ernstige psoriasis) en een lichaamsgewicht ≥ 120 kg die niet volledig psoriasisvrij waren in week 16, biedt 320 mg elke 4 weken na week 16 mogelijk een betere behandelingsrespons (zie rubriek 5.1).
Ouderen (≥ 65 jaar)
Aanpassing van de dosis is niet vereist (zie rubriek 5.2).
Nier- of leverfunctiestoornis
Bimekizumab is niet onderzocht in deze patiëntenpopulaties. Dosisaanpassingen worden niet nodig geacht op basis van de farmacokinetiek (zie rubriek 5.2).
Pediatrische patiënten
De veiligheid en werkzaamheid van bimekizumab bij kinderen en adolescenten jonger dan 18 jaar zijn nog niet vastgesteld. Er zijn geen gegevens beschikbaar.
Wijze van toediening
Dit geneesmiddel wordt toegediend via subcutane injectie. Een dosis van 320 mg kan worden gegeven als 2 subcutane injecties van 160 mg of 1 subcutane injectie van 320 mg.
Geschikte gebieden voor injectie omvatten het bovenbeen, de buik en de bovenarm. Injectielocaties moeten worden afgewisseld en injecties mogen niet worden toegediend in gebieden waar de huid gevoelig, rood of verhard is, blauwe plekken heeft, of is aangedaan door psoriasis. Toediening in de bovenarm mag alleen worden uitgevoerd door een professionele zorgverlener of verzorger.
De voorgevulde spuit of voorgevulde pen mag niet worden geschud.
Na adequate training in subcutane injectietechniek kunnen patiënten Bimzelx zelf injecteren met een voorgevulde spuit of voorgevulde pen, indien hun arts van mening is dat het kan en zo nodig met medische controles. Patiënten dienen geïnstrueerd te worden om de volledige hoeveelheid Bimzelx te injecteren volgens de gebruiksaanwijzing in de bijsluiter.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
Klinisch belangrijke actieve infecties (bijvoorbeeld actieve tuberculose, zie rubriek 4.4).
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De meest gemelde bijwerkingen waren infecties van de bovenste luchtwegen (respectievelijk 14,5%, 14,6%, 16,3%, 8,8% bij plaque-psoriasis, artritis psoriatica, axiale spondyloartritis (axSpA) en hidradenitis suppurativa) en orale candidiasis (respectievelijk 7,3%, 2,3%, 3,7%, 5,6% bij PSO, PsA, axSpA en HS).
Tabel met bijwerkingen
Bijwerkingen uit klinische onderzoeken en meldingen tijdens de fase na het in de handel brengen (tabel 1) worden geclassificeerd volgens MedDRA-systeem-/orgaanklasse en frequentie, aan de hand van de volgende conventie: zeer vaak (≥ 1/10), vaak (≥ 1/100 tot < 1/10), soms (≥ 1/1.000 tot < 1/100), zelden (≥ 1/10.000 tot < 1/1.000), zeer zelden (< 1/10.000), niet bekend (kan met de beschikbare gegevens niet worden bepaald).
In totaal zijn 5.862 patiënten behandeld met bimekizumab in geblindeerde en open-label klinische onderzoeken naar plaque-psoriasis (PSO), artritis psoriatica (PsA), axiale spondyloartritis (nr-axSpA en AS) en hidradenitis suppurativa (HS) wat neerkomt op 11.468,6 patiëntjaren blootstelling. Daarvan werden 4.660 patiënten minstens één jaar blootgesteld aan bimekizumab. Over het geheel genomen is het veiligheidsprofiel van bimekizumab consistent voor alle indicaties.
Tabel 1: Lijst van bijwerkingen
Systeem-/orgaanklasse | Frequentie | Bijwerking |
Infecties en parasitaire aandoeningen | Zeer vaak | Bovenste luchtweginfecties |
Vaak | Orale candidiasis, | |
Soms | Mucosale en cutane candidiasis (waaronder oesofagale candidiasis), | |
Bloed- en lymfestelselaandoeningen | Soms | Neutropenie |
Zenuwstelselaandoeningen | Vaak | Hoofdpijn |
Maag-darmstelselaandoeningen | Soms | Inflammatoire darmziekte |
Huid- en onderhuidaandoeningen | Vaak | Uitslag, dermatitis en eczeem, |
Algemene aandoeningen en toedieningsplaatsstoornissen | Vaak | Reacties op de injectieplaatsa, |
a) Omvat: erytheem, reactie, oedeem, pijn, zwelling, hematoom op de injectieplaats.
Beschrijving van geselecteerde bijwerkingen
Infecties
In de placebogecontroleerde periode van klinische fase III-onderzoeken bij plaque-psoriasis, werden infecties gemeld bij 36,0% van de patiënten die gedurende maximaal 16 weken behandeld waren met bimekizumab, vergeleken met 22,5% van de met placebo behandelde patiënten. Ernstige infecties kwamen voor bij 0,3% van de patiënten behandeld met bimekizumab en 0% bij degenen die werden behandeld met placebo.
De meeste infecties waren niet-ernstige, lichte tot matige bovenste luchtweginfecties zoals nasofaryngitis. Er waren hogere percentages van orale en orofaryngeale candidiasis bij patiënten die werden behandeld met bimekizumab in overeenstemming met het werkingsmechanisme (respectievelijk 7,3% en 1,2% in vergelijking met 0% voor met placebo behandelde patiënten). Meer dan 98% van de gevallen waren niet-ernstig, licht of matig van aard, en vereisten geen stopzetting van de behandeling. Een licht verhoogde incidentie van orale candidiasis werd gemeld bij patiënten < 70 kg (8,5% vs. 7,0% bij patiënten ≥ 70 kg).
Over de gehele behandelperiode van fase III-onderzoeken bij plaque-psoriasis werden infecties gemeld bij 63,2% van de met bimekizumab behandelde patiënten (120,4 per 100 patiëntjaren). Ernstige infecties werden gemeld bij 1,5% van de met bimekizumab behandelde patiënten (1,6 per 100 patiëntjaren) (zie rubriek 4.4).
Infectiepercentages waargenomen in klinische fase III-onderzoeken bij PsA en axSpA (nr-axSpA en AS) waren vergelijkbaar met die waargenomen bij plaque-psoriasis, met uitzondering van de percentages bij orale en orofaryngeale candidiasis bij patiënten behandeld met bimekizumab, die lager waren met respectievelijk 2,3% en 0% bij PsA en respectievelijk 3,7% en 0,3% bij axSpA vergeleken met 0% bij placebo.
Infectiepercentages waargenomen in klinische fase III-onderzoeken bij HS waren vergelijkbaar met die waargenomen bij andere indicaties. In de placebogecontroleerde periode waren de percentages orale en orofaryngeale candidiasis bij patiënten behandeld met bimekizumab respectievelijk 7,1% en 0% vergeleken met 0% bij placebo.
Neutropenie
Neutropenie werd waargenomen in klinische fase III-onderzoeken met bimekizumab bij plaque-psoriasis. Over de gehele behandelperiode van fase III-onderzoeken werd neutropenie van graad 3/4 waargenomen bij 1% van de patiënten behandeld met bimekizumab.
De frequentie van neutropenie bij klinische onderzoeken naar PsA, axSpA (nr-axSpA en AS) en HS was vergelijkbaar met die waargenomen in klinische onderzoeken naar plaque-psoriasis.
Meer dan 80% van de gevallen was van voorbijgaande aard en vereiste geen stopzetting van de behandeling. Er werden geen ernstige infecties in verband gebracht met neutropenie.
Overgevoeligheid
Ernstige overgevoeligheidsreacties, waaronder anafylactische reacties, zijn waargenomen bij het gebruik van IL-17-remmers (zie rubriek 4.4).
Immunogeniciteit
Plaque-psoriasis
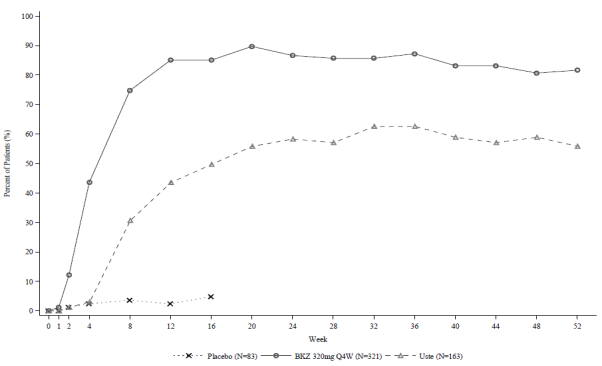
Ongeveer 45% van de patiënten met plaque-psoriasis behandeld met bimekizumab gedurende maximaal 56 weken met het aanbevolen doseringsschema (320 mg elke 4 weken tot week 16 en 320 mg elke 8 weken daarna) ontwikkelde antilichamen tegen het geneesmiddel. Van de patiënten die antilichamen tegen het geneesmiddel ontwikkelden, had ongeveer 34% (16% van alle patiënten behandeld met bimekizumab) antilichamen die werden geclassificeerd als neutraliserend.
Artritis psoriatica
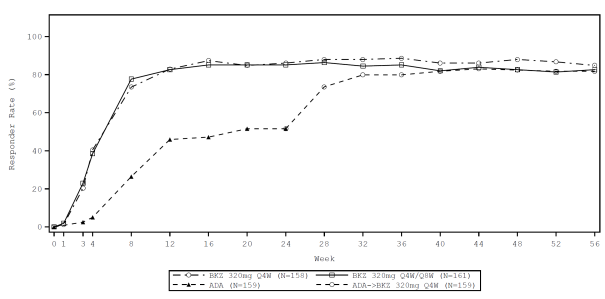
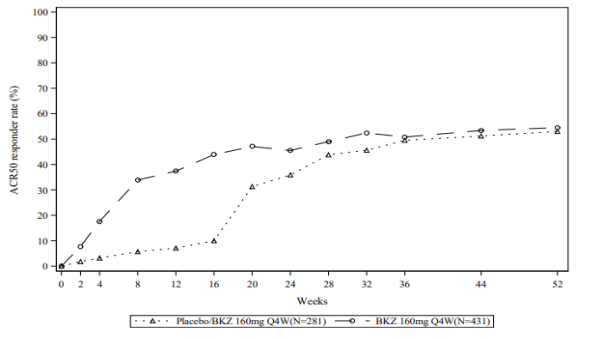
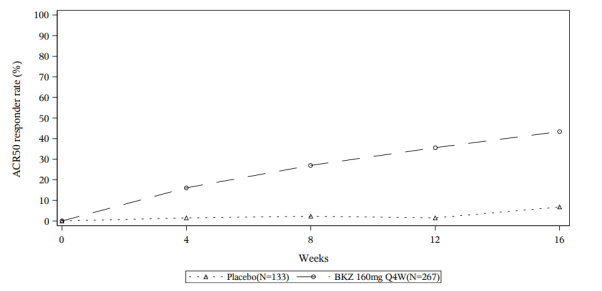
Ongeveer 31% van de patiënten met artritis psoriatica die tot 16 weken werden behandeld met bimekizumab volgens het aanbevolen doseringsschema (160 mg om de 4 weken) hadden antilichamen tegen het geneesmiddel. Van de patiënten met antilichamen tegen het geneesmiddel had ongeveer 33% (10% van alle patiënten behandeld met bimekizumab) antilichamen die geclassificeerd werden als neutraliserend. In week 52 had ongeveer 47% van de patiënten met artritis psoriatica die niet eerder waren blootgesteld aan een biologisch ziektemodificerend antireumaticum (biologic disease-modifying anti-rheumatic drug, bDMARD) in het BE OPTIMAL-onderzoek antilichamen tegen het geneesmiddel. Zij werden behandeld met bimekizumab volgens het aanbevolen doseringsschema (160 mg om de 4 weken). Van de patiënten met antilichamen tegen het geneesmiddel had ongeveer 38% (18% van alle patiënten in het BE OPTIMAL-onderzoek behandeld met bimekizumab) antilichamen die geclassificeerd werden als neutraliserend.
Axiale spondyloartritis (nr-axSpA en AS)
Ongeveer 57% van de patiënten met nr-axSpA die tot 52 weken werden behandeld met bimekizumab volgens het aanbevolen doseringsschema (160 mg elke 4 weken) hadden antilichamen tegen het geneesmiddel. Van de patiënten met antilichamen tegen het geneesmiddel had ongeveer 44% (25% van alle met bimekizumab behandelde patiënten) antilichamen die werden geclassificeerd als neutraliserend.
Ongeveer 44% van de patiënten met AS die tot 52 weken met bimekizumab werden behandeld volgens het aanbevolen doseringsschema (160 mg elke 4 weken) had antilichamen tegen het geneesmiddel. Van de patiënten met antilichamen tegen het geneesmiddel had ongeveer 44% (20% van alle met bimekizumab behandelde patiënten) antilichamen die werden geclassificeerd als neutraliserend.
Hidradenitis suppurativa
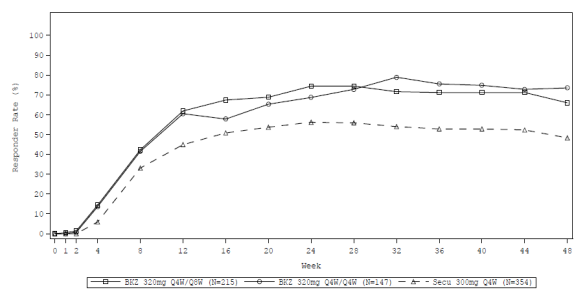
Ongeveer 59% van de HS-patiënten die tot 48 weken werden behandeld met bimekizumab volgens het aanbevolen doseringsschema (320 mg elke 2 weken tot week 16 en 320 mg elke 4 weken daarna) ontwikkelden antilichamen tegen het geneesmiddel. Van de patiënten die antilichamen tegen het geneesmiddel ontwikkelden, had ongeveer 63% (37% van alle patiënten behandeld met bimekizumab) antilichamen die werden geclassificeerd als neutraliserend.
Onder alle indicaties werd geen klinisch significante invloed op de klinische respons geassocieerd met de ontwikkeling van antilichamen tegen bimekizumab, en een associatie tussen immunogeniciteit en tijdens de behandeling optredende bijwerkingen is niet duidelijk vastgesteld.
Oudere patiënten (≥ 65 jaar)
Blootstelling is beperkt bij oudere patiënten.
Oudere patiënten kunnen meer risico lopen op het krijgen van bepaalde bijwerkingen zoals orale candidiasis, dermatitis en eczeem bij het gebruik van bimekizumab.
In de placebogecontroleerde periode van fase III-studies naar plaque-psoriasis werd orale candidiasis waargenomen bij 18,2% van de patiënten ≥ 65 jaar vs. 6,3% bij < 65 jaar, dermatitis en eczeem bij 7,3% van de patiënten ≥ 65 jaar vs. 2,8% bij < 65 jaar.
In de placebogecontroleerde periode van klinische fase III-studies naar artritis psoriatica werd orale candidiasis waargenomen bij 7,0% van de patiënten ≥ 65 jaar vs. 1,6% bij < 65 jaar, dermatitis en eczeem bij 1,2% van de patiënten ≥ 65 jaar vs. 2,0% bij < 65 jaar.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
UCB Pharma S.A.
Allée de la Recherche 60
B-1070 Bruxelles
België
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Bimzelx 160 mg, oplossing voor injectie in een voorgevulde spuit
EU/1/21/1575/001
EU/1/21/1575/002
EU/1/21/1575/003
EU/1/21/1575/004
Bimzelx 320 mg oplossing voor injectie in een voorgevulde spuit
EU/1/21/1575/009
EU/1/21/1575/010
Bimzelx 160 mg, oplossing voor injectie in een voorgevulde pen
EU/1/21/1575/005
EU/1/21/1575/006
EU/1/21/1575/007
EU/1/21/1575/008
Bimzelx 320 mg oplossing voor injectie in een voorgevulde pen
EU/1/21/1575/011
EU/1/21/1575/012
10. DATUM VAN HERZIENING VAN DE TEKST
04/2026
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4383923 | BIMZELX 160MG OPL INJ VOORGEVULDE SPUIT 2 | L04AC21 | € 1752,14 | - | Ja | € 12,8 | € 8,5 |