1. NAAM VAN HET GENEESMIDDEL
Trimbow 88 microgram/5 microgram/9 microgram inhalatiepoeder
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke afgegeven dosis (de dosis die uit het mondstuk komt) bevat 88 microgram beclometasondipropionaat, 5 microgram formoterolfumaraatdihydraat en 9 microgram glycopyrronium (als 11 microgram glycopyrroniumbromide).
Elke afgepaste dosis bevat 100 microgram beclometasondipropionaat, 6 microgram formoterolfumaraatdihydraat en 10 microgram glycopyrronium (als 12,5 microgram glycopyrroniumbromide).
Hulpstof met bekend effect:
Elke inhalatie bevat 9,9 mg lactosemonohydraat.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Inhalatiepoeder
Wit of bijna wit poeder in een witte inhalator (NEXThaler).
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Onderhoudsbehandeling bij volwassen patiënten met matige tot ernstige chronische obstructieve longziekte (COPD) die niet voldoende kunnen worden behandeld met een combinatie van een inhalatiecorticosteroïde en een langwerkende bèta‑2‑agonist of een combinatie van een langwerkende bèta‑2‑agonist en een langwerkende muscarineantagonist (voor effecten op het onder controle krijgen van de symptomen en het voorkomen van exacerbaties, zie rubriek 5.1).
4.2 Dosering en wijze van toediening
Dosering
De aanbevolen dosering is twee inhalaties tweemaal daags.
De maximumdosering is twee inhalaties tweemaal daags.
Bijzondere populaties
Ouderen
De dosering hoeft niet te worden aangepast bij oudere patiënten (65 jaar en ouder).
Nierfunctiestoornis
Trimbow kan worden gebruikt bij de aanbevolen dosering bij patiënten met een lichte (glomerulaire filtratiesnelheid [GFR] ≥50 tot <80 ml/min/1,73 m2) tot matige (GFR ≥30 tot <50 ml/min/1,73 m2) nierfunctiestoornis. Gebruik bij patiënten met een ernstige nierfunctiestoornis (GFR <30 ml/min/1,73 m2) of nierfalen (GFR <15 ml/min/1,73 m2) dat dialyse vereist, met name indien dit gepaard gaat met een significante daling van het lichaamsgewicht, mag alleen worden overwogen indien het verwachte voordeel opweegt tegen het mogelijke risico (zie rubriek 4.4 en 5.2).
Leverfunctiestoornis
Er zijn geen relevante gegevens over het gebruik van Trimbow bij patiënten met een ernstige leverfunctiestoornis (geclassificeerd als Child-Pugh-klasse C); het geneesmiddel moet met voorzichtigheid worden gebruikt bij deze patiënten (zie rubriek 4.4 en 5.2).
Pediatrische patiënten
Er is geen relevante toepassing van Trimbow bij kinderen (jonger dan 18 jaar) voor de indicatie van chronische obstructieve longziekte (COPD).
Wijze van toediening
Voor inhalatie.
De inhalator is een ademgestuurde inhalator. Om er zeker van te zijn dat het geneesmiddel op de juiste wijze wordt toegediend, dient een arts of andere beroepsbeoefenaar in de gezondheidszorg de patiënt het correcte gebruik van de inhalator te tonen en regelmatig te controleren dat de inhalatietechniek van de patiënt adequaat is (zie “Gebruiksaanwijzing” hieronder).
De patiënt dient te worden geadviseerd om de patiëntenbijsluiter zorgvuldig te lezen en zich te houden aan de gebruiksaanwijzingen zoals die in de bijsluiter staan.
De patiënt moet na elke inhalatie de mond spoelen of gorgelen met water zonder het in te slikken of deze moet de tanden poetsen (zie rubriek 4.4).
Gebruiksaanwijzing




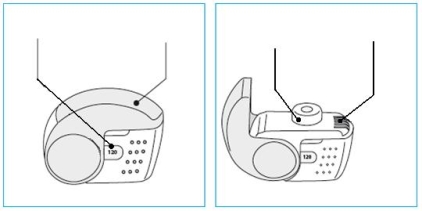
De patiënt informeren bij gebruik van een nieuwe inhalator
- Als de zak niet is verzegeld of als deze beschadigd is, of als de inhalator zichtbaar kapot is of beschadigingen heeft, moet de patiënt hem terugbrengen naar de apotheker van wie de patiënt hem heeft gekregen en een nieuwe vragen.
- De patiënt moet op het etiket op de verpakking de datum noteren waarop de zak geopend is.
- Het venster van de dosisteller moet op “120” staan. Als het weergegeven cijfer lager is dan “120”, moet de patiënt de inhalator terugbrengen naar de persoon die hem heeft gegeven en een nieuwe vragen.
Gebruik van de inhalator
De patiënt dient te staan of rechtop te zitten bij het inademen vanuit de inhalator. De stappen hieronder moeten worden gevolgd.
1. De patiënt dient de inhalator rechtop vast te houden, het aantal doses te controleren (elk getal tussen de “1” en “120” geeft aan dat er nog doses over zijn in de inhalator) en het beschermkapje volledig te openen.
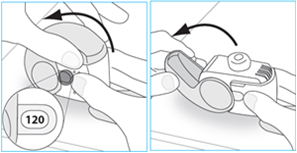
2. De patiënt dient zo langzaam en diep mogelijk als comfortabel voor hen is uit te ademen om de longen leeg te maken.
3. De patiënt dient de lippen rondom het mondstuk te sluiten, zonder de luchtinlaat te bedekken of via de luchtinlaat in te ademen.
4. De patiënt dient krachtig en diep via de mond in te ademen. Het kan zijn dat hij/zij iets proeft of een klikje hoort of voelt wanneer hij/zij de dosis inneemt.
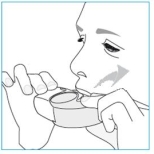
5. De patiënt dient vervolgens de inhalator uit de mond te nemen, de adem zo lang als comfortabel voor hem/haar is (5‑10 seconden lang) in te houden en daarna langzaam uit te ademen. De patiënt mag niet via de inhalator uitademen.
6. Na gebruik dient de patiënt de inhalator weer rechtop te kantelen, het beschermkapje volledig te sluiten en te controleren of de dosisteller met 1 dosis heeft afgeteld.
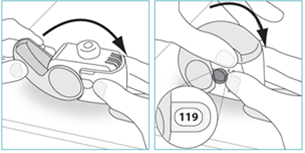
7. Als nog een dosis moet worden ingenomen, moet de patiënt de stappen 1 tot en met 6 herhalen.
NB: Het aantal inhalaties dat in het venster op het omhulsel wordt weergegeven, telt niet af wanneer het beschermkapje wordt gesloten als de patiënt niet heeft ingeademd via de inhalator. De patiënt dient geïnstrueerd te worden dat hij/zij het beschermkapje van de inhalator alleen mag openen wanneer dat nodig is. In het geval dat de patiënt de inhalator heeft geopend, maar niet heeft ingeademd en het beschermkapje wordt gesloten, gaat de dosis terug naar het poederreservoir in de inhalator; de volgende dosis kan op veilige wijze worden ingeademd.
Reinigen
Het is normaal gesproken niet nodig de inhalator schoon te maken. De patiënt mag de inhalator na gebruik schoonmaken met een droge doek of tissue, maar niet met water of andere vloeistoffen.
4.3 Contra‑indicaties
Overgevoeligheid voor de werkzame stoffen of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
In een 4 weken durend onderzoek was het veiligheidsprofiel van Trimbow inhalatiepoeder vergelijkbaar met het veiligheidsprofiel dat is waargenomen voor Trimbow aerosol.
De meest frequent gemelde bijwerkingen bij patiënten met COPD of astma met Trimbow aerosol zijn respectievelijk dysfonie (0,3% en 1,5%) en orale candidiasis (0,8% en 0,3%), die doorgaans in verband worden gebracht met inhalatiecorticosteroïden; spierspasmen (0,4% en 0,2%), die kunnen worden toegeschreven aan de langwerkende bèta‑2‑agonist en een droge mond (0,4% en 0,5%), dat een typisch anticholinerg effect is. Zo ook werd droge mond gemeld bij 2 patiënten (0,6%) met Trimbow inhalatiepoeder. Bij astmatische patiënten bestaat de neiging tot clustervorming van de bijwerkingen tijdens de eerste 3 maanden na het instellen van de behandeling en komen de bijwerkingen minder vaak voor bij langduriger gebruik (na een behandeling van 6 maanden).
Lijst van bijwerkingen in tabelvorm
Bijwerkingen die in verband worden gebracht met beclometasondipropionaat/formoterol/glycopyrronium die optraden tijdens klinische onderzoeken en ervaring na het in de handel brengen, alsmede bijwerkingen die worden vermeld voor de in de handel verkrijgbare afzonderlijke componenten, worden hieronder vermeld, onderverdeeld naar systeem/orgaanklasse en frequentie.
De frequenties worden als volgt gedefinieerd: zeer vaak (≥ 1/10); vaak (≥ 1/100, < 1/10); soms (≥ 1/1.000, < 1/100); zelden (≥ 1/10.000, < 1/1.000); zeer zelden (< 1/10.000) en niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Systeem/orgaanklasse volgens MedDRA | Bijwerking | Frequentie |
Infecties en parasitaire aandoeningen | Pneumonie (bij COPD‑patiënten), faryngitis, orale candidiasis, urineweginfectie1, nasofaryngitis1 | Vaak |
Griep1, orale schimmelinfectie, orofaryngeale candidiasis, slokdarmcandidiasis, (oro)faryngitis door schimmels, sinusitis1, rinitis1, gastro‑enteritis1, vulvovaginale candidiasis1 | Soms | |
Infectie van onderste luchtwegen (door schimmels) | Zelden | |
Bloed‑ en lymfestelselaandoeningen | Granulocytopenie1 | Soms |
Trombocytopenie1 | Zeer zelden | |
Immuunsysteemaandoeningen | Dermatitis allergisch1 | Soms |
Overgevoeligheidsreacties, waaronder erytheem, oedeem van lippen, gezicht, ogen en farynx | Zelden | |
Endocriene aandoeningen | Bijniersuppressie1 | Zeer zelden |
Voedings‑ en stofwisselingsstoornissen | Hypokaliëmie, hyperglykemie | Soms |
Verminderde eetlust | Zelden | |
Psychische stoornissen | Rusteloosheid1 | Soms |
Psychomotorische hyperactiviteit1, slaapstoornissen1, angst, depressie1, agressie1, gedragsveranderingen (voornamelijk bij kinderen)1 | Frequentie niet bekend | |
Insomnia | Zelden | |
Zenuwstelselaandoeningen | Hoofdpijn | Vaak |
Tremor, duizeligheid, dysgeusie1, hypo‑esthesie1 | Soms | |
Hypersomnie | Zelden | |
Oogaandoeningen | Gezichtsvermogen wazig1 (zie ook rubriek 4.4) | Frequentie niet bekend |
Glaucoom1, cataract1 | Zeer zelden | |
Evenwichtsorgaan‑ en ooraandoeningen | Otosalpingitis1 | Soms |
Hartaandoeningen | Atriumfibrillatie, elektrocardiogram QT verlengd, tachycardie, tachyaritmie1, hartkloppingen | Soms |
Angina pectoris (stabiel1 en onstabiel), extrasystolen (ventriculair1 en supraventriculair), nodaal ritme, sinusbradycardie | Zelden | |
Bloedvataandoeningen | Hyperemie1, overmatig blozen1, hypertensie | Soms |
Extravasatie | Zelden | |
Ademhalingsstelsel‑, borstkas‑ en mediastinumaandoeningen | Dysfonie | Vaak |
Astmatische crisis1, hoesten, productieve hoest1, keelirritatie, bloedneus1, faryngeaal erytheem | Soms | |
Paradoxaal bronchospasme1, exacerbatie van astma, orofaryngeale pijn, farynxontsteking, droge keel | Zelden | |
Dyspneu1 | Zeer zelden | |
Maagdarmstelselaandoeningen | Diarree1, droge mond, dysfagie1, nausea, dyspepsie1, branderig gevoel van de lippen1, tandcariës1, (afteuze) stomatitis | Soms |
Huid‑ en onderhuidaandoeningen | Rash1, urticaria, pruritus, hyperhidrose1 | Soms |
Angio‑oedeem1 | Zelden | |
Skeletspierstelsel‑ en bindweefselaandoeningen | Spierspasmen, myalgie, pijn in extremiteit1, skeletspierstelsel borstpijn1 | Soms |
Groeivertraging1 | Zeer zelden | |
Nier‑ en urinewegaandoeningen | Dysurie, urineretentie, nefritis1 | Zelden |
Algemene aandoeningen en toedieningsplaatsstoornissen | Vermoeidheid1 | Soms |
Asthenie | Zelden | |
Oedeem perifeer1 | Zeer zelden | |
Onderzoeken | C‑reactief proteïne verhoogd1, bloedplaatjestelling verhoogd1, vrije vetzuren verhoogd1, bloedinsuline verhoogd1, bloedketonlichaam verhoogd1, cortisol verlaagd1 | Soms |
Bloeddruk verhoogd1, bloeddruk verlaagd1 | Zelden | |
Botdichtheid verlaagd1 | Zeer zelden |
1 Bijwerkingen gemeld in de SPC van ten minste een van de afzonderlijke componenten, maar niet waargenomen als bijwerkingen in de klinische ontwikkeling van Trimbow
Van de waargenomen bijwerkingen treden de volgende doorgaans op bij:
Beclometasondipropionaat
Pneumonie, orale schimmelinfecties, infectie van de onderste luchtwegen door schimmels, dysfonie, keelirritatie, hyperglykemie, psychische stoornissen, cortisol verlaagd, wazig zien.
Formoterol
Hypokaliëmie, hyperglykemie, tremor, hartkloppingen, spierspasmen, elektrocardiogram QT verlengd, bloeddruk verhoogd, bloeddruk verlaagd, atriumfibrillatie, tachycardie, tachyaritmie, angina pectoris (stabiel en instabiel), ventriculaire extrasystolen, nodaal ritme.
Glycopyrronium
Glaucoom, atriumfibrillatie, tachycardie, hartkloppingen, een droge mond, tandcariës, dysurie, urineretentie, urineweginfectie.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem zoals vermeld in aanhangsel V.
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Chiesi Farmaceutici S.p.A.
Via Palermo 26/A
43122 Parma
Italië
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/17/1208/010
EU/1/17/1208/011
EU/1/17/1208/012
10. DATUM VAN HERZIENING VAN DE TEKST
03/2022
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau http://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4347779 | TRIMBOW 88/5 /9MCG INHALATIEPOEDER FL 1 (120D) | R03AL09 | € 64,11 | - | Ja | € 12,8 | € 8,5 |