1. NAAM VAN HET GENEESMIDDEL
Pentasa 500 mg tabletten met verlengde afgifte
Pentasa 1 g tabletten met verlengde afgifte
Pentasa Sachet 1 g granulaat met verlengde afgifte
Pentasa Sachet 2 g granulaat met verlengde afgifte
Pentasa Sachet 4 g granulaat met verlengde afgifte
Pentasa 1 g zetpillen
Pentasa 1 g/100 ml suspensie voor rectaal gebruik
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Werkzame stof: mesalazine.
Pentasa 500 mg tabletten met verlengde afgifte
1 tablet bevat 500 mg mesalazine.
Pentasa 1 g tabletten met verlengde afgifte
1 tablet bevat 1 g mesalazine.
Pentasa Sachet 1 g, 2 g en 4 g granulaat met verlengde afgifte
1 zakje bevat respectievelijk 1 g, 2 g en 4 g mesalazine.
Pentasa 1 g zetpillen
1 zetpil bevat 1 g mesalazine.
Pentasa 1 g/100 ml suspensie voor rectaal gebruik
100 ml suspensie voor rectaal gebruik bevat 1 g mesalazine (1 g/100 ml).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Pentasa 500 mg en 1 g tabletten met verlengde afgifte
Tabletten met verlengde afgifte
Pentasa Sachet 1 g, 2 g en 4 g granulaat met verlengde afgifte
Granulaat met verlengde afgifte
Pentasa 1 g zetpillen
Zetpillen
Pentasa 1 g/100 ml suspensie voor rectaal gebruik
Suspensie voor rectaal gebruik
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Tabletten en granulaat met verlengde afgifte
Symptomatische behandeling van colitis ulcerosa en de ziekte van Crohn ongeacht de lokalisatie, d.w.z. ook indien gelokaliseerd in het duodenum en jejunum. Preventie van recidieven bij colitis ulcerosa in remissie.
Zetpillen
Proctitis ulcerosa.
Suspensie voor rectaal gebruik
Behandeling van lichte tot matige ulceratieve proctosigmoïditis en linkszijdige colitis.
4.2 Dosering en wijze van toediening
Dosering
Tabletten en granulaat[1] met verlengde afgifte, voor orale toediening
Volwassenen en adolescenten
Aanvalsbehandeling: - colitis ulcerosa: 2 tot 4 g per dag.
- ziekte van Crohn: 4 g per dag.
Onderhoudsbehandeling: colitis ulcerosa: 1,5 tot 2 g per dag.
Pediatrische patiënten
Er zijn slechts beperkte gegevens over het effect bij kinderen (leeftijd 6 – 18 jaar).
Kinderen van 6 jaar en ouder
Aanvalsbehandeling:
- colitis ulcerosa en ziekte van Crohn: Individueel te bepalen, starten met 30 – 50 mg/kg/dag in verschillende doses. Maximale dosis: 75 mg/kg/dag in verschillende doses. De totale dosis mag niet 4 g/dag (maximale dosis voor volwassenen) overschrijden.
Onderhoudsbehandeling:
- colitis ulcerosa: Individueel te bepalen, starten met 15 – 30 mg/kg/dag in verschillende doses. De totale dosis mag niet 2 g/dag (aanbevolen dosis voor volwassenen) overschrijden.
In het algemeen wordt er aanbevolen dat de helft van de dosis voor volwassenen mag worden gegeven aan kinderen met een lichaamsgewicht tot 40 kg en de normale dosis voor volwassenen aan kinderen boven 40 kg.
Zetpillen
Volwassenen en adolescenten
Pediatrische patiënten
Er is weinig ervaring en er zijn slechts beperkte gegevens over het effect bij kinderen.
Suspensie voor rectaal gebruik
De dosering dient aangepast te worden aan de leeftijd en de ernst van de ziekte. In het algemeen wordt aanbevolen:
Volwassenen en adolescenten
1 g/100 ml/dag.
Pediatrische patiënten
Er is weinig ervaring en er zijn slechts beperkte gegevens over het effect bij kinderen.
Wijze van toediening
Tabletten
De tabletten doorslikken met water of een andere drank.
De tabletten mogen gebroken worden om het doorslikken te vergemakkelijken.
Granulaat (Pentasa Sachet)
Het granulaat wordt achteraan op de tong gestrooid en doorgeslikt met water of een andere drank. Het granulaat kan ook met wat yoghurt[2] of water worden gemengd en onmiddellijk worden ingenomen zonder op het granulaat te kauwen.
Uit praktische overwegingen worden de tabletten en het granulaat vóór inname het best niet in een drank opgelost.
De tabletten en het granulaat mogen niet gekauwd worden.
Bij maagklachten kunnen de tabletten of het granulaat tijdens of vlak na de maaltijd worden ingenomen.
Zetpillen
Het wordt aanbevolen om vóór toediening eerst naar het toilet te gaan.
Suspensie voor rectaal gebruik
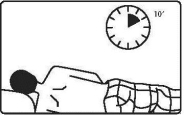
De suspensie wordt toegediend in liggende toestand, iedere avond vóór het slapengaan, gedurende minimaal twee weken. De maximale duur van de behandeling wordt aangepast volgens de evolutie van de ziekte. Het is aan te raden de suspensie gedurende minimaal 10 minuten op te houden in het rectum terwijl u blijft liggen.
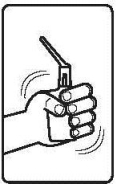
1. | Neem onmiddellijk vóór gebruik het flesje met de suspensie voor rectaal gebruik uit de aluminiumfolieverpakking en schud het goed. |
|
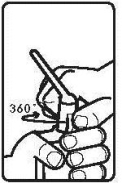
2. | Om de verzegeling te verbreken, draai het uiteinde van het flesje eenmaal volledig rond (na het draaien moet het uiteinde zich in dezelfde positie bevinden als vóór het draaien). |
|
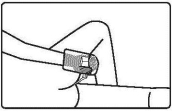
3. | Steek uw hand in een van de plastic wegwerpzakjes die meegeleverd zijn in de verpakking. |
|
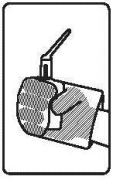
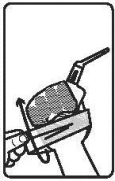
4. | Houd het flesje zoals wordt getoond op de afbeelding. |
|
5. | Om de suspensie voor rectaal gebruik toe te dienen, ga liggen op uw linkerzijde met uw linkerbeen gestrekt en uw rechterbeen naar voren gebogen om het evenwicht te bewaren. Breng het uiteinde van het flesje voorzichtig via de anus in. Oefen voldoende en constante druk uit met uw hand terwijl u de inhoud van het flesje toedient. De inhoud van het flesje moet binnen maximaal 30 – 40 seconden toegediend zijn. |
|
6. | Zodra het flesje leeg is, trek het uiteinde van het flesje uit de anus terwijl u blijft drukken op het flesje. |
|
7. | De suspensie moet worden opgehouden in de darm. Blijf ontspannen liggen in dezelfde houding als tijdens de toediening, gedurende 5 – 10 minuten of totdat de drang om de suspensie uit te stoten, verdwenen is. |
|
8. | Trek het plastic wegwerpzakje over het lege flesje. Gooi het weg en was uw handen. |
|
Opmerking: Wanneer u een beetje knoeit met de vloeistof, kunnen er bruine vlekken in beddengoed of kleding ontstaan die nog moeilijk te verwijderen zijn. Indien dit gebeurt, laat het bevlekte goed dan onmiddellijk weken. Gebruik bij voorkeur oud goed of ga vóór toediening eerst op een absorberende doek liggen.
4.3 Contra-indicaties
Overgevoeligheid voor mesalazine, voor salicylzuurderivaten of voor een van de in rubriek 6.1 vermelde hulpstoffen.
Ernstige lever- of nierfunctiestoornissen.
Enkel voor de tabletten en het granulaat
Maag- of duodenumulcera.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel:
De meest voorkomende bijwerkingen die in klinische studies zijn waargenomen, zijn diarree, misselijkheid, buikpijn, hoofdpijn, braken en huiduitslag. Overgevoeligheidsreacties en geneesmiddelenkoorts kunnen af en toe voorkomen. Er zijn ernstige bijwerkingen van de huid gemeld in verband met de behandeling met mesalazine, zoals geneesmiddelenreactie met eosinofilie en systemische symptomen (DRESS), Stevens-Johnson-syndroom (SJS) en toxische epidermale necrolyse (TEN) (zie rubriek 4.4).
Na rectale toediening kunnen lokale reacties optreden zoals pruritis, rectaal ongemak en urgentieplassen.
Frequentie van bijwerkingen gebaseerd op klinische studies en rapporten van postmarketingsurveillance
Orgaanklasse volgens MedDRA | vaak | zelden | zeer zelden | niet bekend |
Bloed- en lymfestelsel-aandoeningen |
|
| afwijkingen in de bloedtelling (anemie, aplastische anemie, agranulocytose, neutropenie, leukopenie (inclusief granulocytopenie), pancytopenie, trombocytopenie en eosinofilie (als deel van een allergische reactie)) |
|
Immuunsysteem-aandoeningen |
|
| overgevoeligheidsreactie inclusief anafylactische reactie |
|
Zenuwstelsel-aandoeningen | hoofdpijn | duizeligheid | perifere neuropathie | idiopathische intracraniële hypertensie (zie rubriek 4.4) |
Hartaandoeningen |
| myocarditis* en pericarditis* |
|
|
Ademhalingsstelsel-, borstkas- en mediastinum-aandoeningen |
|
| allergische en fibrotische longreacties (inclusief dyspneu, hoesten, bronchospasme, allergische alveolitis, pulmonale eosinofilie, interstitiële longaandoening, longinfiltratie, pneumonitis) |
|
Maag-darmstelsel-aandoeningen | diarree, buikpijn, misselijkheid, braken, verlies van eetlust, winderigheid | verhoogde amylase, acute pancreatitis* | pancolitis |
|
Lever- en galaandoeningen |
|
| verhoging in transaminasen, verhoging in cholestaseparameters (bv. alkalische fosfatase, gamma-glutamyltransferase en bilirubine), hepatotoxiciteit (inclusief hepatitis*, cholestatische hepatitis, cirrose, leverfalen) |
|
Huid- en onderhuid-aandoeningen | huiduitslag (inclusief urticaria, erytheem) | fotosensitiviteit** | reversibele alopecia, allergische dermatitis, erythema multiforme | Stevens-Johnson-syndroom (SJS), toxische epidermale necrolyse (TEN), geneesmiddelen-reactie met eosinofilie en systemische symptomen (DRESS) |
Skeletspierstelsel- en bindweefsel-aandoeningen |
|
| myalgie, artralgie, lupus erythematosusachtig syndroom (systemische lupus erythematosus) |
|
Nier- en urineweg-aandoeningen |
|
| nierfunctiestoornis (inclusief acute en chronische interstitiële nefritis*, nefrotisch syndroom, nierinsufficiëntie) | nefrolithiase***, verkleuring van de urine*** |
Voortplantings-stelsel- en borstaandoeningen |
|
| oligospermie (reversibel) |
|
Algemene aandoeningen en toedieningsplaats-stoornissen | alleen met de suspensie voor rectaal gebruik: anaal ongemak en irritatie op de plaats van applicatie, pruritis (anaal) en rectale tenesmus |
| geneesmiddelenkoorts |
|
* Het mechanisme van mesalazinegeïnduceerde myocarditis en pericarditis, pancreatitis, nefritis en hepatitis is onbekend, maar kan een allergische oorzaak hebben.
** Fotosensitiviteit: Bij patiënten met reeds bestaande huidaandoeningen zoals atopische dermatitis en atopisch eczeem worden ernstigere reacties gemeld.
*** Zie rubriek 4.4. voor meer informatie.
Het is belangrijk te weten dat verscheidene van bovengenoemde stoornissen ook door de inflammatoire darmaandoening kunnen veroorzaakt worden.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (www.fagg.be)
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
E-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Ferring N.V., The Crescent Business Center
Lenniksebaan 451, B-1070 Anderlecht
8. NUMMERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Pentasa 500 mg tabletten met verlengde afgifte (blisterverpakking): BE156055
Pentasa 500 mg tabletten met verlengde afgifte (pot): BE230991
Pentasa 1 g tabletten met verlengde afgifte: BE477306
Pentasa Sachet 1 g granulaat met verlengde afgifte: BE209772
Pentasa Sachet 2 g granulaat met verlengde afgifte: BE343734
Pentasa Sachet 4 g granulaat met verlengde afgifte: BE506604
Pentasa 1 g zetpillen: BE164972
Pentasa 1 g/100 ml suspensie voor rectaal gebruik: BE150683
10. DATUM VAN HERZIENING VAN DE TEKST
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 0251520 | PENTASA SUSP RECT 7X1G/100ML | A07EC02 | € 20,88 | - | Ja | - | - |
| 0287698 | PENTASA COMP 300X500MG | A07EC02 | € 121,78 | - | Ja | - | - |
| 0287706 | PENTASA COMP 90X500MG | A07EC02 | € 23,33 | - | Ja | - | - |
| 1550771 | PENTASA SACH GRAN 50 X 1 G | A07EC02 | € 40,53 | - | Ja | € 10,19 | € 6,06 |
| 1550789 | PENTASA SACH GRAN 150 X 1 G | A07EC02 | € 90,76 | - | Ja | € 15,9 | € 10,5 |
| 2744910 | PENTASA SACH GRAN 60 X 2 G | A07EC02 | € 78,25 | - | Ja | € 12,8 | € 8,5 |
| 3010154 | PENTASA SUPP 28X1G | A07EC02 | € 38,98 | - | Ja | € 9,82 | € 5,84 |
| 3786829 | PENTASA GRAN VERLENGDE AFGIFTE 4G ZAKJE 30 | A07EC02 | € 78,25 | - | Ja | € 12,8 | € 8,5 |