BIJLAGE I
SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Ilumetri 100 mg oplossing voor injectie in voorgevulde spuit
Ilumetri 200 mg oplossing voor injectie in voorgevulde spuit
Ilumetri 100 mg oplossing voor injectie in voorgevulde pen
Ilumetri 200 mg oplossing voor injectie in voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Ilumetri 100 mg oplossing voor injectie in voorgevulde spuit
Elke voorgevulde spuit bevat 100 mg tildrakizumab in 1 ml.
Ilumetri 200 mg oplossing voor injectie in voorgevulde spuit
Elke voorgevulde spuit bevat 200 mg tildrakizumab in 2 ml.
Ilumetri 100 mg oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 100 mg tildrakizumab in 1 ml.
Ilumetri 200 mg oplossing voor injectie in voorgevulde pen
Elke voorgevulde pen bevat 200 mg tildrakizumab in 2 ml.
Tildrakizumab is een gehumaniseerd IgG1/k monoklonaal antilichaam dat met behulp van recombinant-DNA-technologie in ovariumcellen van de Chinese hamster (CHO-cellen) wordt geproduceerd.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
Hulpstof met bekend effect
Elke Ilumetri 100 mg oplossing voor injectie in voorgevulde spuit bevat 0,5 mg polysorbaat 80 (E 433).
Elke Ilumetri 200 mg oplossing voor injectie in voorgevulde spuit bevat 1 mg polysorbaat 80 (E 433).
Elke Ilumetri 100 mg oplossing voor injectie in voorgevulde pen bevat 0,5 mg polysorbaat 80 (E 433).
Elke Ilumetri 200 mg oplossing voor injectie in voorgevulde pen bevat 1 mg polysorbaat 80 (E 433).
3. FARMACEUTISCHE VORM
Oplossing voor injectie (injectievloeistof)
De oplossing is helder tot licht opalescent en kleurloos tot lichtgeel. De pH van de oplossing varieert van 5,7 tot 6,3 en de osmolaliteit ligt tussen 258 en 311 mOsm/kg.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Ilumetri is geïndiceerd voor de behandeling van volwassenen met matige tot ernstige plaque psoriasis die in aanmerking komen voor systemische behandeling.
4.2 Dosering en wijze van toediening
Dit geneesmiddel is bedoeld voor gebruik onder begeleiding en supervisie van artsen met ervaring in het diagnosticeren en behandelen van plaque psoriasis.
Dosering
De aanbevolen dosis is 100 mg via subcutane injectie in week 0, week 4 en daarna om de 12 weken.
Naar oordeel van de arts kan bij patiënten met een zware ziektelast of bij patiënten met een lichaamsgewicht boven de 90 kg een dosis van 200 mg een grotere werkzaamheid vertonen.
Stopzetting van de behandeling dient te worden overwogen bij patiënten die na 28 weken niet op de behandeling hebben gereageerd. Sommige patiënten met een aanvankelijke gedeeltelijke respons, kunnen vervolgens verbeteren wanneer de behandeling wordt voortgezet na de periode van 28 weken.
Dosis overgeslagen
Indien een dosis is overgeslagen, dient de dosis zo snel mogelijk te worden toegediend. Daarna kan de dosering worden voortgezet volgens het reguliere schema.
Speciale populaties
Ouderen
Er zijn geen dosisaanpassingen vereist (zie rubriek 5.2).
Nier- of leverfunctiestoornis
Ilumetri werd niet onderzocht bij deze patiëntpopulaties. Er kunnen geen specifieke dosisaanbevelingen worden gegeven. Voor verdere informatie over de eliminatie van tildrakizumab, zie rubriek 5.2.
Pediatrische patiënten
De veiligheid en werkzaamheid van Ilumetri bij kinderen en jongeren tot 18 jaar zijn nog niet vastgesteld. Er zijn geen gegevens beschikbaar.
Wijze van toediening
Dit geneesmiddel wordt toegediend als een subcutane injectie. De injectieplaatsen moeten worden afgewisseld. Ilumetri mag niet worden geïnjecteerd op plaatsen waar de huid is aangetast door plaque psoriasis of waar de huid gevoelig, gekneusd, rood, verhard of verdikt, of schilferig is. De spuit of pen mag niet worden geschud. Elke spuit of pen is uitsluitend voor eenmalig gebruik.
Na een goede training in de subcutane injectietechniek, kunnen patiënten Ilumetri zelf injecteren indien de arts dit geschikt vindt. De arts moet echter wel zorgen voor een geschikte follow-up van de patiënten. Patiënten moeten worden geïnstrueerd om de volledige hoeveelheid tildrakizumab te injecteren volgens de instructies in de bijsluiter. De bijsluiter bevat uitgebreide instructies voor het toedienen.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
Actieve infectie van klinische betekenis, bv. actieve tuberculose (zie rubriek 4.4).
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De meest voorkomende bijwerkingen waren infecties van de bovenste luchtwegen (12,6%), hoofdpijn (4,0%), diarree (1,6%), gastro-enteritis (1,5%), rugpijn (1,5%), misselijkheid (1,3%) en pijn op de injectieplaats (1,3%).
Overzicht van bijwerkingen in tabelvorm
Bijwerkingen van klinische onderzoeken (tabel 1) worden vermeld volgens MedDRA systeem/orgaanklasse (system organ class, SOC) en frequentie gebaseerd op de volgende afspraak: zeer vaak (≥1/10); vaak (≥1/100 tot <1/10); soms (≥1/1.000 tot <1/100); zelden (≥1/10.000 tot <1/1.000); zeer zelden (<1/10.000); en niet bekend (kan met de beschikbare gegevens niet worden bepaald). Binnen elke frequentiegroep worden bijwerkingen weergegeven op volgorde van afnemende ernst.
Tabel 1. Lijst van bijwerkingen
MedDRA Systeem/orgaanklasse | Voorkeursterm | Frequentiecategorie |
Infecties en parasitaire aandoeningen | Infecties van de bovenste luchtwegena | Zeer vaak |
Zenuwstelselaandoeningen | Hoofdpijn | Vaak |
Maagdarmstelselaandoeningen | Gastro-enteritis | Vaak |
Diarree | Vaak | |
Misselijkheid | Vaak | |
Algemene aandoeningen en toedieningsplaatsstoornissen | Rugpijn | Vaak |
Pijn op de injectieplaats | Vaak |
aInclusief nasofaryngitis.
Veiligheid op lange termijn
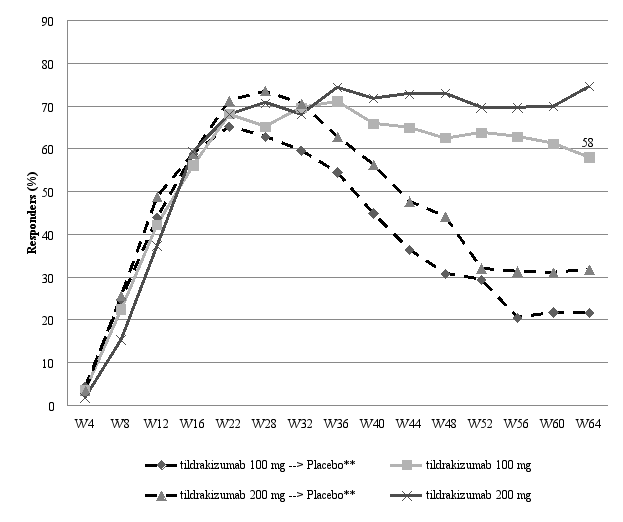
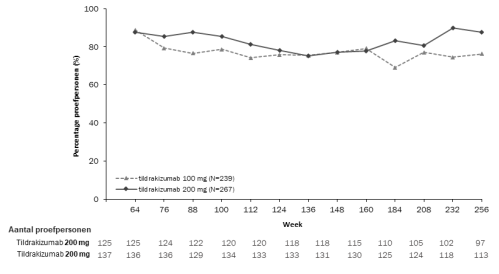
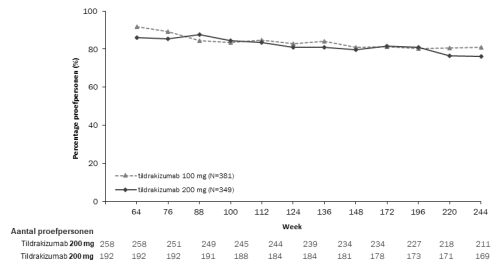
Het veiligheidsprofiel van tildrakizumab dat werd waargenomen tijdens de langlopende uitbreidingsperioden van reSURFACE 1 en reSURFACE 2 was consistent met dat van de dubbelblinde perioden.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg worden verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten, www.fagg.be, Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
Nederland
Nederlands Bijwerkingen Centrum Lareb, Website: www.lareb.nl.
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Almirall, S.A.
Ronda General Mitre, 151
08022 Barcelona
Spanje
8. NUMMERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/18/1323/001
EU/1/18/1323/002
EU/1/18/1323/003
EU/1/18/1323/004
EU/1/18/1323/005
10. DATUM VAN HERZIENING VAN DE TEKST
06/2024
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4166740 | ILUMETRI 100MG OPL INJ VOORGEVULDE SPUIT 1X1ML | L04AC17 | € 2817,11 | - | Ja | € 12,8 | € 8,5 |
| 4575163 | ILUMETRI 200MG OPL INJ VOORGEVULDE SPUIT 1X2ML | € 2817,11 | - | Ja | € 12,8 | € 8,5 | |
| 4800777 | ILUMETRI 100MG OPL INJ VOORGEVULDE PEN 1X1ML | € 2817,11 | - | Ja | € 12,8 | € 8,5 |