1. NAAM VAN HET GENEESMIDDEL
Aimovig 70 mg oplossing voor injectie in een voorgevulde spuit
Aimovig 140 mg oplossing voor injectie in een voorgevulde spuit
Aimovig 70 mg oplossing voor injectie in een voorgevulde pen
Aimovig 140 mg oplossing voor injectie in een voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Aimovig 70 mg oplossing voor injectie in een voorgevulde spuit
Elke voorgevulde spuit bevat 70 mg erenumab.
Aimovig 140 mg oplossing voor injectie in een voorgevulde spuit
Elke voorgevulde spuit bevat 140 mg erenumab.
Aimovig 70 mg oplossing voor injectie in een voorgevulde pen
Elke voorgevulde pen bevat 70 mg erenumab.
Aimovig 140 mg oplossing voor injectie in een voorgevulde pen
Elke voorgevulde pen bevat 140 mg erenumab.
Erenumab is een volledig humaan IgG2‑monoklonaal antilichaam vervaardigd door middel van DNA‑recombinatietechniek in ovariumcellen van Chinese hamsters (CHO‑cellen).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie (injectievloeistof)
De oplossing is helder tot opaalachtig, kleurloos tot lichtgeel.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Aimovig is geïndiceerd voor profylaxe van migraine bij volwassenen die ten minste 4 migrainedagen per maand hebben.
4.2 Dosering en wijze van toediening
De behandeling dient te worden opgestart door artsen die ervaring hebben met de diagnose en behandeling van migraine.
Dosering
De behandeling is bedoeld voor patiënten met ten minste 4 migrainedagen per maand bij het starten van de behandeling met erenumab.
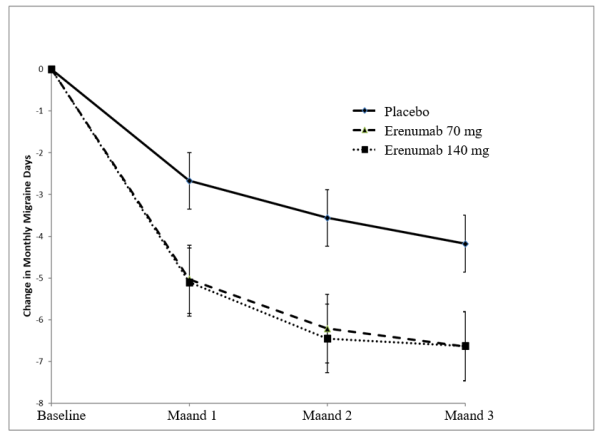
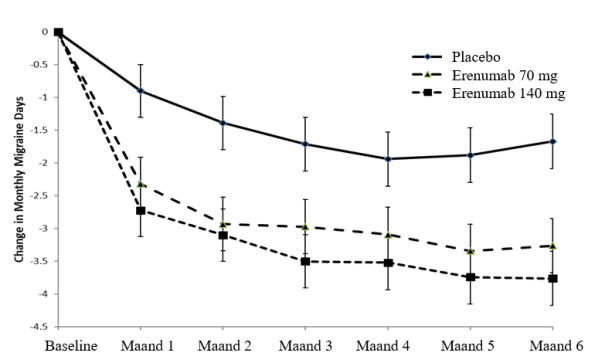
De aanbevolen dosis is 70 mg erenumab elke 4 weken. Sommige patiënten kunnen baat hebben bij een dosis van 140 mg elke 4 weken (zie rubriek 5.1).
Elke dosis van 140 mg wordt gegeven in één subcutane injectie van 140 mg of in twee subcutane injecties van 70 mg.
Uit klinische onderzoeken is gebleken dat bij de meeste patiënten die reageren op de behandeling er binnen 3 maanden sprake was van klinisch voordeel. Bij patiënten die na 3 maanden behandeling geen respons hebben vertoond moet worden overwogen de behandeling te staken. Daarna is regelmatige evaluatie van de noodzaak om de behandeling voort te zetten aanbevolen.
Speciale populaties
Ouderen (65 jaar en ouder)
Aimovig is niet onderzocht bij oudere patiënten. Er is geen dosisaanpassing vereist aangezien de farmacokinetiek van erenumab niet door leeftijd wordt beïnvloed.
Nierfunctiestoornis/leverfunctiestoornis
Bij patiënten met een lichte tot matige nier‑ of leverfunctiestoornis is geen dosisaanpassing noodzakelijk (zie rubriek 5.2).
Pediatrische patiënten
De veiligheid en werkzaamheid van Aimovig bij kinderen jonger dan 18 jaar zijn nog niet vastgesteld. Er zijn geen gegevens beschikbaar.
Wijze van toediening
Aimovig is voor subcutaan gebruik.
Aimovig is, na gepaste training, bedoeld voor zelftoediening door de patiënt. De injecties kunnen ook worden toegediend door een ander persoon die op juiste wijze is geïnstrueerd. De injectie kan worden toegediend in de buik, het bovenbeen of in de buitenkant van de bovenarm (de arm mag alleen worden gebruikt als de injectie wordt toegediend door een ander persoon; zie rubriek 5.2). De injectieplaatsen moeten worden afgewisseld en er mogen geen injecties worden toegediend op plekken waar de huid gevoelig, gekneusd, rood of hard is.
Voorgevulde spuit
De gehele inhoud van de Aimovig voorgevulde spuit moet worden geïnjecteerd. Elke voorgevulde spuit is uitsluitend bedoeld voor eenmalig gebruik en zodanig ontworpen dat de gehele inhoud wordt afgegeven zonder dat er iets achterblijft.
Uitgebreide instructies voor toediening staan vermeld in de instructies voor gebruik in de bijsluiter.
Voorgevulde pen
De gehele inhoud van de Aimovig voorgevulde pen moet worden geïnjecteerd. Elke voorgevulde pen is uitsluitend bedoeld voor eenmalig gebruik en zodanig ontworpen dat de gehele inhoud wordt afgegeven zonder dat er iets achterblijft.
Uitgebreide instructies voor toediening staan vermeld in de instructies voor gebruik in de bijsluiter.
4.3 Contra‑indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
Een totaal van meer dan 2.500 patiënten (meer dan 2.600 patiëntjaren) zijn met Aimovig behandeld in registratieonderzoeken. Van deze patiënten werden meer dan 1.300 patiënten gedurende ten minste 12 maanden blootgesteld en 218 patiënten werden gedurende 5 jaar blootgesteld. Het algemeen veiligheidsprofiel van Aimovig bleef consistent gedurende 5 jaar langdurige openlabel behandeling.
De bijwerkingen voor 70 mg en 140 mg waren injectieplaatsreacties (5,6%/4,5%), constipatie (1,3%/3,2%), spierspasmen (0,1%/2,0%) en pruritus (0,7%/1,8%). De meeste reacties waren licht tot matig van ernst. Minder dan 2% van de patiënten in deze onderzoeken staakte de behandeling vanwege bijwerkingen.
Lijst van bijwerkingen in tabelvorm
In tabel 1 staan alle bijwerkingen vermeld die zich voordeden bij met Aimovig behandelde patiënten tijdens de 12 weken durende placebogecontroleerde periodes van de onderzoeken evenals in de post-marketingsetting. Binnen elke systeem/orgaanklasse zijn de bijwerkingen gerangschikt naar frequentie, met de meest voorkomende bijwerkingen als eerste. Binnen elke frequentiegroep zijn de bijwerkingen vermeld in volgorde van afnemende ernst. Daarnaast is de overeenkomende frequentiecategorie voor elke bijwerking gebaseerd op de volgende afspraak: zeer vaak (≥ 1/10), vaak (≥ 1/100, < 1/10), soms (≥ 1/1.000, < 1/100), zelden (≥ 1/10.000, < 1/1.000), zeer zelden (< 1/10.000), niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Tabel 1 Lijst van bijwerkingen
Systeem/orgaanklasse | Bijwerking | Frequentiecategorie |
Immuunsysteemaandoeningen | Overgevoeligheidsreactiesa waaronder anafylaxie, angio-oedeem, rash, zwelling/oedeem en urticaria | Vaak |
Maagdarmstelselaandoeningen | Constipatie | Vaak |
| Orale aftenb | Niet bekend |
Huid‑ en onderhuidaandoeningen | Pruritusc | Vaak |
| Alopecia | Niet bekend |
Skeletspierstelsel‑ en bindweefselaandoeningen | Spierspasmen | Vaak |
Algemene aandoeningen en toedieningsplaatsstoornissen | Injectieplaatsreactiesa | Vaak |
a Zie rubriek ‘Beschrijving van geselecteerde bijwerkingen’ hieronder. | ||
d Rash omvat de termen papulaire rash, exfoliatieve rash, erythemateuze rash, urticaria, blaar. | ||
Beschrijving van geselecteerde bijwerkingen
Injectieplaatsreacties
In de geïntegreerde 12 weken durende placebogecontroleerde fase van de onderzoeken waren injectieplaatsreacties licht en meestal van voorbijgaande aard. Er was één geval van het staken van de behandeling bij een patiënt die de 70 mg dosis kreeg vanwege uitslag op de injectieplaats. De meest voorkomende injectieplaatsreacties waren gelokaliseerde pijn, erytheem en pruritus. De pijn op de injectieplaats verdween meestal binnen 1 uur na toediening.
Huid- en overgevoeligheidsreacties
In de geïntegreerde 12 weken durende placebogecontroleerde fase van de onderzoeken werden niet-ernstige gevallen van huiduitslag, pruritus en zwelling/oedeem waargenomen. Deze waren in de meeste gevallen licht en leidden niet tot het staken van de behandeling.
In de postmarketingsetting werden gevallen van anafylaxie en angio-oedeem werden waargenomen.
Immunogeniciteit
Tijdens de dubbelblinde behandelfase van de klinische onderzoeken was de incidentie van de ontwikkeling van antilichamen tegen erenumab 6,3% (56/884) bij personen die een dosis van 70 mg erenumab kregen (3 van hen hadden in vitro neutraliserende activiteit) en 2,6% (13/504) bij degenen die de dosis van 140 mg erenumab kregen (bij geen van deze personen was sprake van in vitro neutraliserende activiteit). In een open-label onderzoek met een behandeling tot 256 weken, was de incidentie van de ontwikkeling van antilichamen tegen erenumab 11,0% (25/225) bij patiënten die gedurende het hele onderzoek slechts 70 mg of 140 mg Aimovig kregen (van wie 2 in vitro neutraliserende activiteit). De ontwikkeling van antilichamen tegen erenumab had geen invloed op de werkzaamheid of veiligheid van erenumab.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Ierland
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/18/1293/001‑006
10. DATUM VAN HERZIENING VAN DE TEKST
19.12.2024
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau http://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3954039 | AIMOVIG 140MG OPL INJ VOORGEVULDE PEN 1 | N02CD01 | € 470,47 | - | Ja | € 12,8 | € 8,5 |