SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Taltz 80 mg oplossing voor injectie in voorgevulde pen.
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke voorgevulde pen bevat 80 mg ixekizumab in 1 ml.
Ixekizumab is geproduceerd in CHO-cellen met behulp van DNA-recombinatietechniek.
Hulpstof met bekend effect:
Eén ml oplossing bevat 0,30 mg polysorbaat 80.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1
3. FARMACEUTISCHE VORM
Oplossing voor injectie
De oplossing is helder en kleurloos tot lichtgeel, met een pH van niet minder dan 5,2 en niet meer
dan 6,2 en een osmolariteit van minimaal 235 mOsm/kg en maximaal 360 mOsm/kg.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Plaque psoriasis
Taltz is geïndiceerd voor de behandeling van matige tot ernstige plaque psoriasis bij volwassenen die in aanmerking komen voor systemische therapie.
Pediatrische plaque psoriasis
Taltz is geïndiceerd voor de behandeling van matige tot ernstige plaque psoriasis bij kinderen vanaf de leeftijd van 6 jaar en met een lichaamsgewicht van ten minste 25 kg en adolescenten die in aanmerking komen voor systemische therapie.
Artritis psoriatica
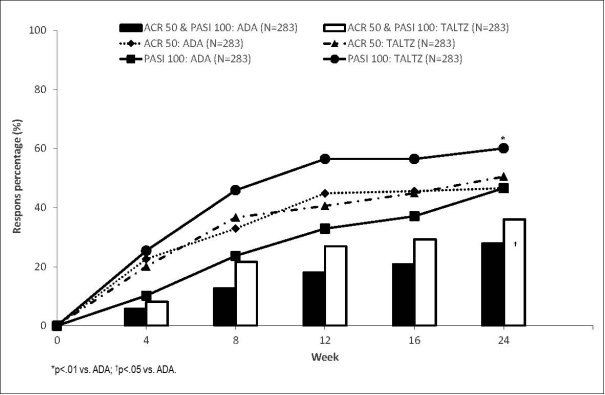
Taltz, alleen of in combinatie met methotrexaat, is geïndiceerd voor de behandeling van actieve artritis psoriatica bij volwassen patiënten die één of meer therapieën met disease-modifying antirheumatic drugs (DMARD’s) niet verdroegen of daar ontoereikend op reageerden (zie rubriek 5.1).
Axiale spondyloartritis
Spondylitis ankylopoetica (radiografische axiale spondyloartritis)
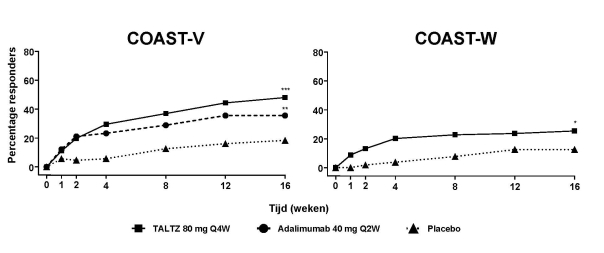
Taltz is geïndiceerd voor de behandeling van volwassenen met actieve spondylitis ankylopoetica die ontoereikend reageerden op conventionele therapie.
Niet-radiografische axiale spondyloartritis
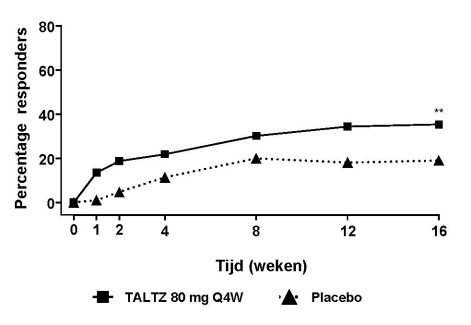
Taltz is geïndiceerd voor de behandeling van volwassenen met actieve niet-radiografische axiale spondyloartritis met objectieve verschijnselen van ontsteking zoals aangetoond door een verhoogd C-reactief proteïne (CRP) en/of magnetische kernspinresonantie (MRI) die ontoereikend reageerden op niet-steroïdale ontstekingsremmers (NSAID’s).
Juveniele idiopathische artritis (JIA)
Juveniele artritis psoriatica (JPsA)
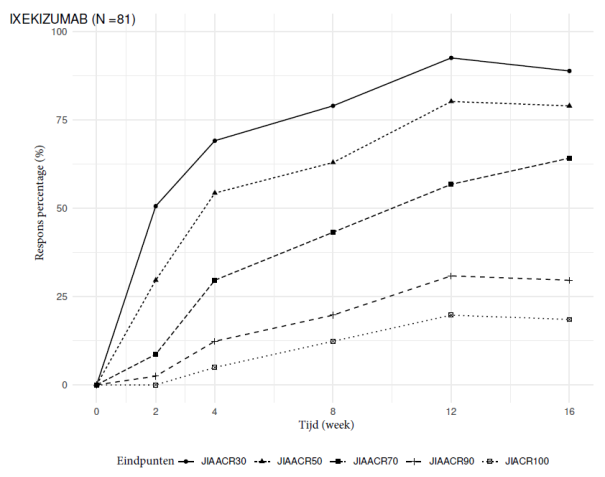
Taltz, alleen of in combinatie met methotrexaat, is geïndiceerd voor de behandeling van actieve JPsA bij patiënten van 6 jaar en ouder en met een lichaamsgewicht van ten minste 25 kg, die ontoereikend hebben gereageerd op conventionele therapie of die conventionele therapie niet verdroegen.
Aan enthesitis gerelateerde artritis (ERA)
Taltz, alleen of in combinatie met methotrexaat, is geïndiceerd voor de behandeling van actieve ERA bij patiënten van 6 jaar en ouder en met een lichaamsgewicht van ten minste 25 kg, die ontoereikend hebben gereageerd op conventionele therapie of die conventionele therapie niet verdroegen.
4.2 Dosering en wijze van toediening
Dit geneesmiddel is bedoeld voor gebruik onder begeleiding en supervisie van een arts met ervaring in de diagnose en behandeling van aandoeningen waar het voor is geïndiceerd.
Dosering
Plaque psoriasis bij volwassenen
De aanbevolen dosis is 160 mg per subcutane injectie (twee injecties van 80 mg) in week 0, gevolgd door 80 mg (één injectie) in de weken 2, 4, 6, 8, 10, en 12, daarna een onderhoudsdosering van 80 mg (één injectie) elke 4 weken (Q4W).
Pediatrische plaque psoriasis (6 jaar en ouder)
Bij kinderen onder de leeftijd van 6 jaar zijn geen werkzaamheids- en veiligheidsgegevens beschikbaar (zie rubriek 5.1). Een dosering voor een lichaamsgewicht minder dan 25 kg wordt door de beschikbare gegevens niet onderbouwd.
De aanbevolen dosering die via subcutane injectie aan kinderen wordt gegeven, is gebaseerd op de volgende gewichtsklassen:
Lichaamsgewicht kinderen | Aanbevolen startdosering (week 0) | Aanbevolen dosering elke 4 weken (Q4W) hierna |
Hoger dan 50 kg | 160 mg (twee injecties van 80 mg) | 80 mg |
25 tot 50 kg | 80 mg | 40 mg |
Indien de presentatie van 40 mg niet beschikbaar is, moeten doses ixekizumab van 40 mg worden bereid en toegediend door een gekwalificeerde zorgverlener, daarbij gebruik makend van de commercieel verkrijgbare Taltz 80 mg voorgevulde injectiespuit.
Gebruik de Taltz 80 mg voorgevulde pen alleen bij kinderen die een dosis van 80 mg nodig hebben en geen dosisvoorbereiding nodig hebben.
Taltz wordt niet aanbevolen voor gebruik bij kinderen met een lichaamsgewicht van minder dan 25 kg. Het lichaamsgewicht van kinderen moet vóór de toediening worden geregistreerd en regelmatig opnieuw worden gecontroleerd.
Artritis psoriatica
De aanbevolen dosis is 160 mg per subcutane injectie (twee injecties van 80 mg) in week 0, gevolgd door 80 mg (één injectie) elke 4 weken hierna. Voor patiënten met artritis psoriatica met gelijktijdig matige tot ernstige plaque psoriasis is de aanbevolen dosering hetzelfde als bij plaque psoriasis.
Axiale spondyloartritis (radiografisch en niet-radiografisch)
De aanbevolen dosis is 160 mg per subcutane injectie (twee injecties van 80 mg) in week 0, gevolgd door 80 mg elke 4 weken (zie rubriek 5.1 voor meer informatie).
Juveniele idiopathische artritis (6 jaar en ouder)
Juveniele artritis psoriatica of aan enthesitis gerelateerde artritis
Bij kinderen onder de leeftijd van 6 jaar zijn geen werkzaamheids- en veiligheidsgegevens beschikbaar (zie rubriek 5.1). Een dosering voor een lichaamsgewicht minder dan 25 kg wordt door de beschikbare gegevens niet onderbouwd.
De aanbevolen dosering die via subcutane injectie aan kinderen wordt gegeven, is gebaseerd op de volgende gewichtsklassen:
Lichaamsgewicht kinderen | Aanbevolen startdosering (week 0) | Aanbevolen dosering elke 4 weken (Q4W) hierna |
Hoger dan 50 kg | 160 mg (twee injecties van 80 mg) | 80 mg |
25 tot 50 kg | 80 mg | 40 mg |
Indien de presentatie van 40 mg niet beschikbaar is, moeten doses ixekizumab van 40 mg worden bereid en toegediend door een gekwalificeerde zorgverlener, daarbij gebruik makend van de commercieel verkrijgbare Taltz 80 mg voorgevulde injectiespuit.
Gebruik de Taltz 80 mg voorgevulde pen alleen bij kinderen die een dosis van 80 mg nodig hebben en geen dosisvoorbereiding nodig hebben.
Taltz wordt niet aanbevolen voor gebruik bij kinderen met een lichaamsgewicht van minder dan 25 kg. Het lichaamsgewicht van kinderen moet vóór de toediening worden geregistreerd en regelmatig opnieuw worden gecontroleerd.
Voor alle indicaties (plaque psoriasis bij volwassenen en kinderen, artritis psoriatica, axiale spondyloartritis, juveniele idiopathische artritis, waaronder juveniele artritis psoriatica en aan enthesitis gerelateerde artritis) moet stoppen met de behandeling overwogen worden bij patiënten die na 16 tot 20 weken behandeling geen respons hebben laten zien. Enkele patiënten die aanvankelijk een gedeeltelijke respons vertonen, kunnen met voortgezette behandeling na 20 weken alsnog een verbetering laten zien.
Speciale patiëntengroepen
Ouderen
Er is geen dosisaanpassing nodig bij patiënten in de leeftijd van ≥ 65 jaar (zie rubriek 5.2).
Er is beperkte informatie over patiënten ≥ 75 jaar.
Nier- of leverfunctiestoornis
Taltz is in deze patiëntenpopulatie niet bestudeerd. Er kan geen aanbeveling voor de dosering worden gedaan.
Pediatrische patiënten
Pediatrische plaque psoriasis en juveniele idiopathische artritis (juveniele artritis psoriatica en aan enthesitis gerelateerde artritis (lichaamsgewicht minder dan 25 kg en jonger dan 6 jaar)
Er is bij kinderen met een lichaamsgewicht minder dan 25 kg en jonger dan 6 jaar geen relevante toepassing voor het gebruik van Taltz bij de indicatie van matige tot ernstige plaque psoriasis en juveniele idiopathische artritis, waaronder juveniele artritis psoriatica en aan enthesitis gerelateerde artritis.
Wijze van toediening
Subcutaan gebruik.
Taltz is bedoeld voor subcutane injectie. De injectieplaatsen kunnen worden afgewisseld. Indien mogelijk dienen delen van de huid die psoriasis vertonen, vermeden te worden als injectieplaatsen. De oplossing/de pen mag niet geschud worden.
Na de juiste training in de subcutane injectietechniek, kunnen patiënten Taltz zelf injecteren als de zorgverlener vaststelt dat dat kan. De arts dient echter een juiste follow-up van patiënten te organiseren. In de patiëntenbijsluiter en de gebruikershandleiding worden begrijpelijke instructies voor de toediening gegeven.
4.3 Contra-indicaties
Ernstige overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
Actieve infecties van klinische betekenis (bijv. actieve tuberculose, zie rubriek 4.4).
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De meest gemelde bijwerkingen waren reacties op de injectieplaats (15,5%) en infecties aan de bovenste luchtwegen (16,4%) (meestal nasofaryngitis).
Tabel met bijwerkingen
Bijwerkingen uit klinische studies en postmarketingrapporten (tabel 1) zijn weergegeven naar systeem/orgaanklasse volgens MedDRA. Binnen iedere systeem/orgaanklasse zijn de bijwerkingen gerangschikt op frequentie, met de meest voorkomende bijwerkingen als eerste. Binnen iedere frequentiegroep zijn de bijwerkingen vermeld in volgorde van afnemende ernst. Bovendien is voor elke bijwerking de frequentiecategorie gebaseerd op de volgende conventie: zeer vaak (≥ 1/10); vaak (≥ 1/100, < 1/10); soms (≥ 1/1.000, < 1/100); zelden (≥ 1/10.000, < 1/1.000); zeer zelden (< 1/10.000).
In totaal zijn in geblindeerde en open-label klinische studies bij plaque psoriasis, artritis psoriatica, axiale spondyloartritis en andere auto-immuunaandoeningen 8.956 patiënten behandeld met Taltz. Hiervan werden 6.385 patiënten ten minste 1 jaar blootgesteld aan Taltz, waarmee een cumulatieve blootstelling bereikt werd van in totaal 19.833 patiëntjaren bij volwassenen en 196 kinderen met een cumulatieve blootstelling van 207 patiëntjaren.
Tabel 1. Lijst met bijwerkingen in klinische studies en postmarketingrapporten
Systeem/orgaanklasse | Frequentie | Bijwerking |
Infecties en parasitaire aandoeningen | Zeer vaak | Bovenste luchtweginfectie |
Vaak | Tinea infectie, | |
Soms | Influenza, | |
Zelden | Oesofageale candidiasis | |
Bloed- en lymfestelselaandoeningen | Soms | Neutropenie, |
Immuunsysteem aandoeningen | Soms | Angio-oedeem |
Zelden | Anafylaxie | |
Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen | Vaak | Orofaryngeale pijn |
Maagdarmstelselaandoeningen | Vaak | Misselijkheid |
Soms | Inflammatoire darmziekte | |
Huid- en onderhuidaandoeningen | Soms | Urticaria, |
Zelden | Exfoliatieve dermatitis | |
Algemene aandoeningen en toedieningsplaatsstoornissen | Zeer vaak | Reacties op de injectieplaatsa |
a zie rubriek ‘Beschrijving van geselecteerde bijwerkingen’.
Beschrijving van geselecteerde bijwerkingen
Reacties op de injectieplaats
De meest waargenomen reacties op de injectieplaats waren erytheem en pijn. Deze reacties waren voor het merendeel licht tot matig van aard en leidden niet tot stoppen met Taltz.
In de studies bij plaque psoriasis bij volwassenen kwamen reacties op de injectieplaats vaker voor bij personen met een lichaamsgewicht < 60 kg, vergeleken met de groep met een lichaamsgewicht ≥ 60 kg (25% versus 14% voor de samengevoegde Q2W- en Q4W-groepen). In de studies bij artritis psoriatica kwamen reacties op de injectieplaats vaker voor bij personen met een lichaamsgewicht < 100 kg vergeleken met de groep met een lichaamsgewicht ≥ 100 kg (24% vs. 13% voor de samengevoegde Q2W en Q4W groepen). In de studies bij axiale spondyloartritis waren reacties op de injectieplaats bij personen met een lichaamsgewicht < 100 kg vergelijkbaar met de groep met een lichaamsgewicht ≥ 100 kg (14% versus 9% voor de samengevoegde Q2W- en Q4W-groepen). De toegenomen frequentie van reacties op de injectieplaats in de samengevoegde Q2W en Q4W groepen resulteerde niet in een toename in stopzettingen in de studies naar plaque psoriasis, artritis psoriatica of axiale spondyloartritis.
De hierboven beschreven resultaten zijn verkregen met de oorspronkelijke formulering van Taltz. In een enkelblinde, gerandomiseerde cross-overstudie bij 45 gezonde proefpersonen, waarin de oorspronkelijke formulering werd vergeleken met de gewijzigde, citraatvrije formulering, werden statistisch significant lagere Visual Analogue Scale (VAS)-pijnscores verkregen met de citraatvrije formulering versus de oorspronkelijke formulering tijdens injectie (verschil in LS Mean VAS-score -21,69) en 10 minuten na injectie (verschil in LS Mean VAS-score -4,47).
Infecties
In de placebogecontroleerde periode van de klinische fase III-studies naar plaque psoriasis bij volwassenen werden infecties gerapporteerd bij 27,2% van de patiënten die tot 12 weken behandeld werden met Taltz, vergeleken met 22,9% van de patiënten die behandeld werden met placebo.
De meerderheid van de infecties was niet ernstig en licht tot matig van aard, waarvan de meeste niet noodzaakten tot stoppen met de behandeling. Ernstige infecties kwamen voor bij 13 (0,6%) patiënten behandeld met Taltz en bij 3 (0,4%) patiënten behandeld met placebo (zie rubriek 4.4). Over de hele behandelperiode werden infecties gerapporteerd bij 52,8% van de patiënten behandeld met Taltz (46,9 per 100 patiëntjaren). Ernstige infecties werden gerapporteerd bij 1,6% van de patiënten behandeld met Taltz (1,5 per 100 patiëntjaren).
De waargenomen infectiepercentages in de klinische studies bij artritis psoriatica en axiale spondyloartritis waren gelijk aan de waargenomen percentages in de studies bij plaque psoriasis met uitzondering van de frequenties van de bijwerkingen influenza en conjunctivitis die vaak voorkwamen bij patiënten met artritis psoriatica.
Laboratoriumonderzoek van neutropenie en trombocytopenie
In studies bij plaque psoriasis ontwikkelde 9% van de patiënten die Taltz kregen neutropenie. In de meeste gevallen was het aantal neutrofielen in het bloed ≥ 1.000 cellen/mm3. Een dergelijk niveau van neutropenie kan voortduren, fluctueren of voorbijgaan. 0,1% van de patiënten die Taltz kregen, ontwikkelde een neutrofielenaantal in het bloed < 1.000 cellen /mm3. In het algemeen vereiste neutropenie geen stopzetten van de behandeling met Taltz. 3% van de patiënten blootgesteld aan Taltz kreeg een verandering van een normale baseline trombocytenwaarde naar < 150.000 trombocyten/mm3 tot ≥ 75.000 trombocyten/mm3. Trombocytopenie kan voortduren, fluctueren of voorbijgaan.
De frequentie neutropenie en trombocytopenie in klinische studies bij artritis psoriatica en axiale spondyloartritis is gelijk aan die waargenomen in de studies bij plaque psoriasis.
Immunogeniciteit
Ongeveer 9-17% van de volwassen patiënten met plaque psoriasis die met Taltz in de aanbevolen dosering werden behandeld, ontwikkelde antilichamen tegen het geneesmiddel; de meerderheid hiervan betrof lage titers en werd niet in verband gebracht met afgenomen klinische respons tot 60 weken behandeling. Ongeveer 1% van de patiënten behandeld met Taltz had echter bevestigde neutraliserende antilichamen geassocieerd met lage concentraties geneesmiddel en afgenomen klinische respons.
Bij patiënten met artritis psoriatica die tot 52 weken met de aanbevolen dosering Taltz werden behandeld ontwikkelde ongeveer 11% antilichamen tegen het geneesmiddel, waarvan de meerderheid een lage titer had en ongeveer 8% hadden bevestigde neutraliserende antilichamen. Er werd geen duidelijk verband waargenomen tussen de aanwezigheid van neutraliserende antilichamen en de uitwerking op de concentratie van het geneesmiddel of de werkzaamheid.
Bij pediatrische psoriasis ontwikkelden 21 patiënten (18%) die tot 12 weken werden behandeld met het aanbevolen doseringsregime Taltz antilichamen tegen het geneesmiddel. Ongeveer de helft had een lage titer en 5 patiënten (4%) hadden neutraliserende antilichamen die in verband werden gebracht met een lage concentratie van het geneesmiddel. Er was geen verband met klinische respons of bijwerkingen.
Bij radiografische axiale spondyloartritis ontwikkelde 5,2% van de patiënten die tot 16 weken werden behandeld met de aanbevolen dosering Taltz, antilichamen tegen het geneesmiddel waarvan de meerderheid een lage titer had en 1,5% (3 patiënten) neutraliserende antilichamen (NAb). De NAb-positieve monsters van deze 3 patiënten bevatten lage concentraties ixekizumab en geen van deze patiënten bereikte een ASAS40-respons. Bij niet-radiografische axiale spondyloartritis ontwikkelde 8,9% van de patiënten die tot 52 weken werden behandeld met de aanbevolen dosering Taltz, antilichamen tegen het geneesmiddel; allen hadden een lage titer, er waren geen patiënten met neutraliserende antilichamen, en er werd geen aanwijsbaar verband waargenomen tussen de aanwezigheid van antilichamen tegen het geneesmiddel en concentratie van het geneesmiddel, werkzaamheid of veiligheid.
Bij patiënten met juveniele idiopathische artritis (juveniele artritis psoriatica of aan enthesitis gerelateerde artritis) die tot 104 weken met ixekizumab werden behandeld in het aanbevolen doseringsschema, ontwikkelden 18 patiënten (22,8%) antilichamen tegen het geneesmiddel met in alle gevallen een lage tot matige titer. Er werd geen duidelijk verband waargenomen tussen de aanwezigheid van neutraliserende antilichamen en de uitwerking op de concentratie van het geneesmiddel, de werkzaamheid, of de veiligheid.
Een verband tussen immunogeniciteit en bijwerkingen voortkomend uit de behandeling werd niet duidelijk vastgesteld binnen alle indicaties.
Pediatrische populatie
Het waargenomen veiligheidsprofiel bij kinderen met plaque psoriasis die elke 4 weken met Taltz werden behandeld, is consistent met het veiligheidsprofiel bij volwassen patiënten met plaque psoriasis met uitzondering van de frequenties conjunctivitis, influenza en urticaria, die vaak voorkwamen. Inflammatoire darmziekte kwam ook vaker voor bij pediatrische patiënten alhoewel het nog steeds slechts soms voorkwam. In de pediatrische klinische studie kwam tijdens de placebogecontroleerde periode van 12 weken de ziekte van Crohn in de Taltz-groep voor bij 0,9% van de patiënten en bij 0% van de patiënten in de placebogroep. Tijdens de gecombineerde placebogecontroleerde en onderhoudsperiodes van de pediatrische klinische studie kwam de ziekte van Crohn voor bij in totaal 4 patiënten (2,0%).
In de open-label klinische studie over juveniele idiopathische artritis (juveniele artritis psoriatica of aan enthesitis gerelateerde artritis) kwamen bijwerkingen bij pediatrische patiënten, die met de aanbevolen dosis ixekizumab door middel van subcutane injectie werden behandeld, overeen met het bekende veiligheidsprofiel van ixekizumab in de geïntegreerde veiligheidsdataset voor de indicatie van pediatrische plaque psoriasis, evenals met de indicaties voor volwassenen van matige tot ernstige plaque psoriasis, artritis psoriatica, en axiale spondyloartritis met uitzondering van frequenties voor influenza (vaak), rinitis (vaak) en conjunctivitis (vaak).
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten, www.fagg.be, Afdeling Vigilantie: Website: www.eenbijwerkingmelden.be, e-mail: adr@fagg-afmps.be.
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Eli Lilly and Company (Ireland) Limited, Dunderrow, Kinsale, Co. Cork, Ierland.
8. NUMMERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/15/1085/001
EU/1/15/1085/002
EU/1/15/1085/003
10. DATUM VAN HERZIENING VAN DE TEKST 22 AUGUSTUS 2025.
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
AFLEVERINGSWIJZE Geneesmiddel op beperkt medisch voorschrift.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3510021 | TALTZ 80MG OPL INJ VOORGEVULDE PEN 1 X 1ML | L04AC13 | € 960,19 | - | Ja | € 12,8 | € 8,5 |