SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Lyumjev 100 eenheden/ml oplossing voor injectie in injectieflacon
Lyumjev 100 eenheden/ml oplossing voor injectie in patroon
Lyumjev 100 eenheden/ml KwikPen oplossing voor injectie in voorgevulde pen
Lyumjev 100 eenheden/ml Junior KwikPen oplossing voor injectie in voorgevulde pen
Lyumjev 100 eenheden/ml Tempo Pen oplossing voor injectie in voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Iedere ml bevat 100 eenheden insuline lispro* (overeenkomend met 3,5 mg).
Lyumjev 100 eenheden/ml oplossing voor injectie in injectieflacon
Iedere injectieflacon bevat 1000 eenheden insuline lispro in 10 ml oplossing.
Lyumjev 100 eenheden/ml oplossing voor injectie in patroon
Iedere patroon bevat 300 eenheden insuline lispro in 3 ml oplossing.
Lyumjev 100 eenheden/ml KwikPen oplossing voor injectie in voorgevulde pen
Lyumjev 100 eenheden/ml Tempo Pen oplossing voor injectie in voorgevulde pen
Iedere voorgevulde pen bevat 300 eenheden insuline lispro in 3 ml oplossing.
Bij een enkele injectie geeft iedere voorgevulde pen 1 – 60 eenheden af in stappen van 1 eenheid.
Lyumjev 100 eenheden/ml Junior KwikPen oplossing voor injectie in voorgevulde pen
Iedere voorgevulde pen bevat 300 eenheden insuline lispro in 3 ml oplossing.
Bij een enkele injectie geeft iedere Junior KwikPen 0,5 – 30 eenheden af in stappen van 0,5 eenheden.
*geproduceerd in E. coli met behulp van DNA-recombinatietechniek.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie.
Heldere, kleurloze, waterige oplossing.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Behandeling van diabetes mellitus bij volwassenen, adolescenten en kinderen van 1 jaar en ouder.
4.2 Dosering en wijze van toediening
Dosering
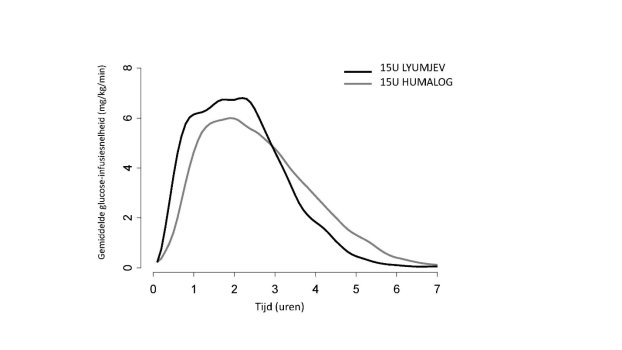
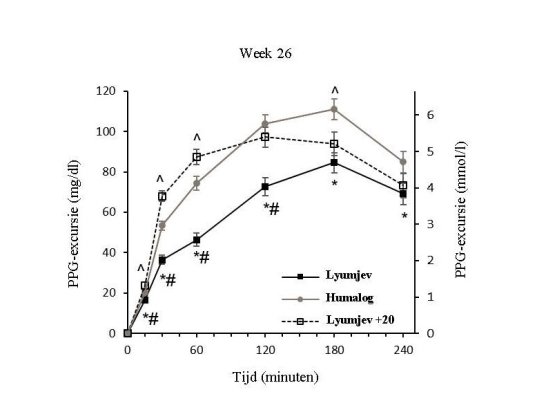
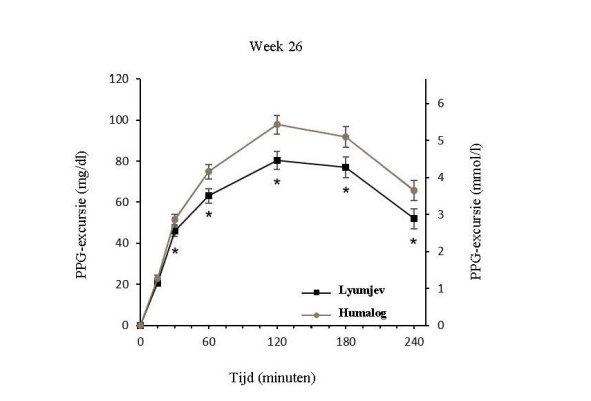
Lyumjev is een maaltijdinsuline voor subcutane injectie en dient 0 tot 2 minuten vóór het begin van de maaltijd te worden toegediend met de mogelijkheid tot toediening tot maximaal 20 minuten na het begin van de maaltijd (zie rubriek 5.1).
Lyumjev 100 eenheden/ml is geschikt voor continue subcutane insuline-infusie (CSII) en wordt gebruikt voor zowel de bolus- als basale insulinebehoefte.
Bij de aanvangsdosering dient rekening gehouden te worden met het type diabetes, gewicht van de patiënt en de bloedglucosewaarden.
De snel intredende werking moet worden overwogen wanneer Lyumjev wordt voorgeschreven (zie rubriek 5.1). Voortgezette aanpassing van de dosering van Lyumjev dient te worden gebaseerd op de metabole behoefte van de patiënt, resultaten van controles van de bloedglucose en de doelstelling betreffende glykemische controle. Om het risico op hypoglykemie of hyperglykemie te minimaliseren kunnen aanpassingen van de dosering nodig zijn bij het overschakelen van een andere insuline, bij veranderingen in lichamelijke activiteit, veranderingen in gelijktijdig gebruikte geneesmiddelen, veranderingen in maaltijdpatronen (d.w.z. hoeveelheid en type voedsel, tijdstip van voedselinname), veranderingen in de nier- of leverfunctie of gedurende acute ziekte (zie rubriek 4.4 en 4.5).
Overschakelen van een ander maaltijdinsulinegeneesmiddel
Bij het overzetten van een andere maaltijdinsuline op Lyumjev, kan de verandering op basis van eenheid-op-eenheid worden gedaan. De sterkte van insuline-analogen, inclusief Lyumjev wordt uitgedrukt in eenheden. Eén (1) eenheid Lyumjev komt overeen met 1 internationale eenheid (IE) humane insuline of andere snelwerkende insuline-analogen.
Gemiste doses
Patiënten die een maaltijddosis vergeten moeten hun bloedglucosespiegel controleren om te besluiten of een dosis insuline nodig is, en dienen hun gebruikelijke dosering bij de volgende maaltijd te vervolgen.
Speciale patiëntengroepen
Ouderen
De veiligheid en werkzaamheid van Lyumjev zijn vastgesteld bij oudere patiënten in de leeftijd van 65 tot 75 jaar. Nauwgezette controle van de glucosespiegel wordt aanbevolen en de insulinedosering dient op individuele basis te worden aangepast (zie rubriek 4.8, 5.1 en 5.2). De therapeutische ervaring bij patiënten met een leeftijd ≥ 75 jaar is beperkt.
Nierfunctiestoornis
Bij een nierfunctiestoornis kan de insulinebehoefte verminderd zijn. Bij patiënten met een nierfunctiestoornis dient het controleren van de glucosespiegel geïntensiveerd te worden en de dosering op een individuele basis te worden aangepast.
Leverfunctiestoornis
De insulinebehoefte kan verminderd zijn bij patiënten met een leverfunctiestoornis vanwege een verminderde capaciteit voor de gluconeogenese en een verminderde insulineafbraak. Bij patiënten met een leverfunctiestoornis dient het controleren van de glucosespiegel geïntensiveerd te worden en de dosering op een individuele basis te worden aangepast.
Pediatrische patiënten
Lyumjev kan worden gebruikt bij adolescenten en kinderen van 1 jaar en ouder (zie rubriek 5.1). Er is geen klinische ervaring met het gebruik van Lyumjev bij kinderen jonger dan 3 jaar. Net als bij volwassenen moet de dosering individueel worden aangepast. Het wordt aanbevolen om Lyumjev nul tot twee minuten voor het begin van de maaltijd toe te dienen, met de mogelijkheid om tot 20 minuten na het begin van de maaltijd toe te dienen indien nodig.
Wijze van toediening
Vóór het starten met Lyumjev moeten patiënten worden getraind in het juiste gebruik en de juiste injectietechniek. Patiënten moet worden verteld om:
- voor toediening altijd het insuline-etiket te controleren.
- Lyumjev voor gebruik visueel te controleren en bij aanwezigheid van vaste deeltjes of verkleuring het middel af te voeren.
- de injectie- of infusieplaatsen dienen altijd te worden afgewisseld binnen eenzelfde gebied om het risico op lipodystrofie en cutane amyloïdose te beperken (zie rubriek 4.4 en 4.8)
- Een reservehulpmiddel bij zich te hebben voor het geval dat een toedieningssysteem kapotgaat.
Subcutane injectie
Lyumjev moet subcutaan in de buik, bovenarm, dij of billen worden geïnjecteerd (zie rubriek 5.2)
Lyumjev dient in het algemeen te worden gebruikt in combinatie met een middellang- of langwerkende insuline. Er moet een andere injectieplaats worden gekozen als tegelijkertijd een andere insuline wordt geïnjecteerd.
Bij het injecteren moet worden voorkomen dat er een bloedvat wordt aangeprikt.
Hulpmiddelen moeten worden weggegooid als een onderdeel kapot is of er beschadigd uitziet.
De naald moet na iedere injectie worden afgevoerd.
Lyumjev injectieflacons
Als subcutane toediening met behulp van een injectiespuit noodzakelijk is, moet een injectieflacon worden gebruikt.
De injectiespuit moet zijn voorzien van markeringen van 100 eenheden/ml.
Patiënten die injectieflacons gebruiken mogen hun naalden of injectiespuiten niet delen.
Lyumjev patronen
Lyumjev in patronen is alleen geschikt voor subcutane injecties met behulp van een voor hergebruik geschikte pen van Lilly.
Lyumjev patronen dienen niet te worden gebruikt met een andere voor hergebruik geschikte pen aangezien de nauwkeurigheid van de dosis met andere pennen niet is vastgesteld.
Voor elke afzonderlijke pen geldt dat de instructies met betrekking tot het plaatsen van de patroon, het aanbrengen van het naaldje en het toedienen van de insuline-injectie moeten worden gevolgd.
Om de mogelijke overdracht van ziekte te voorkomen, dient elke patroon door slechts één patiënt te worden gebruikt, zelfs als de naald op het toedieningssysteem is vervangen.
Lyumjev KwikPennen en Lyumjev Tempo Pen
De KwikPen, Junior KwikPen en Tempo Pen zijn alleen geschikt voor subcutane injecties.
Lyumjev KwikPennen zijn beschikbaar in twee concentraties: Lyumjev 100 eenheden/ml KwikPen en Lyumjev 200 eenheden/ml KwikPen. Zie de afzonderlijke SmPC voor Lyumjev 200 eenheden/ml KwikPen.
De KwikPen geeft 1 – 60 eenheden af in stappen van 1 eenheid in een enkele injectie.
De Lyumjev 100 eenheden/ml Junior KwikPen geeft 0,5 – 30 eenheden af in stappen van 0,5 eenheden in een enkele injectie.
De Lyumjev 100 eenheden/ml Tempo Pen geeft 1 – 60 eenheden af in stappen van 1 eenheid in een enkele injectie.
Het aantal eenheden insuline wordt getoond in het doseervenster van de pen, onafhankelijk van de sterkte en er dient geen dosisomzetting plaats te vinden bij het overzetten van een patiënt op een nieuwe concentratie of op een pen met een andere dosisstap.
Lyumjev 100 eenheden/ml Junior KwikPen is geschikt voor patiënten die profijt kunnen hebben van nauwkeurigere aanpassingen van de dosis insuline.
De Tempo Pen kan worden gebruikt met de Tempo Smart Button, een optionele module voor gegevensoverdracht (zie rubriek 6.6). Patiënten moeten, als zij de Tempo Pen, de Tempo Smart Button en de mobiele applicatie gebruiken, worden geïnstrueerd om, als zij onzeker zijn hoeveel zij hebben geïnjecteerd, hun bloedsuikerspiegels te controleren als zij nog een injectie overwegen of hiertoe een besluit nemen, net zoals bij elke insuline-injectie.
Voor gedetailleerde gebruiksinstructies wordt verwezen naar de instructies die met de bijsluiter geleverd worden.
Om de mogelijke overdracht van ziekte te voorkomen, dient elke pen door slechts één patiënt te worden gebruikt, zelfs als de naald is vervangen.
CSII (Insulinepomp)
Gebruik een pomp die geschikt is voor infusie van insuline. Gebruik een injectieflacon Lyumjev 100 eenheden/ml om het pompreservoir te vullen.
Patiënten die een pomp gebruiken dienen de instructies te volgen die geleverd zijn bij de pomp en de infusieset. Gebruik het juiste reservoir en de juiste katheter voor de pomp.
Bij het vullen van het pompreservoir moet de juiste naaldlengte op het vulsysteem worden gebruikt om beschadiging van te pomp te voorkomen. De infusieset (slang en canule) moet worden vervangen conform de instructies die zijn vermeld in de productinformatie die bij de infusieset wordt geleverd.
Een pompdefect of een obstructie in de infusieset kan resulteren in een snelle stijging van glucosespiegels (zie rubriek 4.4).
Intraveneus gebruik
Lyumjev 100 eenheden/ml is beschikbaar in injectieflacons als toediening van een intraveneuze injectie noodzakelijk is. Dit geneesmiddel mag niet worden gemengd met een andere insuline of enig ander geneesmiddel met uitzondering van de geneesmiddelen genoemd in rubriek 6.6.
Zie rubriek 6.6 voor instructies voor verdunning van het geneesmiddel vóór toediening.
Intraveneuze toediening van Lyumjev 100 eenheden/ml moet onder medisch toezicht uitgevoerd worden.
4.3 Contra-indicaties
Hypoglykemie.
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
Hypoglykemie (zeer vaak) en infusieplaatsreacties bij patiënten die gebruik maken van het CSII-systeem (zeer vaak) zijn de meest frequent gemelde bijwerkingen tijdens de behandeling (zie rubriek 4.2, 4.4 en 4.9).
De volgende bijwerkingen gerelateerd aan klinische onderzoeken zijn hieronder vermeld als MedDRA-voorkeursterm volgens systeem/orgaanklasse en in volgorde van afnemende incidentie (zeer vaak: ≥ 1/10; vaak: ≥ 1/100, < 1/10; soms: ≥ 1/1.000, < 1/100; zelden: ≥ 1/10.000, < 1/1.000; zeer zelden: < 1/10.000) en niet bekend (kan niet worden bepaald met de beschikbare gegevens). Binnen elke frequentiegroep worden de bijwerkingen gerangschikt naar afnemende ernst.
Tabel 1. Bijwerkingen
MedDRA systeem/orgaanklasse | Zeer vaak | Vaak | Soms | Niet bekend |
Voedings- en stofwisselingstoornissen | Hypoglykemie |
|
|
|
|
|
|
|
|
| ||||
| ||||
Algemene aandoeningen en toedieningsplaatsstoornissen | Infusieplaats-reactiesa | Allergische reactiesb | Oedema |
|
| Reacties op de injectieplaatsc |
|
| |
|
|
| ||
Huid- en onderhuidaandoeningen |
|
| Lipodystrofie | Cutane amyloïdose |
Huiduitslag | ||||
Pruritus |
a Gemeld in PRONTO-Pump-2
b Zie rubriek 4.8 Beschrijving van geselecteerde bijwerkingen
c Gemeld in PRONTO-T1D, PRONTO-T2D en PRONTO-Peds
Beschrijving van geselecteerde bijwerkingen
Hypoglykemie
Hypoglykemie is de vaakst waargenomen bijwerking bij patiënten die insuline gebruiken. De incidentie van ernstige hypoglykemie in de 26 weken durende klinische fase 3-studies bij volwassenen was 5,5% bij patiënten met diabetes mellitus type 1 en 0,9% bij patiënten met diabetes mellitus type 2 (zie tabel 2 en 3). Ernstige hypoglykemie werd bij 0,7% van de met Lyumjev behandelde pediatrische patiënten gemeld in de studie PRONTO-Peds.
De verschijnselen van hypoglykemie, zoals lusteloosheid, verwarring, hartkloppingen, zweten, braken en hoofdpijn komen gewoonlijk plotseling op.
In alle onderzoeken waren er bij toediening van Lyumjev of de comparator (een ander geneesmiddel dat insuline lispro bevat) geen klinisch relevante verschillen in de frequentie van hypoglykemie. In de onderzoeken waarin Lyumjev en de comparator werden toegediend op verschillende tijdstippen in relatie tot de maaltijd, waren er geen klinisch relevante verschillen in de frequentie van hypoglykemie.
Als gevolg van de snellere intrede van werking kan hypoglykemie na een injectie/infusie met Lyumjev eerder optreden in vergelijking met andere maaltijdinsulines.
Allergische reacties
Ernstige, levensbedreigende, gegeneraliseerde allergie inclusief anafylaxie, gegeneraliseerde huidreacties, angio-oedeem, bronchospasmen, hypotensie en shock kunnen optreden met alle insulines waaronder Lyumjev.
Reacties op de injectie/infuusplaats
Zoals bij andere insulinetherapieën kunnen patiënten huiduitslag, roodheid, ontsteking, pijn, blauwe plekken of jeuk ervaren op de plaats van toediening van de injectie of infusie met Lyumjev.
In studies PRONTO-T1D en PRONTO-T2D (toediening van meerdere doses per injectie [MDI]), traden reacties op de injectieplaats op bij 2,7% van de met Lyumjev behandelde volwassen patiënten. Deze reacties waren gewoonlijk mild en verdwenen meestal bij voortgezette behandeling. Van de 1.116 patiënten die Lyumjev kregen, stopte 1 patiënt met de behandeling vanwege reacties op de injectieplaats (< 0,1%).
In de studie PRONTO-Peds traden reacties op de injectieplaats op bij 6,2% van de met Lyumjev behandelde pediatrische patiënten. Deze voorvallen waren mild of matig. Van de 418 patiënten die met Lyumjev werden behandeld, stopten er 2 met de behandeling vanwege reacties op de injectieplaats (< 0,5%).
In studie PRONTO-Pump-2 werden reacties op de infuusplaats gemeld bij 38% van de met Lyumjev behandelde patiënten. De meerderheid van deze voorvallen was mild. Van de 215 patiënten die met Lyumjev werden behandeld, stopten 7 patiënten met de behandeling vanwege reacties op de infuusplaats (3,3%).
Immunogeniciteit
De toediening van insuline kan de aanmaak van insuline-antistoffen veroorzaken. De aanwezigheid van antistoffen tegen het geneesmiddel had geen klinisch relevant effect op de farmacokinetiek, werkzaamheid of veiligheid van Lyumjev.
Huid- en onderhuidaandoeningen
Lipodystrofie en cutane amyloïdose kunnen optreden op de injectieplaats en kunnen de plaatselijke insuline-absorptie vertragen. Het continue afwisselen van de injectieplaats binnen eenzelfde gebied kan helpen deze reacties te verminderen of te voorkomen (zie rubriek 4.4)
Oedeem
Er zijn met insulinetherapie gevallen van oedeem gemeld, in het bijzonder als voorafgaande slechte metabole controle verbeterd is door intensieve insulinetherapie.
Pediatrische patiënten
De veiligheid en werkzaamheid zijn onderzocht in een studie ter bevestiging van de therapeutische werkzaamheid bij kinderen met diabetes type 1 in de leeftijd van 3 tot < 18 jaar. In de studie werden 418 patiënten behandeld met Lyumjev. De frequentie, het type en de ernst van bijwerkingen die bij pediatrische patiënten zijn waargenomen, komen overeen met het veiligheidsprofiel bij volwassen patiënten.
Andere speciale patiëntengroepen
Gebaseerd op resultaten uit klinische onderzoeken met insuline lispro wijzen de frequentie, type en ernst van bijwerkingen waargenomen bij oudere patiënten en bij patiënten met een nier-of leverfunctiestoornis in het algemeen niet op enig verschil met de bredere ervaring onder de algemene populatie. De veiligheidsinformatie bij zeer oude patiënten (≥ 75 jaar) of patiënten met een matige tot ernstige nierfunctiestoornis of leverfunctiestoornis is beperkt (zie rubriek 5.1).
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten, www.fagg.be, Afdeling Vigilantie: Website: www.eenbijwerkingmelden.be, e-mail: adr@fagg-afmps.be.
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Eli Lilly Nederland B.V.
Papendorpseweg 83
3528 BJ Utrecht
Nederland
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/20/1422/001
EU/1/20/1422/002
EU/1/20/1422/003
EU/1/20/1422/004
EU/1/20/1422/005
EU/1/20/1422/006
EU/1/20/1422/007
EU/1/20/1422/008
EU/1/20/1422/009
EU/1/20/1422/010
EU/1/20/1422/011
EU/1/20/1422/012
EU/1/20/1422/016
EU/1/20/1422/017
10. DATUM VAN HERZIENING VAN DE TEKST: 13 JANUARI 2025.
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu
AFLEVERINGSWIJZE Geneesmiddel op medisch voorschrift.
1
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 4202701 | LYUMJEV 100IE/ML KWIKPEN OPL INJ VOORGEV.PEN 5X3ML | A10AB04 | € 43,57 | - | Ja | € 2 | € 1 |