SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
ZOLADEX, 3,6 mg, implantaat
ZOLADEX Long Acting, 10,8 mg, implantaat
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
ZOLADEX bevat goserelineacetaat overeenkomend met 3,6 mg peptide base.
ZOLADEX Long Acting bevat goserelineacetaat overeenkomend met 10,8 mg peptide base.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Implantaat.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
ZOLADEX
1) Palliatieve hormonale behandeling van gevorderde prostaatkanker (stadia III en IV).
2) Reductie van de tumorgrootte met het oog op een curatieve totale prostato-vesiculectomie (stadia T2N1-2M0 en T3N0-2M0 of B2-C).
3) Behandeling van gevorderde borstkanker en als alternatief van een adjuvante chemotherapie bij vroegtijdige borstkanker bij pre- en perimenopauzale vrouwen geschikt voor hormonale behandeling. Het voordeel van castratie, geïnduceerd door een LHRH‑analoog tijdens of na chemotherapie, werd nog niet aangetoond.
4) Behandeling van endometriose. ZOLADEX vermindert de symptomen, pijn inbegrepen. ZOLADEX reduceert het aantal en de afmetingen van de endometriosehaarden. De behandelingsduur is maximaal 6 maanden.
5) Behandeling van uterusfibromen. ZOLADEX doet de gezwellen afnemen in grootte, laat toe de anemische toestand te verbeteren en vermindert de symptomen, pijn inbegrepen. ZOLADEX kan toegediend worden in de periode voorafgaand aan een chirurgische ingreep; in dergelijk geval kan ZOLADEX de chirurgische techniek vereenvoudigen en het operatief bloedverlies verminderen. De behandelingsduur is maximaal 3 maanden.
6) Reductie van het endometrium: ZOLADEX reduceert het endometrium, ter voorbereiding van een endometriumablatie, wat de doeltreffendheid van de endometriumresectie zou verhogen en het endoscopisch onderzoek vergemakkelijken. Niettemin kan de behandeling de weerstand tegen dilatatie van de cervix verhogen. Voorzichtigheid is dus geboden bij dilatatie van de cervix.
ZOLADEX Long Acting
1) Palliatieve hormonale behandeling van gevorderde prostaatkanker (stadia III en IV).
2) Reductie van de tumorgrootte met het oog op een curatieve totale prostato-vesiculectomie (stadia T2N1-2M0 en T3N0-2M0 of B2-C).
3) Behandeling van endometriose. ZOLADEX Long Acting vermindert de symptomen, pijn inbegrepen. ZOLADEX Long Acting reduceert het aantal en de afmetingen van de endometriosehaarden.
4) Behandeling van uterusfibromen. ZOLADEX Long Acting doet de gezwellen afnemen in grootte, laat toe de hematologische status te verbeteren en vermindert de symptomen zoals pijn. ZOLADEX Long Acting kan toegediend worden in de periode voorafgaand aan een chirurgische ingreep; in dergelijk geval kan het de chirurgische techniek vergemakkelijken en het operatief bloedverlies reduceren.
4.2 Dosering en wijze van toediening
Wees voorzichtig bij het inbrengen van ZOLADEX/ZOLADEX Long Acting in de voorste buikwand vanwege de nabijheid van de onderliggende inferieure epigastrische slagader en vertakkingen daarvan.
Wees extra voorzichtig bij het toedienen van ZOLADEX/ZOLADEX Long Acting aan patiënten met een laag BMI en/of patiënten die volledige anticoagulatietherapie krijgen (zie rubriek 4.4).
De instructies voor het correct toedienen van ZOLADEX/ZOLADEX Long Acting staan vermeld op de enveloppe en op het einde van deze SKP.
Enkel gebruiken wanneer de verpakking onbeschadigd is. Onmiddellijk na openen van de verpakking toedienen.
- Bij patiënten met nierinsufficiëntie of leverinsufficiëntie is er geen dosisaanpassing nodig.
- Pediatrische patiënten
Het gebruik van ZOLADEX of ZOLADEX Long Acting bij kinderen is niet geïndiceerd.
- Het gebruik van een lokaal anestheticum is toegelaten maar in de meeste gevallen niet vereist.
ZOLADEX (mannen en vrouwen)
Volwassenen (inclusief bejaarden)
- Eén subcutane injectie van een ZOLADEX implantaat om de 28 dagen in de abdominale voorwand.
Endometriose:
Endometriose mag slechts gedurende een periode van zes maanden worden behandeld, aangezien er momenteel geen klinische gegevens beschikbaar zijn voor langere behandelingsperiodes. Herhalingsbehandelingen mogen niet gegeven worden, gezien de bezorgdheid betreffende het verlies van minerale botdensiteit. Bij patiënten die gosereline toegediend kregen voor de behandeling van endometriose, werd aangetoond dat toevoeging van hormonale substitutietherapie (dagelijks een oestrogeen en een progestageen) het verlies van minerale botdensiteit en de vasomotorische symptomen beperkt.
Slinken van het endometrium:
- Voor de indicatie endometriumreductie dienen twee ZOLADEX implantaten toegediend te worden met een tussenperiode van 28 dagen. De chirurgische ingreep dient plaats te vinden binnen de twee weken na toedienen van het tweede ZOLADEX implantaat.
- Behandeling van vier of acht weken. Een tweede implantaat kan nodig zijn voor patiënten met een grote uterus of om meer flexibiliteit te creëren in de timing van de ingreep.
Fibromen van de uterus:
Voor vrouwen met anemie door fibromen van de uterus: het ZOLADEX implantaat met een ijzersupplement mag tot drie maanden voor chirurgie worden toegediend.
ZOLADEX Long Acting
Volwassen mannen (inclusief bejaarden)
Eén subcutane injectie van een ZOLADEX Long Acting implantaat om de 3 maand in de abdominale voorwand.
Volwassen vrouwen (inclusief bejaarden)
Eén subcutane injectie van een ZOLADEX Long Acting implantaat om de 12 weken in de abdominale voorwand.
4.3 Contra-indicaties
- Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
- Zwangerschap en borstvoeding (zie rubriek 4.6 Vruchtbaarheid, zwangerschap en borstvoeding).
4.8 Bijwerkingen
De volgende frequentiegroepen zijn gebaseerd op alle bijwerkingen voorkomende uit klinische studies, studies na het op de markt brengen en spontane rapporteringen. De meest frequent waargenomen bijwerkingen omvatten: warmteopwellingen, zweten en reacties ter hoogte van de injectieplaats.
De volgende overeenkomst is gebruikt voor de frequentie-indeling: zeer vaak (≥1/10), vaak (≥1/100 tot <1/10), soms (≥1/1.000 tot <1/100), zelden (≥1/10.000 tot <1/1.000) en zeer zelden (<1/10.000), niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Tabel: ZOLADEX en ZOLADEX Long Acting bijwerkingen volgens MedDRA Systeem/orgaanklasse
Systeem/orgaanklasse | Frequentie | Mannen | Vrouwen |
Neoplasmata, benigne, maligne en niet-gespecificeerde (inclusief cysten en poliepen) | Zeer zelden | Hypofysetumor | Hypofysetumor |
Niet bekend | N/A | Degeneratie van uterusfibromen bij vrouwen met uterusfibromen | |
Immuunsysteemaandoeningen | Soms | Overgevoeligheid aan het geneesmiddel | Overgevoeligheid aan het geneesmiddel |
Zelden | Anafylactische reactie | Anafylactische reactie | |
Endocriene aandoeningen | Zeer zelden | Hypofyse-hemorragie | Hypofyse-hemorragie |
Voedings- en stofwisselingsstoornissen | Vaak | Verminderde glucosetolerantie a | N/A |
| Soms | N/A | Hypercalciëmie (alleen ZOLADEX) |
Psychische stoornissen | Zeer vaak | Verminderd libido b | Verminderd libido b |
Vaak | Stemmingswijzigingen, depressie | Stemmingswijzigingen, depressie | |
Zeer zelden | Psychotische stoornissen | Psychotische stoornissen | |
Hartaandoeningen | Vaak | Hartinsufficiëntie f | N/A |
Niet bekend | QT‑verlenging (zie rubrieken 4.4 en 4.5) | QT‑verlenging (zie rubrieken 4.4 en 4.5 | |
Zenuwstelselaandoeningen | Vaak | Paresthesie | Paresthesie |
Ruggenmergcompressie | N/A | ||
N/A | Hoofdpijn | ||
Insomnia | Insomnia | ||
Bloedvataandoeningen | Zeer vaak | Warmteopwellingen b | Warmteopwellingen b |
Vaak | Abnormale bloeddruk c | Abnormale bloeddruk c | |
Huid- en onderhuidaandoeningen | Zeer vaak | Hyperhydrosis b | Hyperhydrosis b, acne i |
Vaak | Rash d | Rash d, alopecia g | |
Niet bekend | Alopecia h | (zie vaak) | |
Skeletspierstelsel- en bindweefselaandoeningen | Vaak | Botpijn e | N/A |
(zie soms) | Artralgie | ||
Soms | Artralgie | (zie vaak) | |
Nier- en urinewegaandoeningen | Soms | Ureterobstructie | N/A |
Voortplantingsstelsel- en | Zeer vaak | Erectiele dysfunctie | N/A |
N/A | Vulvovaginale droogte | ||
N/A | Vergroting van de borst | ||
Vaak | Gynaecomastie | N/A | |
Soms | Pijnlijke borsten | N/A | |
Zelden | N/A | Ovariumcyste | |
Niet bekend | N/A | Dervingbloeding (zie rubriek 4.4) | |
Algemene aandoeningen en toedieningsplaatsstoornissen | Zeer vaak | (zie vaak) | Reacties ter hoogte van de toedieningsplaats |
Vaak | Reacties ter hoogte van de toedieningsplaats | (zie zeer vaak) | |
N/A | Toename van het tumorvolume (tumor flare), pijnlijke tumor | ||
Onderzoeken | Vaak | Verminderde botdensiteit (zie rubriek 4.4), gewichtstoename | Verminderde botdensiteit (zie rubriek 4.4), gewichtstoename |
a Er werd een verminderde glucosetolerantie waargenomen bij mannen die LHRH‑agonisten kregen. Dit kan zich uiten als diabetes of verminderde glykemiecontrole bij patiënten met reeds bestaande diabetes mellitus.
b Dit zijn farmacologische effecten waarvoor de behandeling zelden moet gestopt worden. Hyperhydrosis en warmteopwellingen kunnen blijven voorkomen na het stoppen van ZOLADEX.
c Deze kunnen zich uiten als hypotensie of hypertensie en werden af en toe waargenomen bij patiënten die gosereline kregen. Deze wijzigingen zijn meestal tijdelijk en verdwijnen tijdens voortgezette behandeling of na stopzetting van de behandeling met gosereline. Zelden was medische tussenkomst vereist voor dergelijke wijzigingen, waaronder stopzetting van de behandeling met gosereline.
d Deze zijn doorgaans licht en nemen vaak af zonder stopzetting van de behandeling.
e Eerst kunnen prostaatkankerpatiënten tijdelijk meer botpijn hebben. Dit kan symptomatisch behandeld worden.
f Geobserveerd tijdens een farmaco-epidemiologische studie met LHRH-agonisten gebruikt bij de behandeling van prostaatkanker. Het risico blijkt toe te nemen wanneer gebruikt in combinatie met anti-androgenen.
g Verlies van hoofdhaar is gemeld bij vrouwen, inclusief jongere patiënten die behandeld worden voor goedaardige aandoeningen. Dit is meestal licht maar kan soms ernstig zijn.
h In het bijzonder verlies van lichaamshaar, een verwacht effect van verlaagde androgene niveaus.
i In de meeste gevallen, werd acne gemeld binnen een maand na het begin van ZOLADEX.
N/A:Niet van toepassing
Postmarketing ervaring
Er zijn een klein aantal meldingen van gevallen van gewijzigd aantal bloedcellen, leverdysfunctie, longembool en interstitiële pneumonie in verband met gosereline.
Zelden menopauseren vrouwen tijdens behandeling met LHRH‑analogen en menstrueren ze niet opnieuw na het stoppen van de behandeling. Het is niet bekend of dit een effect is van de behandeling met gosereline of een weerspiegeling van hun gynaecologische toestand.
ZOLADEX
Daarnaast werden de volgende bijwerkingen gemeld bij vrouwen die behandeld werden voor goedaardige, gynaecologische indicaties:
acne, gewijzigde lichaamsbeharing, droge huid, gewichtstoename, gestegen serumcholesterol, ovariumoverstimuleringssyndroom (bij gelijktijdig gebruik van gonadotrofines), vaginitis, vaginale afscheiding, nervositas, slaapstoornissen, moeheid, perifeer oedeem, myalgie, kuitkrampen, nausea, braken, diarree, constipatie, buikklachten, stemwijzigingen.
Borstkankerpatiënten kunnen eerst een tijdelijke toename van de tekenen en symptomen hebben. Dit kan symptomatisch behandeld worden.
Zelden ontstond bij het aanvatten van de behandeling hypercalciëmie bij patiënten met gemetastaseerde borstkanker. Indien zich symptomen voordoen die op hypercalciëmie kunnen wijzen (bijv. dorst.), moet hypercalciëmie uitgesloten worden.
ZOLADEX Long Acting
Er is een klein aantal gevallen van hypercalciëmie gerapporteerd bij vrouwen die werden behandeld voor endometriose en/of fibromen. Indien zich symptomen voordoen die op hypercalciëmie kunnen wijzen (bijv. dorst.), moet hypercalciëmie uitgesloten worden.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem – zie onderstaande details.
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
AstraZeneca nv/sa
Alfons Gossetlaan 40 bus 201
1702 Groot-Bijgaarden
België
Tel. +32 (0)2/370 48 11
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
ZOLADEX: BE138731
ZOLADEX Long Acting: BE179277
10. DATUM VAN HERZIENING VAN DE TEKST
11-2024
De volgende informatie is alleen bestemd voor artsen of andere beroepsbeoefenaren in de gezondheidszorg
ZOLADEX/ZOLADEX Long Acting wordt toegediend door subcutane injectie – Gelieve voor toediening alle instructies te lezen en ervoor te zorgen dat u deze volledig begrepen heeft
1. Leg de patiënt in een comfortabele positie, met het bovenlichaam iets omhoog.
Bereid de injectieplaats voor in overeenstemming met de plaatselijke richtlijnen en procedures.
OPMERKING: Wees voorzichtig bij het inbrengen van ZOLADEX/ZOLADEX Long Acting in de voorste buikwand omwille van de nabijheid van de inferieure epigastrische slagader en vertakkingen daarvan; zeer magere patiënten lopen een groter risico op vasculaire letsels.
2. Controleer of de enveloppe en spuit niet beschadigd zijn. Haal de injectiespuit uit de geopende enveloppe en houd de spuit lichtjes schuin naar het licht. Controleer of ten minste een gedeelte van het ZOLADEX/ZOLADEX Long Acting implantaat zichtbaar is (Figuur 1).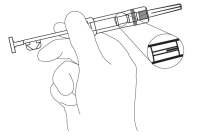 Figuur 1
Figuur 1
3. Neem de plastieken veiligheidsklem vast, trek deze van de spuit weg en gooi ze weg (Figuur 2).
Verwijder de naaldbeschermer. In tegenstelling tot vloeibare injectiepreparaten is het niet nodig om luchtbellen te verwijderen, gezien pogingen hiertoe het ZOLADEX/ZOLADEX Long Acting implantaat kunnen verplaatsen.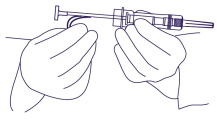 Figuur 2
Figuur 2
4. Houd de injectiespuit vast bij de beschermhuls. Gebruik hiervoor een aseptische techniek. Knijp de huid van de patiënt samen in een plooi en breng de naald in onder een lichte hoek (30 tot 45 graden) met de huid. Houd de opening van de naald naar boven gericht. Breng de naald in in het subcutane weefsel van de voorste buikwand onder de navellijn tot de beschermhuls de huid van de patiënt raakt. (Figuur 3).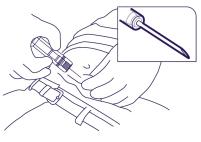 Figuur 3
Figuur 3
OPMERKING: De ZOLADEX/ZOLADEX Long Acting injectiespuit kan niet worden gebruikt voor aspiratie. Als de hypodermische naald een groot bloedvat raakt, zal er onmiddellijk bloed zichtbaar zijn in het venster van de spuit. Indien een bloedvat werd geraakt, verwijder de naald dan en stelp onmiddellijk elke verdere bloeding, terwijl u de patiënt opvolgt voor tekenen of symptomen van een abdominale bloeding. Nadat zeker is gesteld dat de patiënt hemodynamisch stabiel is, kan een ander ZOLADEX/ZOLADEX Long Acting-implantaat op een andere plek worden geïnjecteerd met een nieuwe injectiespuit. Wees extra voorzichtig bij het toedienen van ZOLADEX/ZOLADEX Long Acting aan patiënten met een lage BMI en/of patiënten die volledige anticoagulatietherapie krijgen.
5. Niet injecteren in spierweefsel of door het buikvlies. Foutieve manier van vastnemen en toedieningshoek wordt getoond in Figuur 4.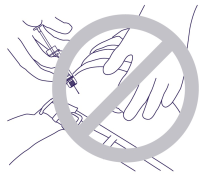 Figuur 4
Figuur 4
6. Druk de zuiger volledig in tot u niet verder kunt, om het ZOLADEX/ZOLADEX Long Acting implantaat af te geven en de beschermhuls te activeren. U kunt een ‘klik’ horen en u zal voelen dat de beschermhuls automatisch vooruit schuift om de naald te bedekken. Indien de zuiger niet volledig is ingedrukt zal de beschermhuls NIET geactiveerd worden.
OPMERKING: De naald trekt zich niet terug.
7. Houd de spuit zoals aangegeven in Figuur 5 en trek de naald terug zodat de beschermhuls verder over de naald kan schuiven. Gooi de spuit weg in een geschikte container voor scherpe voorwerpen.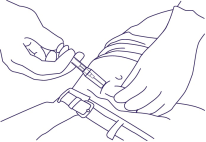 Figuur 5
Figuur 5
OPMERKING: In het onwaarschijnlijke geval dat het nodig zou zijn om chirurgisch een ZOLADEX/ZOLADEX Long Acting-implantaat te verwijderen, kan het staafje met ultrasound geluid worden gelokaliseerd.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 0603159 | ZOLADEX SER INJ SC 1X3,6MG | L02AE03 | € 122,11 | - | Ja | € 2 | € 1 |
| 1278480 | ZOLADEX LONG ACTION SER 1X10,8 MG | L02AE03 | € 297,11 | - | Ja | € 2 | € 1 |