1. NAAM VAN HET GENEESMIDDEL
Fiasp 100 eenheden/ml FlexTouch oplossing voor injectie in een voorgevulde pen
Fiasp 100 eenheden/ml Penfill oplossing voor injectie in een patroon
Fiasp 100 eenheden/ml oplossing voor injectie in een injectieflacon
Fiasp 100 eenheden/ml PumpCart oplossing voor injectie in een patroon
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
1 ml van de oplossing bevat 100 eenheden insuline aspart* (equivalent aan 3,5 mg).
Fiasp 100 eenheden/ml FlexTouch oplossing voor injectie in een voorgevulde pen
Elke voorgevulde pen bevat 300 eenheden insuline aspart in 3 ml oplossing.
Fiasp 100 eenheden/ml Penfill oplossing voor injectie in een patroon
Elke patroon bevat 300 eenheden insuline aspart in 3 ml oplossing.
Fiasp 100 eenheden/ml oplossing voor injectie in een injectieflacon
Elke injectieflacon bevat 1.000 eenheden insuline aspart in 10 ml oplossing.
Fiasp 100 eenheden/ml PumpCart oplossing voor injectie in een patroon
Elke patroon bevat 160 eenheden insuline aspart in 1,6 ml oplossing.
*Insuline aspart wordt geproduceerd in Saccharomyces cerevisiae met behulp van recombinant-DNA-technologie.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Fiasp 100 eenheden/ml FlexTouch oplossing voor injectie in een voorgevulde pen
Oplossing voor injectie (FlexTouch).
Fiasp 100 eenheden/ml Penfill oplossing voor injectie in een patroon
Oplossing voor injectie (Penfill).
Fiasp 100 eenheden/ml oplossing voor injectie in een injectieflacon
Oplossing voor injectie.
Fiasp 100 eenheden/ml PumpCart oplossing voor injectie in een patroon
Oplossing voor injectie (PumpCart).
Heldere, kleurloze, waterige oplossing.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Behandeling van diabetes mellitus bij volwassenen, adolescenten en kinderen van 1 jaar en ouder.
4.2 Dosering en wijze van toediening
Dosering
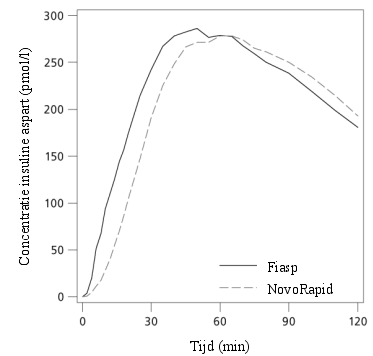
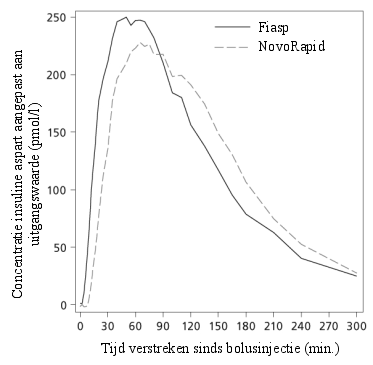
Fiasp is een maaltijdinsuline voor subcutane toediening. Fiasp moet 0 tot 2 minuten voor het begin van de maaltijd worden toegediend, met de mogelijkheid tot toediening tot maximaal 20 minuten na het begin van de maaltijd (zie rubriek 5.1).
De dosering van Fiasp is per persoon verschillend en wordt bepaald in overeenstemming met de behoeften van de patiënt. Fiasp gegeven als subcutane injectie moet worden gecombineerd met ten minste eenmaal daags toegediende middellang- of langwerkende insuline. In een behandeling met een basaalbolusregime kan Fiasp voorzien in ongeveer 50% van de behoefte en kan in de rest worden voorzien door middellang of langwerkende insuline.
De individuele totale dagelijkse insulinebehoefte bij volwassenen, adolescenten en kinderen kan variëren en ligt gewoonlijk tussen 0,5 en 1 eenheid/kg/dag.
Bloedglucosecontrole en dosisaanpassing van de insuline worden aanbevolen om optimale glykemische controle te bereiken.
Aanpassing van de dosis kan noodzakelijk zijn wanneer patiënten zich fysiek meer inspannen, hun gebruikelijke dieet wijzigen of in geval van een bijkomende ziekte. Onder deze omstandigheden dient de bloedglucosespiegel adequaat te worden gecontroleerd.
De werkingsduur zal variëren naar gelang de dosis, injectieplaats, bloedcirculatie, temperatuur en mate van fysieke inspanning.
Patiënten op een basaalbolusregime die een maaltijddosis vergeten, wordt geadviseerd hun bloedglucosespiegel te controleren om te beslissen of een insulinedosis nodig is. Bij de volgende maaltijd dienen patiënten hun gebruikelijke doseerschema te vervolgen.
De sterkte van insuline-analogen, waaronder Fiasp, wordt uitgedrukt in eenheden. Een (1) eenheid Fiasp komt overeen met 1 internationale eenheid humane insuline of 1 eenheid van andere snelwerkende insuline-analogen.
De snel intredende werking moet worden overwogen wanneer Fiasp wordt voorgeschreven (zie rubriek 5.1).
Starten
Patiënten met diabetes mellitus type 1
De aanbevolen startdosis bij insuline-naïeve patiënten met diabetes type 1 is ongeveer 50% van de totale dagelijkse insulinedosis en dient over de maaltijden te worden verdeeld op basis van de hoeveelheid en samenstelling van de maaltijden. De rest van de totale dagelijkse dosis insuline dient te worden toegediend in de vorm van middellang- of langwerkende insuline. Als algemene regel geldt dat voor het berekenen van de totale dagelijkse startdosis insuline voor insuline-naïeve patiënten met diabetes type 1 kan worden uitgegaan van 0,2 tot 0,4 eenheden insuline per kilogram lichaamsgewicht.
Patiënten met diabetes mellitus type 2
De voorgestelde startdosis is 4 eenheden bij een of meerdere maaltijden. Het aantal injecties en de daaropvolgende titratie zijn afhankelijk van de individuele glykemische doelstelling en de hoeveelheid en samenstelling van de maaltijden.
Dosisaanpassing kan dagelijks worden overwogen op basis van de zelf gemeten plasmaglucose (self-measured plasmaglucose, SMPG) op de voorgaande dag(en) volgens tabel 1.
• De dosis vóór het ontbijt dient te worden aangepast volgens de SMPG vóór het middageten van de vorige dag
• De dosis vóór het middageten dient te worden aangepast volgens de SMPG vóór het avondeten van de vorige dag
• De dosis vóór het avondeten dient te worden aangepast volgens de SMPG bij het slapengaan van de vorige dag
Tabel 1. Dosisaanpassing | ||
SMPG (zie hierboven) | Dosisaanpassing | |
mmol/l | mg/dl | Eenheid |
< 4 | < 71 | -1 |
4-6 | 71-108 | Geen aanpassing |
> 6 | > 108 | +1 |
Specifieke doelgroepen
Oudere patiënten (≥ 65 jaar)
De veiligheid en werkzaamheid van Fiasp bij oudere patiënten van 65 tot 75 jaar zijn vastgesteld. Nauwgezette controle van de glucosespiegel wordt aanbevolen en de insulinedosis dient individueel te worden aangepast (zie rubriek 5.1 en 5.2). Er is beperkte therapeutische ervaring bij patiënten ≥ 75 jaar.
Nierinsufficiëntie
Nierinsufficiëntie kan de insulinebehoefte van de patiënt verlagen. Bij patiënten met nierinsufficiëntie dient de glucosespiegel vaker te worden gecontroleerd en dient de dosis individueel te worden aangepast (zie rubriek 5.2).
Leverinsufficiëntie
Leverinsufficiëntie kan de insulinebehoefte van de patiënt verlagen. Bij patiënten met leverinsufficiëntie dient de glucosespiegel vaker te worden gecontroleerd en dient de dosis individueel te worden aangepast (zie rubriek 5.2).
Pediatrische patiënten
Fiasp kan worden gebruikt bij adolescenten en kinderen van 1 jaar en ouder (zie rubriek 5.1). Er is geen klinische ervaring met het gebruik van Fiasp bij kinderen jonger dan 2 jaar.
Het wordt aanbevolen om Fiasp 0 tot 2 minuten voor het begin van de maaltijd toe te dienen, echter in situaties waarbij er onzekerheid is over de maaltijdinname is het tijdstip van toediening flexibel tot maximaal 20 minuten na het begin van de maaltijd.
Overschakelen van andere insulines
Een nauwgezette controle van de bloedglucosespiegel verdient aanbeveling tijdens het overschakelen van andere maaltijdinsulines en gedurende de eerste weken daarna. Er kan worden overgeschakeld van een andere maaltijdinsuline op basis van eenheid op eenheid. Een patiënt overschakelen, van een ander type of merk insuline of van insuline van een andere fabrikant, op Fiasp moet onder strikt medisch toezicht plaatsvinden en kan een dosisaanpassing noodzakelijk maken.
Het kan noodzakelijk zijn de doses en het tijdstip van toediening van gelijktijdig gebruikte middellang- of langwerkende insulines of de overige tegelijkertijd gevolgde diabetesbehandeling aan te passen.
Wijze van toediening
Subcutane injectie
Het wordt aanbevolen om Fiasp subcutaan toe te dienen door middel van een injectie in de buikwand of de bovenarm (zie rubriek 5.2). De injectieplaatsen dienen altijd te worden afgewisseld binnen eenzelfde gebied om het risico op lipodystrofie en cutane amyloïdose te beperken (zie rubriek 4.4 en 4.8).
Fiasp 100 eenheden/ml FlexTouch oplossing voor injectie in een voorgevulde pen
De voorgevulde pen (FlexTouch) levert 1–80 eenheden, in stappen van 1 eenheid.
FlexTouch wordt geleverd met een bijsluiter met gedetailleerde gebruiksinstructies die moeten worden opgevolgd. Voor instructies over toediening, zie “Gebruiksaanwijzing voor Fiasp FlexTouch” aan het einde van de bijsluiter.
De voorgevulde pen is alleen geschikt voor subcutane injecties. Als toediening met een injectiespuit of intraveneuze injectie noodzakelijk is, moet een injectieflacon worden gebruikt. Indien toediening via een infusiepomp noodzakelijk is, moet een injectieflacon of een PumpCart patroon worden gebruikt.
Fiasp 100 eenheden/ml Penfill oplossing voor injectie in een patroon
Toediening met een herbruikbare insulinepen
Als toediening met een injectiespuit of intraveneuze injectie noodzakelijk is, moet een injectieflacon worden gebruikt. Indien toediening via een infusiepomp noodzakelijk is, moet een injectieflacon of een PumpCart patroon worden gebruikt (zie rubriek 6.6).
Fiasp 100 eenheden/ml oplossing voor injectie in een injectieflacon
Toediening met een spuit
De injectieflacon moet worden gebruikt met insulinespuiten met de bijbehorende schaalverdeling (eenheden-100 of 100 eenheden/ml).
Continue subcutane insuline-infusie (CSII)
Fiasp oplossing voor injectie in een injectieflacon kan worden gebruikt voor CSII in pompen die geschikt zijn voor insuline-infusie en zal voorzien in zowel de behoefte aan bolusinsuline (ongeveer 50%) als basale insuline. Het kan worden toegediend volgens de instructies van de fabrikant van de pomp, bij voorkeur in de buik. Bij gebruik in een insuline-infusiepomp mag het niet worden verdund of gemengd met andere geneesmiddelen die insuline bevatten.
Patiënten die CSII toepassen moeten instructies krijgen over het gebruik van de pomp en moeten het juiste reservoir en de juiste slang voor de pomp gebruiken (zie rubriek 6.6). De infusieset (slang en canule) moet worden vervangen conform de instructies die zijn vermeld in de productinformatie die bij de infusieset wordt geleverd.
Patiënten die Fiasp toedienen via CSII moeten worden getraind in het toedienen van insuline via injectie en moeten een alternatieve insulinebehandeling tot hun beschikking hebben voor het geval dat de pomp niet functioneert.
Fiasp 100 eenheden/ml PumpCart oplossing voor injectie in een patroon
Toediening via CSII
De patroon (PumpCart) is alleen voor gebruik met een insuline-infusiepompsysteem dat ontwikkeld is voor gebruik met deze patroon (zie rubriek 6.6).
Fiasp voorziet in zowel de behoefte aan bolusinsuline (ongeveer 50%) als aan de basale insulinebehoefte. Het kan worden toegediend volgens de instructies van de fabrikant van de pomp, bij voorkeur in de buik. De infusieplaats moet worden afgewisseld binnen eenzelfde gebied om de kans op lipodystrofie te verminderen.
Patiënten die CSII toepassen moeten instructies krijgen over het gebruik van de pomp en moeten de juiste slang voor de pomp gebruiken (zie rubriek 6.6). De infusieset (slang en canule) moet worden vervangen conform de instructies die zijn vermeld in de productinformatie die bij de infusieset wordt geleverd.
Patiënten die Fiasp toedienen via CSII moeten worden getraind in het toedienen van insuline via injectie en moeten een alternatieve insulinebehandeling tot hun beschikking hebben voor het geval dat de pomp niet functioneert.
De patroon (PumpCart) is alleen geschikt voor CSII in pompsystemen die geschikt zijn voor insuline-infusie. Indien toediening via een injectiespuit of intraveneuze injectie noodzakelijk is, moet een injectieflacon worden gebruikt.
Intraveneus gebruik
Fiasp 100 eenheden/ml oplossing voor injectie in een injectieflacon
Zo nodig kan Fiasp intraveneus worden toegediend door beroepsbeoefenaren in de gezondheidszorg.
Voor intraveneus gebruik moet het middel worden gebruikt in concentraties van 0,5 eenheid/ml tot 1 eenheid/ml insuline aspart in infusiesystemen, met behulp van infusiezakken van polypropyleen.
Fiasp mag niet worden gemengd met andere insulines of met andere geneesmiddelen uitgezonderd de geneesmiddelen die vermeld worden in rubriek 6.6. Voor instructies over verdunning van het geneesmiddel voor toediening, zie rubriek 6.6.
Bloedglucosecontrole is noodzakelijk tijdens de insuline-infusie. Er moet voor worden gezorgd dat de insuline in de infusiezak wordt geïnjecteerd en niet alleen in de toegangspoort.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De meest frequent gemelde bijwerking tijdens de behandeling is hypoglykemie (zie rubriek ‘Beschrijving van een geselecteerd aantal bijwerkingen’ hieronder).
Lijst met bijwerkingen in tabelvorm
De hierna vermelde bijwerkingen (tabel 2) zijn gebaseerd op gegevens uit zes afgeronde therapeutische bevestigingsstudies bij volwassenen. Frequentiecategorieën zijn gedefinieerd aan de hand van de volgende regel: zeer vaak (≥1/10); vaak (≥1/100, <1/10); soms (≥1/1.000, <1/100); zelden (≥1/10.000, <1/1.000); zeer zelden (<1/10.000) en niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Tabel 2. Bijwerkingen gemeld in klinische studies
MedDRA systeem/orgaanklasse | Zeer vaak | Vaak | Soms | Niet bekend |
Immuunsysteem-aandoeningen |
|
| Overgevoeligheid | Anafylactische reacties |
Voedings- en stofwisselingsstoornissen | Hypoglykemie |
|
|
|
Huid- en onderhuidaandoeningen |
| Allergische huidreacties | Lipodystrofie | Cutane amyloïdose† |
Algemene aandoeningen en toedieningsplaats-stoornissen |
| Reacties op de injectie-/infusieplaats |
|
|
† ADR (Adverse Drug Reaction) afkomstig van postmarketing bronnen.
Beschrijving van een geselecteerd aantal bijwerkingen
Allergische reacties
Allergische huidreacties die zijn gemeld bij het gebruik van Fiasp (1,8% t.o.v. 1,5% voor de comparator), zijn onder meer eczeem, rash, rash pruritus, urticaria en dermatitis.
Met Fiasp werden soms gegeneraliseerde overgevoeligheidsreacties (verschijnselen: gegeneraliseerde huidrash en gezichtsoedeem) gemeld (0,2% t.o.v. 0,3% voor de comparator).
Hypoglykemie
Hypoglykemie kan optreden wanneer de insulinedosis te hoog is ten opzichte van de insulinebehoefte. Ernstige hypoglykemie kan leiden tot verlies van het bewustzijn en/of convulsies en kan een tijdelijke of permanente beschadiging van de hersenfunctie of zelfs de dood tot gevolg hebben. De symptomen van hypoglykemie treden meestal plotseling op. Deze symptomen kunnen zijn: koud zweet, een koude bleke huid, vermoeidheid, zenuwachtigheid of tremor, angstgevoelens, ongewone vermoeidheid of zwakte, verwardheid, concentratiestoornissen, sufheid, overmatig hongergevoel, visusstoornissen, hoofdpijn, misselijkheid en hartkloppingen (zie rubriek 4.4 en 5.1). Hypoglykemie kan eerder optreden na een injectie of infusie met Fiasp vergeleken met andere maaltijdinsulines vanwege de eerder intredende werking.
Huid- en onderhuidaandoeningen
Lipodystrofie (waaronder lipohypertrofie, lipoatrofie) en cutane amyloïdose kunnen optreden op de injectieplaats en kunnen de plaatselijke insuline-absorptie vertragen. Lipodystrofie werd gemeld op de injectie-/infusieplaats bij patiënten die met Fiasp werden behandeld (0,5% t.o.v. 0,2% bij de comparator). Het continue afwisselen van de injectieplaats binnen eenzelfde gebied kan helpen deze reacties te verminderen of te voorkomen (zie rubriek 4.4).
Reacties op de injectie-/infusieplaats
Reacties op de injectieplaats (waaronder rash, roodheid, ontsteking, pijn en blauwe plekken) werden gemeld bij patiënten die met Fiasp werden behandeld (1,3% t.o.v. 1,0% bij de comparator). Bij patiënten die CSII gebruiken (N=261): infusieplaatsreacties (waaronder roodheid, ontsteking, irritatie, pijn, blauwe plekken en jeuk) werden gemeld bij patiënten die met Fiasp werden behandeld (10,0% t.o.v. 8,3% bij de comparator). Deze reacties zijn gewoonlijk mild en voorbijgaand van aard en verdwijnen normaliter tijdens het voortzetten van de behandeling.
Pediatrische patiënten
Veiligheid en werkzaamheid zijn onderzocht in een therapeutische bevestigingsstudie bij kinderen van 2 tot 18 jaar oud met diabetes type 1. In de studie werden 519 patiënten behandeld met Fiasp. In het algemeen wijzen frequentie, type en ernst van bijwerkingen bij pediatrische patiënten niet op verschillen met de ervaringen bij volwassen patiënten. Lipodystrofie (inclusief lipohypertrofie, lipoatrofie) op de injectieplaats werd vaker gerapporteerd in deze studie met pediatrische patiënten in vergelijking met studies bij volwassenen (zie hierboven). Bij pediatrische patiënten werd lipodystrofie gerapporteerd met een frequentie van 2,1% bij Fiasp versus 1,6% bij NovoRapid.
Andere specifieke doelgroepen
Gebaseerd op de resultaten van klinische studies met insuline aspart over het algemeen, wijzen de frequentie, type en ernst van bijwerkingen waargenomen bij oudere patiënten en bij patiënten met nier- of leverinsufficiëntie niet op enig verschil vergeleken met de uitgebreidere ervaring in de algemene populatie. Het veiligheidsprofiel bij zeer oude patiënten (≥ 75 jaar) of patiënten met matig ernstige tot ernstige nierinsufficiëntie of leverinsufficiëntie is beperkt. Fiasp werd toegediend aan oudere patiënten om de farmacokinetische eigenschappen te onderzoeken (zie rubriek 5.2).
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het nationale meldsysteem:
België
Federaal agentschap voor geneesmiddelen en gezondheidsproducten
Afdeling Vigilantie
Postbus 97
B-1000 Brussel Madou
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Novo Nordisk A/S
Novo Allé
DK-2880 Bagsværd
Denemarken
8. NUMMERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/16/1160/001
EU/1/16/1160/002
EU/1/16/1160/003
EU/1/16/1160/004
EU/1/16/1160/005
EU/1/16/1160/006
EU/1/16/1160/007
EU/1/16/1160/008
EU/1/16/1160/009
EU/1/16/1160/010
EU/1/16/1160/011
EU/1/16/1160/012
EU/1/16/1160/013
10. DATUM VAN HERZIENING VAN DE TEKST
08/2021
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau http://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3593720 | FIASP 100E/ML OPL INJ FL INJ 1 X 10ML | A10AB05 | € 24,41 | - | Ja | € 2 | € 1 |
| 3593746 | FIASP 100E/ML OPL INJ VOORGEVULDE PEN 10 X 3ML | A10AB05 | € 79,19 | - | Ja | € 2 | € 1 |
| 3593712 | FIASP 100E/ML PENFILL OPL INJ PATRONEN 5 X 3ML | A10AB05 | € 36,33 | - | Ja | € 2 | € 1 |