SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Fasenra 30 mg oplossing voor injectie in voorgevulde spuit
Fasenra 30 mg oplossing voor injectie in voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Voorgevulde spuit
Elke voorgevulde spuit bevat 30 mg benralizumab* in 1 ml.
Voorgevulde pen
Elke voorgevulde pen bevat 30 mg benralizumab* in 1 ml.
*Benralizumab is een gehumaniseerd monoklonaal antilichaam dat geproduceerd wordt uit ovariumcellen van de Chinese hamster (Chinese hamster ovary, CHO) met behulp van recombinant-DNA-technologie.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie (injectie) in voorgevulde spuit
Oplossing voor injectie (injectie) in voorgevulde pen (Fasenra Pen)
Heldere tot opalescente, kleurloze tot gele oplossing die mogelijk transparante of witte tot bijna witte deeltjes kan bevatten.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Astma
Fasenra is geïndiceerd als aanvullende onderhoudsbehandeling bij volwassen patiënten met ernstig eosinofiel astma die onvoldoende onder controle is ondanks hoog gedoseerde inhalatiecorticosteroïden en langwerkende β-agonisten (zie rubriek 5.1).
Eosinofiele granulomatose met polyangiitis (EGPA)
Fasenra is geïndiceerd als aanvullende behandeling voor volwassen patiënten met recidiverende of refractaire eosinofiele granulomatose met polyangiitis (zie rubriek 5.1).
4.2 Dosering en wijze van toediening
De behandeling met Fasenra moet worden gestart door een arts die ervaring heeft met de diagnose en behandeling van aandoeningen waarvoor benralizumab is geïndiceerd (zie rubriek 4.1).
Na de juiste training in de subcutane injectietechniek en voorlichting over tekenen en symptomen van overgevoeligheidsreacties (zie rubriek 4.4), kunnen patiënten of zorgverleners Fasenra toedienen, als hun arts bepaalt dat dit passend is en er geen bekende voorgeschiedenis van anafylaxie is, met waar nodig medische follow-up. Het zelf toedienen kan alleen worden overwogen bij patiënten die al ervaring hebben met de behandeling met Fasenra.
Dosering
Fasenra is bestemd voor langdurige behandeling. Er dient minstens jaarlijks beslist te worden of de therapie dient te worden voortgezet op basis van de ernst van de ziekte, de mate waarin de ziekte onder controle is en het aantal eosinofielen in het bloed.
Astma
De aanbevolen dosering van benralizumab is 30 mg via subcutane injectie elke 4 weken voor de eerste 3 doses en daarna elke 8 weken.
EGPA
De aanbevolen dosering van benralizumab is 30 mg via subcutane injectie elke 4 weken.
Voor patiënten bij wie levensbedreigende verschijnselen van EGPA optreden, moet worden nagegaan of voortzetting van de behandeling noodzakelijk is, aangezien Fasenra bij deze populatie niet is onderzocht.
Gemiste dosis
Als een injectie op de geplande datum wordt gemist, moet de dosering zo snel mogelijk worden hervat volgens het aangegeven doseringsregime. Er mag geen dubbele dosis worden toegediend.
Ouderen
Er is geen dosisaanpassing nodig bij oudere patiënten (zie rubriek 5.2).
Nier- en leverinsufficiëntie
Er is geen dosisaanpassing nodig voor patiënten met nier- of leverinsufficiëntie (zie rubriek 5.2).
Pediatrische patiënten
De veiligheid en werkzaamheid van Fasenra bij kinderen en adolescenten in de leeftijd van 6 tot en met 17 jaar met astma zijn niet vastgesteld. De momenteel beperkte gegevens bij kinderen van 6 tot en met 11 jaar oud en gegevens bij adolescenten van 12 tot en met 17 jaar worden beschreven in rubrieken 4.8, 5.1 en 5.2, maar er kan geen doseringsadvies worden gegeven.
De veiligheid en werkzaamheid van Fasenra bij kinderen jonger dan 6 jaar met astma zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
De veiligheid en werkzaamheid van Fasenra bij kinderen en adolescenten jonger dan 18 jaar met EGPA zijn niet vastgesteld.
Wijze van toediening
Dit geneesmiddel wordt toegediend als een subcutane injectie.
Dit middel moet worden geïnjecteerd in de dij of buik. Als de beroepsbeoefenaar in de gezondheidszorg of zorgverlener de injectie toedient, kan de bovenarm ook worden gebruikt. Het mag niet worden geïnjecteerd in gebieden waar de huid gevoelig is, blauwe plekken heeft, erythemateus of verhard is.
Uitgebreide instructies voor toediening met de voorgevulde spuit/voorgevulde pen zijn te vinden in de ‘Gebruiksaanwijzing’.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
Het veiligheidsprofiel van benralizumab bij astma en bij EGPA is vergelijkbaar.
Bij astma zijn de meest gemelde bijwerkingen tijdens de behandeling hoofdpijn (8%) en faryngitis (3%). De meest gemelde bijwerking bij EGPA is hoofdpijn (17%). Er zijn gevallen van anafylactische reacties van uiteenlopende ernst gemeld voor benralizumab.
Tabel met lijst van bijwerkingen
De volgende bijwerkingen zijn tijdens klinische onderzoeken met benralizumab bij astma en EGPA en uit postmarketingervaring gemeld.
De frequentie van bijwerkingen wordt gedefinieerd als: zeer vaak (≥ 1/10); vaak (≥ 1/100, < 1/10); soms (≥ 1/1.000, < 1/100); zelden (≥ 1/10.000, < 1/1.000); zeer zelden (< 1/10.000) en niet bekend (kan met de beschikbare gegevens niet worden bepaald). Binnen elke frequentiegroep worden de bijwerkingen gerangschikt naar afnemende ernst.
Tabel 1. Tabel met lijst van bijwerkingen
MedDRA Systeem/orgaanklasse | Bijwerking | Frequentie |
Infecties en parasitaire aandoeningen | Faryngitisa | Vaak |
Immuunsysteemaandoeningen | Overgevoeligheidsreactiesb | Vaak |
Zenuwstelselaandoeningen | Hoofdpijnc | Vaak |
Algemene aandoeningen en toedieningsplaatsstoornissen | Pyrexie | Vaak |
a. Faryngitis is gedefinieerd door de volgende gegroepeerde voorkeurstermen: ‘Faryngitis’, ‘Bacteriële faryngitis’, ‘Virale faryngitis’, ‘Streptokokkenfaryngitis’.
b. Overgevoeligheidsreacties zijn gedefinieerd door de volgende gegroepeerde voorkeurstermen: ‘Urticaria’, ‘Papuleuze urticaria’ en ‘Rash’. Voor voorbeelden van de gemelde bijbehorende verschijnselen en een beschrijving van de tijd tot begin, zie rubriek 4.4.
c. Zeer vaak in het EGPA-studie
d. Zie “Beschrijving van geselecteerde bijwerkingen”
Beschrijving van geselecteerde bijwerkingen
Reacties op de injectieplaats
In placebogecontroleerde astmastudies traden reacties op de injectieplaats (bijv. pijn, roodheid, jeuk, papels) op met een frequentie van 2,2% bij patiënten die behandeld werden met de aanbevolen dosis benralizumab in vergelijking met 1,9% bij patiënten die werden behandeld met placebo. De reacties waren van voorbijgaande aard.
Veiligheid op de lange termijn
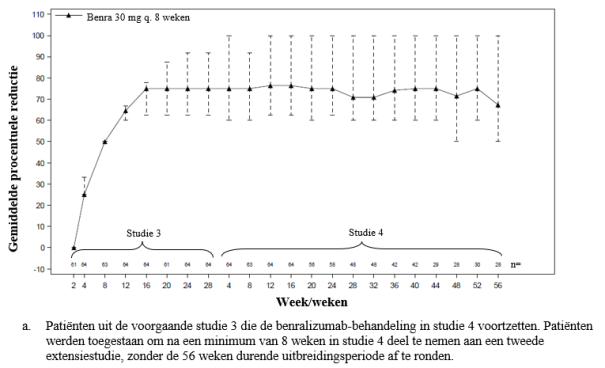
In een extensiestudie van 56 weken (studie 4) bij patiënten met astma van de studies 1, 2 en 3, werden 842 patiënten behandeld met Fasenra in de aanbevolen dosis en bleven in de studie. Het algemene veiligheidsprofiel was vergelijkbaar met dat van de hierboven beschreven astmastudies. Daarnaast werden in een ‘open label’-extensiestudie naar de veiligheid (studie 5) bij patiënten met astma uit eerdere studies 226 patiënten behandeld met Fasenra in de aanbevolen dosis gedurende maximaal 43 maanden. In combinatie met de behandelingsperiode in eerdere studies, komt dit overeen met een mediane opvolging van 3,4 jaar (spreiding: 8,5 maanden ‑ 5,3 jaar). Het veiligheidsprofiel gedurende deze follow-upperiode was consistent met het bekende veiligheidsprofiel van Fasenra.
Pediatrische patiënten
Er zijn beperkte gegevens bij pediatrische patiënten. Er waren 108 adolescenten van 12 tot en met 17 jaar met astma die deelnamen aan de fase 3-studies (studie 1: n=53, studie 2: n=55). Van hen kregen er 46 placebo, 40 kregen benralizumab elke 4 weken voor de eerste 3 doses, gevolgd door elke 8 weken, en 22 kregen benralizumab elke 4 weken. Adolescente patiënten van 12 tot en met 17 jaar (n=86) uit studie 1 en 2 zetten de behandeling met benralizumab in studie 4 voort gedurende maximaal 108 weken. De bij adolescente patiënten waargenomen frequentie, type en ernst van bijwerkingen waren vergelijkbaar met die bij volwassenen.
In een open-label, ongecontroleerd farmacokinetisch en farmacodynamisch onderzoek van 48 weken bij een beperkt aantal pediatrische patiënten (n=28) met ongecontroleerd ernstig astma was het veiligheidsprofiel voor patiënten van 6 tot en met 11 jaar oud vergelijkbaar met dat voor de volwassenen- en adolescentenpopulatie (zie rubriek 4.2).
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
AstraZeneca AB
SE‑151 85 Södertälje
Zweden
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/17/1252/001 1 voorgevulde spuit
EU/1/17/1252/002 1 voorgevulde pen
10. DATUM VAN HERZIENING VAN DE TEKST
10/2024
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3678448 | FASENRA 30MG OPL INJ VOORGEVULDE SPUIT 1ML | R03DX10 | € 2422,49 | - | Ja | € 12,8 | € 8,5 |