SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
RISPERDAL CONSTA 25 mg, poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte
RISPERDAL CONSTA 37,5 mg, poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte
RISPERDAL CONSTA 50 mg, poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
1 injectieflacon bevat 25 mg risperidon.
1 injectieflacon bevat 37,5 mg risperidon.
1 injectieflacon bevat 50 mg risperidon.
1 ml gereconstitueerde suspensie bevat 12,5 mg risperidon.
1 ml gereconstitueerde suspensie bevat 18,75 mg risperidon.
1 ml gereconstitueerde suspensie bevat 25 mg risperidon.
Hulpstoffen met bekend effect
1 ml gereconstitueerde suspensie bevat 3 mg natrium.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Poeder en oplosmiddel voor suspensie voor injectie met verlengde afgifte.
Injectieflacon met poeder
Wit tot gebroken wit los poeder.
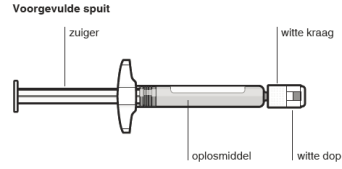
Voorgevulde spuit met oplosmiddel voor bereiding van de suspensie
Heldere, kleurloze, waterige oplossing.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
RISPERDAL CONSTA is geïndiceerd voor de onderhoudsbehandeling van schizofrenie bij patiënten die reeds gestabiliseerd zijn met orale antipsychotica.
4.2 Dosering en wijze van toediening
Dosering
Volwassenen
Startdosering
Voor de meeste patiënten is de aanbevolen dosering 25 mg intramusculair per twee weken.
Voor patiënten die gedurende twee weken of langer met een vaste dosis oraal risperidon worden behandeld, dient het volgende conversieschema in acht te worden genomen. Bij patiënten met een dosis van 4 mg oraal risperidon of lager moet RISPERDAL CONSTA 25 mg worden toegediend. Voor patiënten met een hogere orale dosering dient een dosis RISPERDAL CONSTA van 37,5 mg te worden overwogen.
Bij patiënten die momenteel niet behandeld worden met oraal risperidon, dient de orale dosis vóór de behandeling te worden overwogen bij het kiezen van de intramusculaire startdosis. De aanbevolen startdosering is 25 mg RISPERDAL CONSTA per twee weken. Voor patiënten met hogere doseringen van het gebruikte orale antipsychoticum kan de hogere dosis RISPERDAL CONSTA van 37,5 mg worden overwogen.
Gedurende drie weken na de eerste RISPERDAL CONSTA-injectie dient een adequaat antipsychotisch effect gewaarborgd te worden met oraal risperidon of het laatst gebruikte antipsychoticum (zie rubriek 5.2).
RISPERDAL CONSTA mag niet bij acute exacerbaties van schizofrenie worden gebruikt zonder dat de patiënt verder behandeld wordt met oraal risperidon of een eerder gebruikt antipsychoticum, gedurende de eerste drie weken na de eerste injectie met RISPERDAL CONSTA.
Onderhoudsdosis
Voor de meeste patiënten is de aanbevolen dosering 25 mg intramusculair per twee weken. Sommige patiënten kunnen baat hebben bij een hogere dosering van 37,5 mg of 50 mg. De dosis mag niet vaker dan elke vier weken worden verhoogd. Het effect van deze dosisaanpassing kan niet eerder dan drie weken na de eerste injectie met de hogere dosis worden verwacht. In klinische studies werd er geen bijkomend voordeel waargenomen met 75 mg. Doseringen hoger dan 50 mg iedere twee weken worden niet aanbevolen.
Ouderen
Er is geen dosisaanpassing nodig. De aanbevolen dosis is 25 mg intramusculair elke twee weken. Bij patiënten die momenteel niet behandeld worden met oraal risperidon is de aanbevolen dosis 25 mg RISPERDAL CONSTA per twee weken. Voor patiënten die gedurende twee weken of langer met een vaste dosis oraal risperidon worden behandeld, dient het volgende conversieschema in acht te worden genomen. Bij patiënten met een dosis van 4 mg oraal risperidon of lager moet RISPERDAL CONSTA 25 mg worden toegediend. Voor patiënten met een hogere orale dosering dient een dosis RISPERDAL CONSTA van 37,5 mg te worden overwogen.
Gedurende drie weken na de eerste RISPERDAL CONSTA-injectie dient een adequaat antipsychotisch effect gewaarborgd te worden (zie rubriek 5.2). Klinische gegevens van RISPERDAL CONSTA bij ouderen zijn beperkt. RISPERDAL CONSTA dient met voorzichtigheid te worden gebruikt bij ouderen.
Lever- en nierfunctiestoornissen
RISPERDAL CONSTA is niet onderzocht bij patiënten met lever- of nierinsufficiëntie.
Als een patiënt met een slechte lever- of nierfunctie moet worden behandeld met RISPERDAL CONSTA, wordt een aanvangsdosis van 0,5 mg oraal risperidon tweemaal daags aanbevolen tijdens de eerste week. De tweede week kan 1 mg tweemaal daags of 2 mg eenmaal daags worden gegeven. Als een orale dosis van tenminste 2 mg per dag goed wordt verdragen, kan overgeschakeld worden naar een injectie van 25 mg RISPERDAL CONSTA elke twee weken.
Gedurende drie weken na de eerste RISPERDAL CONSTA-injectie dient een adequaat antipsychotisch effect gewaarborgd te worden (zie rubriek 5.2).
Pediatrische patiënten
De veiligheid en werkzaamheid van RISPERDAL CONSTA bij kinderen jonger dan 18 jaar zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
Wijze van toediening
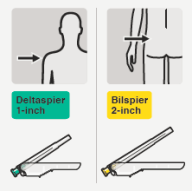
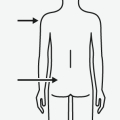
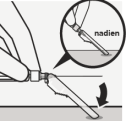
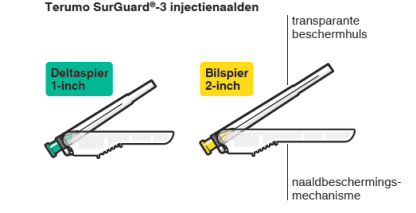
RISPERDAL CONSTA moet elke twee weken worden toegediend door een diepe intramusculaire injectie in de deltaspier of bilspier met de daarvoor bestemde veiligheidsnaald. Gebruik de 1-inch (25 mm) naald voor toediening in de deltaspier, afwisselend in de linker- en de rechterarm. Gebruik de 2-inch (51 mm) naald voor toediening in de bilspier, afwisselend in de linker- en de rechterbil. Niet intraveneus toedienen (zie rubrieken 4.4 en 6.6).
Voor instructies over reconstitutie van het geneesmiddel voorafgaand aan toediening, zie rubriek 6.6.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor één van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
De meest frequent gerapporteerde bijwerkingen (incidentie ≥ 1/10) zijn: slapeloosheid, angst, hoofdpijn, infectie van de bovenste luchtwegen, parkinsonisme en depressie.
De bijwerkingen die dosisgerelateerd bleken te zijn, omvatten parkinsonisme en acathisie.
Ernstige reacties op de injectieplaats waaronder necrose op de injectieplaats, abces, cellulitis, zweer, hematoom, cyste en knobbeltje werden in de postmarketingfase gemeld. De frequentie is beschouwd als onbekend (kan niet worden geschat uit de beschikbare gegevens). In een enkel geval was een chirurgische ingreep nodig.
Hieronder staan alle bijwerkingen die met risperidon werden gerapporteerd in klinisch onderzoek en in de postmarketingfase, waarbij de frequentiecategorie is geschat op basis van klinisch onderzoek met RISPERDAL CONSTA. De volgende termen en frequenties worden gebruikt: zeer vaak (≥ 1/10), vaak (≥ 1/100 tot < 1/10), soms (≥ 1/1.000 tot < 1/100), zelden (≥ 1/10.000 tot < 1/1.000), zeer zelden (< 1/10.000) en niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Binnen elke frequentiegroep worden bijwerkingen gerangschikt op afnemende ernst.
Systeem/Orgaan-klassen | Bijwerking | |||||
Frequentie | ||||||
| Zeer vaak | Vaak | Soms | Zelden | Zeer zelden | Niet bekend |
Infecties en parasitaire aandoeningen | bovenste luchtweginfec-tie | pneumonie, bronchitis, sinusitis, urineweginfectie, influenza | luchtweginfectie, cystitis, oorinfectie, ooginfectie, tonsillitis, onychomycose, cellulitis, infectie, gelokaliseerde infectie, virale infectie, acarodermatitis, subcutaan abces |
|
|
|
Bloed- en lymfestelselaandoe-ningen |
| anemie | witte bloedcellen verlaagd, trombocytopenie, hematocriet verlaagd | agranulocytosec, neutropenie, eosinofielentelling verhoogd |
|
|
Immuunsysteemaan-doeningen |
|
| overgevoeligheid | anafylactische reactiec |
|
|
Endocriene aandoeningen |
| hyperprolactinemiea | glucose in urine | antidiuretisch hormoonsecrectie-deficiëntie |
|
|
Voedings- en stofwisselingsstoor-nissen |
| hyperglykemie, gewicht verhoogd, gestimuleerde eetlust, gewicht verlaagd, verminderde eetlust | diabetes mellitusb, anorexie, bloed triglyceriden verhoogd, bloed cholesterol verhoogd | waterintoxicatiec, hypoglykemie, hyperinsulinemiec, polydipsie | diabetische ketoacidose |
|
Psychische stoornissen | insomniad, depressie, angst | slaapstoornis, agitatie, verminderd libido | manie, verwarde toestand, anorgasmie, zenuwachtigheid, nachtmerrie | katatonie, |
|
|
Zenuwstelselaandoe-ningen | parkinsonismed, hoofdpijn | sedatie/somnolentie, acathisied, dystonied, duizeligheid, dyskinesied, tremor | tardieve dyskinesie, cerebrale ischemie, bewustzijnsverlies, convulsied, syncope, psychomotorische hyperactiviteit, evenwichtsstoornis, coördinatie afwijkend, duizeligheid houdingsafhankelijk, aandachtsstoornis, dysartrie, dysgeusie, hypo-esthesie, paresthesie | maligne neurolepti-casyndroom, cerebrovasculaire stoornis, niet reagerend op prikkels, verminderd bewustzijn, diabetisch coma, titubatie van het hoofd |
|
|
Oogaandoeningen |
| gezichtsvermogen wazig | conjunctivitis, droog oog, traanproductie verhoogd, oculaire hyperemie | retina arterie occlusie, glaucoom, oogbewegingsafwij-king, oogrollen, fotofobie, schilferige ooglidrand, floppy iris‑syndroom (intraoperatief)c |
|
|
Evenwichtsorgaan- en ooraandoeningen |
|
| vertigo, tinnitus, oorpijn |
|
|
|
Hartaandoeningen |
| tachycardie | atriumfibrilatie, atrioventriculair blok, geleidingsstoornis, electrocardiogram QT verlengd, bradycardie, electrocardiogram abnormaal, hartkloppingen | sinusaritmie |
|
|
Bloedvataandoening-en |
| hypotensie, hypertensie | orthostatische hypotensie | longembolie, veneuze trombose, overmatig blozen |
|
|
Ademhalingsstelsel-, borstkas- en mediastinumaandoe-ningen |
| dyspneu, faryngolaryngeale pijn, hoest, neuscongestie | hyperventilatie, luchtwegcongestie, piepen, bloedneus | slaapapneusyndroom, aspiratiepneumonie, longstuwing, roggelen, dysfonie, ademhalingsstoornis |
|
|
Maagdarmstelselaan-doeningen |
| abdominale pijn, abdominaal ongemak, braken, nausea, constipatie, gastro-enteritis, diarree, dyspepsie, droge mond, tandpijn | fecale incontinentie, dysfagie, flatulentie | pancreatitis, intestinale obstructie, gezwollen tong, fecaloom, cheilitis | ileus |
|
Huid- en onderhuid-aandoeningen |
| rash | pruritus, alopecia, eczeem, droge huid, erytheem, huidverkleuring, acne, seborroïsche dermatitis | geneesmiddelenerup-tie, urticaria, hyperkeratose, hoofdroos, huidaandoening, huidlaesie | angio-oedeem | Stevens-Johnson-syndroom/toxische epidermale necrolysec |
Skeletspierstelsel- en bindweefselaan-doeningen |
| spierspasmen, musculoskeletale pijn, rugpijn, artralgie | bloed creatinefosfoki-nase verhoogd, gewrichtsstijfheid, gewrichtszwelling, spierzwakte, nekpijn | rabdomyolyse, houding afwijkend |
|
|
Nier- en urineweg-aandoeningen |
| urine-incontinentie | pollakisurie, urineretentie, dysurie |
|
|
|
Zwangerschap, perinatale periode en puerperium |
|
|
| neonataal onttrekkingssyn-droomc |
|
|
Voortplantingsstelsel- en borstaandoeningen |
| erectiestoornissen, amenorroe, galactorroe | ejaculatiestoornis, uitstel van menstruatie, menstruatiestoornisd, gynaecomastie, seksuele disfunctie, pijn in de borsten, gevoelige borsten, vaginale afscheiding | priapismec, bloedaandrang in de borsten, borstvergroting, borstuitvloed |
|
|
Algemene aandoe-ningen en toedie-ningsplaatsstoornis-sen |
| oedeemd, pyrexie, borstkaspijn, asthenie, vermoeidheid, pijn, injectieplaatsreactie | gezichtsoedeem, koude rillingen, lichaamstemperatuur verhoogd, gangafwijking, dorst, ongemak op de borst, malaise, abnormaal gevoel, induratiec | hypothermie, lichaamstemperatuur verlaagd, perifere koude, geneesmiddelontrek-kingssyndroom, onbehagen |
|
|
Lever- en galaan-doeningen |
| transaminasen verhoogd, gamma- glutamyltransferase verhoogd | leverenzym verhoogd | geelzucht |
|
|
Letsels, intoxicaties en verrichtingscom-plicaties |
| vallen | procedurepijn |
|
|
|
a Hyperprolactinemie kan in sommige gevallen leiden tot gynaecomastie, menstruatiestoornissen, amenorroe, anovulatie, galactorrhoea, fertiliteitsstoornis, verminderd libido en erectiele disfunctie.
b In placebogecontroleerde studies werd diabetes mellitus gemeld bij 0,18% van de met risperidon behandelde personen tegenover 0,11% in de placebogroep. De totale incidentie uit alle klinische studies was 0,43% bij alle personen behandeld met risperidon.
c Niet waargenomen in klinische studies met RISPERDAL CONSTA, maar waargenomen in de post-marketing omgeving met risperidon.
d Extrapiramidale stoornissen kunnen optreden: Parkinsonisme (speekselvloed, musculoskeletale stijfheid, parkinsonisme, kwijlen, tandradfenomeen, bradykinesie, hypokinesie, gemaskerd gelaat, gespannen spieren, akinesie, stijve nek, spierstijfheid, parkinsonachtige gang en abnormale glabella reflex, parkinsonachtige rusttremor), acathisie (acathisie, rusteloosheid, hyperkinesie en rusteloze-benensyndroom), tremor, dyskinesie (dyskinesie, spiertrekkingen, choreoathetose, athetose en myoclonus), dystonie. Dystonie omvat dystonie, hypertonie, torticollis, onwillekeurige spierbewegingen, spiercontracties, blefarospasme, oculogyratie, verlamde tong, gezichtsspasme, laryngospasme, myotonie, opisthotonus, orofaryngeaal spasme, pleurothotonus, tongspasme en kaakklem. Het dient te worden opgemerkt dat een breder spectrum van symptomen is opgenomen, dat niet noodzakelijkerwijs een extrapiramidale oorzaak heeft. Insomnia omvat initiële insomnia, doorslaapstoornis. Convulsie omvat grand mal convulsie. Menstruatiestoornis omvat onregelmatige menstruatie, oligomenorroe. Oedeem omvat gegeneraliseerd oedeem, perifeer oedeem, putjesoedeem.
Bijwerkingen gezien bij formuleringen op basis van paliperidon
Aangezien paliperidon de actieve metaboliet is van risperidon zijn de bijwerkingenprofielen van deze stoffen (waaronder zowel de orale als de injectieformuleringen) relevant voor elkaar. Naast de bovengenoemde bijwerkingen werd de volgende bijwerking waargenomen bij het gebruik van producten op basis van paliperidon en kan verwacht worden dat deze ook optreedt bij RISPERDAL CONSTA.
Hartaandoeningen
Postureel orthostatisch tachycardiesyndroom
Anafylactische reactie
Bij patiënten die eerder oraal risperidon konden verdragen, zijn er tijdens postmarketingervaring zeldzame gevallen van anafylactische reactie gemeld na injectie met RISPERDAL CONSTA (zie rubriek 4.4).
Klasse-effecten
Net als bij andere antipsychotica, zijn er tijdens de postmarketingfase bij risperidon zeer zelden gevallen van QT-verlenging gemeld. Andere klassegerelateerde effecten op het hart die zijn gemeld bij antipsychotica die een verlengde QT-tijd vertonen, zijn ventrikelaritmie, ventrikelfibrilleren, ventrikeltachycardie, plotse dood, hartstilstand en Torsades de Pointes.
Veneuze trombo-embolie
Er zijn bij gebruik van antipsychotica gevallen van veneuze trombo-embolie gemeld, waaronder gevallen van longembolie en diepe veneuze trombose. Frequentie niet bekend.
Gewichtstoename
In de dubbelblinde, placebogecontroleerde studie van 12 weken, ervaarde 9% van de patiënten behandeld met RISPERDAL CONSTA een gewichtstoename van 7% van het lichaamsgewicht op het eindpunt, in vergelijking met 6% van de patiënten behandeld met placebo. In de open-label studie van 1 jaar met RISPERDAL CONSTA bleven de veranderingen in lichaamsgewicht bij individuele patiënten over het algemeen binnen 7% van baseline; 25% van de patiënten had een gewichtstoename van 7%.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via
het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Janssen-Cilag NV
Antwerpseweg 15-17
B-2340 Beerse
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
RISPERDAL CONSTA 25 mg: BE 254597
RISPERDAL CONSTA 37,5 mg: BE 254606
RISPERDAL CONSTA 50 mg: BE 254615
10. DATUM VAN HERZIENING VAN DE TEKST
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 2093797 | RISPERDAL CONSTA 50,0 MG FL IM 1X50,0MG/2ML+SOLV | N05AX08 | € 89 | - | Ja | € 12,8 | € 8,5 |
| 2093805 | RISPERDAL CONSTA 37,5 MG FL IM 1X37,5MG/2ML+SOLV | N05AX08 | € 76,8 | - | Ja | € 12,8 | € 8,5 |
| 2093813 | RISPERDAL CONSTA 25,0 MG FL IM 1X25,0MG/2ML+SOLV | N05AX08 | € 58,93 | - | Ja | € 12,8 | € 8,5 |



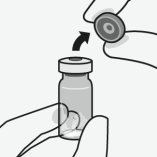

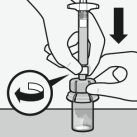
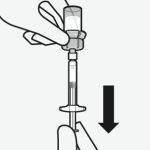
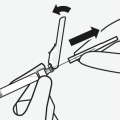
 Sluit de injectieflaconadapter aan op de injectieflacon
Sluit de injectieflaconadapter aan op de injectieflacon 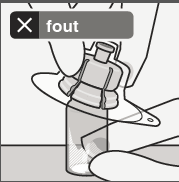
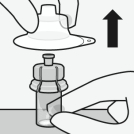


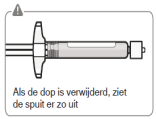
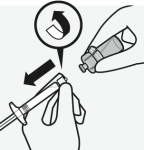
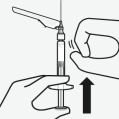
 Verwijder de dop
Verwijder de dop