SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Kyleena 19,5 mg afleveringsysteem voor intra-uterien gebruik
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Het afleveringsysteem voor intra-uterien gebruik bevat 19,5 mg levonorgestrel.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
Voor details van de afgiftesnelheid, zie rubriek 5.2.
3. FARMACEUTISCHE VORM
Afleveringsysteem voor intra-uterien gebruik (IUS).
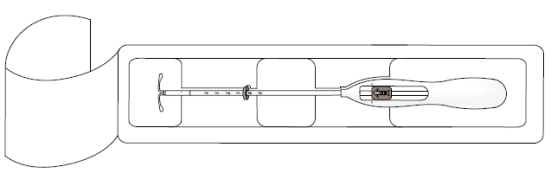
Het product bestaat uit een witte of nagenoeg witte geneesmiddelkern, bedekt met een half ondoorzichtig membraan, die op de verticale stam van een T-lichaam is bevestigd. Bovendien bevat de verticale stam een zilveren ring die zich dicht bij de horizontale armen bevindt. Het witte T-lichaam heeft een lus aan één uiteinde van de verticale stam en twee horizontale armen aan het andere uiteinde. Aan de lus zijn blauwe draden bevestigd om het systeem te verwijderen. De verticale stam van het IUS wordt in de inbrengbuis op de tip van de applicator geplaatst. De applicator bestaat uit een handvat en een glijder met een ring, slot, voorgebogen insertiebuis en plunjer. De draden om het IUS te verwijderen zitten in de insertiebuis en het handvat.
Afmetingen van Kyleena: 28 x 30 x 1,55 mm
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Anticonceptie voor maximaal 5 jaar.
4.2 Dosering en wijze van toediening
Dosering
Kyleena wordt in de uterusholte geplaatst en blijft gedurende maximaal 5 jaar werkzaam.
Inbrengen
Het wordt aanbevolen dat Kyleena uitsluitend wordt ingebracht door zorgverleners die ervaring hebben met het inbrengen van IUS’en en/of een training hebben gevolgd voor de procedure van het inbrengen van Kyleena.
Vóór het inbrengen moet de patiënt zorgvuldig zijn onderzocht om eventuele contra-indicaties voor het inbrengen van een IUS te detecteren. Sluit zwangerschap uit vóór het inbrengen. Overweeg de mogelijkheid van ovulatie en bevruchting voordat u dit product gebruikt. Kyleena is niet geschikt voor gebruik als postcoïtaal anticonceptiemiddel (zie rubriek 4.3 en rubriek 4.4 onder ‘Medisch onderzoek/consultatie’).
Tabel 1: Wanneer Kyleena inbrengen bij vrouwen in de vruchtbare leeftijd
Starten met Kyleena |
|
Postpartum insertie | In aanvulling op de bovenstaande instructies (Starten met Kyleena): Postpartum-inserties moeten worden uitgesteld tot de baarmoeder volledig is geïnvolueerd, maar mogen niet eerder dan 6 weken na de bevalling worden uitgevoerd. Als de involutie aanzienlijk is vertraagd, overweeg dan om te wachten tot 12 weken na de bevalling. |
Insertie na abortus in het eerste trimester | Kyleena kan direct na een abortus in het eerste trimester worden ingebracht. In dit geval is er geen aanvullende anticonceptie nodig. |
Kyleena vervangen | Kyleena kan op elk moment in de menstruatiecyclus worden vervangen door een nieuw systeem. In dit geval is er geen aanvullende anticonceptie nodig. |
Overstappen van een andere anticonceptiemethode (bijv. gecombineerde hormonale anticonceptiva, implantaat) |
|
Belangrijke informatie om te overwegen tijdens of na het inbrengen
In het geval dat het inbrengen moeilijk is en/of in geval van uitzonderlijke pijn of bloeding tijdens of na het inbrengen, moet de mogelijkheid van perforatie overwogen worden en dienen gepaste stappen te worden ondernomen, zoals lichamelijk onderzoek en echografie.
Na de insertie moeten vrouwen na 4 tot 6 weken opnieuw worden onderzocht om de verwijderingsdraden te controleren en ervoor te zorgen dat het IUS in de juiste positie zit. Enkel een lichamelijk onderzoek (inclusief het controleren van de draadjes) is mogelijk niet voldoende om een gedeeltelijke perforatie uit te sluiten en echografie kan worden overwogen (zie rubriek 4.4).
Kyleena is te onderscheiden van andere IUS’en door de combinatie van een zilveren ring die zichtbaar is op echografie en de blauwe kleur van de draden. Het T-vormige frame van Kyleena bevat bariumsulfaat, waardoor het zichtbaar is bij röntgenonderzoek.
Verwijderen/vervangen
Kyleena wordt verwijderd door voorzichtig met een forceps aan de draden te trekken. Het gebruik van excessieve kracht/scherpe instrumenten tijdens het verwijderen van Kyleena kan breuk van het spiraaltje veroorzaken. Na het verwijderen van Kyleena moet het systeem gecontroleerd worden om na te gaan of het intact is en of het in zijn geheel is verwijderd. Als de draden niet zichtbaar zijn, bepaal dan de locatie van het systeem via echografie of een andere methode. Indien het systeem in de uterusholte aanwezig is, kan het met een smalle forceps worden verwijderd. Hiervoor kan dilatatie van het cervixkanaal of een andere chirurgische ingreep nodig zijn.
Het systeem moet uiterlijk aan het einde van het vijfde jaar worden verwijderd.
Voortzetten van anticonceptie na het verwijderen
- Als de vrouw dezelfde methode wil blijven gebruiken, kan direct na het verwijderen van het oorspronkelijke systeem een nieuw systeem worden geplaatst.
- Als de vrouw niet dezelfde methode wil blijven gebruiken maar zwangerschap niet gewenst is, dient het verwijderen binnen 7 dagen na het begin van de menstruatie te gebeuren, als de vrouw nog regelmatig menstrueert. Als het systeem op een ander moment tijdens de cyclus wordt verwijderd of als de vrouw geen regelmatige menstruatie meer heeft en de vrouw in de voorafgaande week geslachtsgemeenschap heeft gehad, bestaat er een kans dat zij zwanger wordt. Om continue contraceptie te verzekeren, moet een barrière-anticonceptiemethode worden gebruikt (zoals condooms) vanaf ten minste 7 dagen vóór de verwijdering. Na verwijdering moet de nieuwe anticonceptiemethode onmiddellijk worden gestart (volg de instructies voor gebruik van de nieuwe anticonceptiemethode).
Oudere patiënten
Kyleena is niet toegewezen voor gebruik bij postmenopauzale vrouwen.
Patiënten met leverfunctiestoornis
Kyleena is niet onderzocht bij vrouwen met een leverfunctiestoornis. Kyleena is gecontra-indiceerd bij vrouwen met acute leverziekte of levertumor (zie rubriek 4.3).
Patiënten met nierfunctiestoornis
Kyleena is niet onderzocht bij vrouwen met een nierfunctiestoornis.
Pediatrische patiënten
Het gebruik van dit product vóór de menarche is niet geïndiceerd. Voor gegevens over veiligheid en effectiviteit in adolescenten, zie rubriek 5.1.
Wijze van toediening
Moet door een zorgverlener worden ingebracht, met gebruik van aseptische techniek.
Kyleena wordt geleverd in een steriele verpakking met een geïntegreerde applicator dat met één hand kan worden geladen. De verpakking mag niet worden geopend voordat dit nodig is voor het inbrengen. Niet opnieuw steriliseren. Kyleena is, zoals het geleverd wordt, uitsluitend voor eenmalig gebruik. Niet gebruiken als de blisterverpakking beschadigd of open is. Niet inbrengen na de vervaldatum die staat vermeld op de doos en de blister na EXP.
Al het ongebruikte geneesmiddel of afvalmateriaal dient te worden vernietigd overeenkomstig lokale voorschriften.
Kyleena wordt aangeleverd met een herinneringskaart voor de patiënte in de buitenverpakking. Vul deze herinneringskaart in en geef het na het inbrengen aan de patiënte.
Voorbereiding voor het inbrengen
- Onderzoek de patiënte om contra-indicaties voor plaatsing van Kyleena uit te sluiten (zie rubriek 4.3 en rubriek 4.4 onder ‘Medisch onderzoek/consultatie’).
- Breng een speculum in, maak de cervix zichtbaar en reinig de cervix en vagina vervolgens grondig met een geschikte antiseptische oplossing.
- Laat u indien nodig assisteren.
- Grijp de voorste lip van de cervix vast met een tenaculum of een andere forceps om de baarmoeder te stabiliseren. Als de baarmoeder in retroversie ligt, kan het beter zijn om de achterste lip van de cervix te grijpen. Om het cervixkanaal recht te krijgen, kunt u voorzichtig aan de forceps trekken. De forceps moet op zijn plaats blijven en tijdens de insertieprocedure moet voorzichtige tegendruk worden uitgeoefend op de cervix.
- Steek een uterussonde via het cervicale kanaal tot in de fundus om de diepte te meten, om de richting van de baarmoederholte te bevestigen en om intra-uteriene afwijkingen op te sporen (bv. septum, submucosale fibromen) of een vroeger spiraaltje dat niet werd verwijderd. Als u moeilijkheden ondervindt, moet worden overwogen om het kanaal te dilateren. Als dilatatie van de cervix vereist is, kunt u pijnstillers en/of een paracervicaal blok gebruiken.
Het inbrengen
| |
|
|
| |
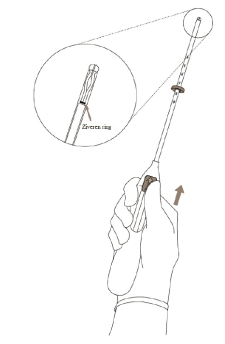
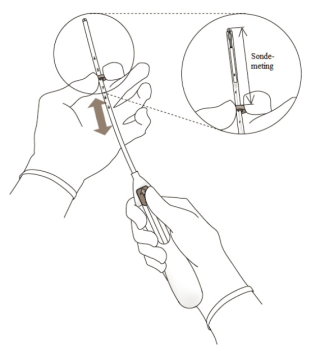
3. Hou de glijder in de verste positie, plaats de bovenrand van de ring op het niveau die overeenstemt met de gesondeerde meting van de diepte van de baarmoeder (afbeelding 3). |
|
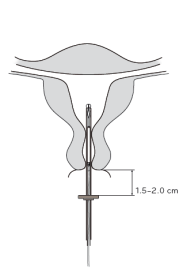
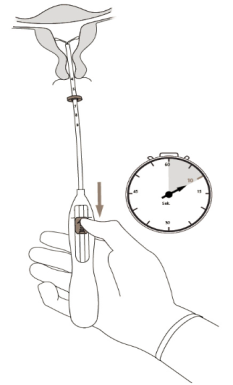
4. Terwijl u de glijder in de verste positie houdt, steekt u het insertiebuisje door de cervix tot de ring ongeveer 1,5-2,0 cm van de baarmoederhals verwijderd is (afbeelding 4). |
|
| |
|
|
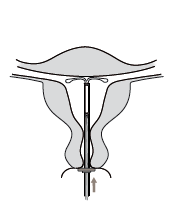
6. Duw het insertiebuisje voorzichtig naar de baarmoederfundus tot de ring tegen de cervix komt. Kyleena zit nu in de fundus (afbeelding 6). |
|
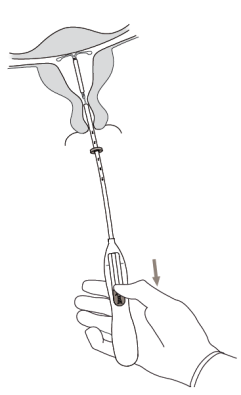
7. Hou het insertiebuisje op zijn plaats en plaats Kyleena door de glijder helemaal naar beneden te trekken (afbeelding 7). Terwijl de glijder de hele tijd naar beneden gehouden wordt, trekt u het insertiebuisje voorzichtig naar buiten. Knip de draden door zodat er ongeveer 2-3 cm draad buiten de cervix te zien is. |
|
| |
Verwijderen/vervangen
Zie voor verwijderen/vervangen rubriek 4.2 Inbrengen en verwijderen/vervangen
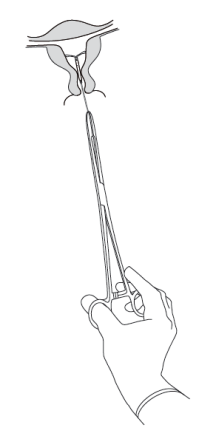
Kyleena wordt verwijderd door voorzichtig met een forceps aan de draden te trekken (afbeelding 8). |
|
4.3 Contra-indicaties
- Zwangerschap (zie rubriek 4.6);
- Acute of terugkerende PID (pelvic inflammatory disease) of aandoeningen die geassocieerd zijn met een verhoogde kans op bekkeninfecties;
- Acute cervicitis of vaginitis;
- Postpartum-endometritis of geïnfecteerde abortus in de afgelopen drie maanden;
- Cervicale intra-epitheliale neoplasie, tot genezing;
- Uteriene of cervicale maligniteit;
- Progestageengevoelige tumoren, bijv. borstkanker;
- Ongewone uteriene bloeding van onbekende etiologie;
- Congenitale of verworven uteriene anomalie, waaronder fibroïden die het inbrengen en / of vasthouden van het intra-uteriene systeem zouden belemmeren (bijv. als zij de uterusholte vervormen);
- Acute leverziekte of levertumor;
- Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
Bij de meeste vrouwen verandert het menstruatiebloedingspatroon na het inbrengen van Kyleena. In de loop van de tijd wordt de frequentie van amenorroe en soms optredende bloedingen hoger en de frequentie van verlengde, onregelmatige en vaak optredende bloedingen lager. De volgende bloedingspatronen werden in klinisch onderzoek waargenomen:
Tabel 3: Bloedingspatronen die in klinisch onderzoek met Kyleena zijn gemeld
Kyleena | Eerste 90 dagen | Tweede 90 dagen | Einde jaar 1 | Einde jaar 3 | Einde jaar 5 |
Amenorroe | < 1% | 5% | 12% | 20% | 23% |
Soms optredende bloedingen | 10% | 20% | 26% | 26% | 26% |
Vaak optredende bloedingen | 25% | 10% | 4% | 2% | 2% |
Verlengde bloedingen* | 57% | 14% | 6% | 2% | 1% |
Onregelmatige bloedingen | 43% | 25% | 17% | 10% | 9% |
*Proefpersonen met verlengde bloedingen kunnen ook in één van de andere categorieën zijn meegeteld (behalve amenorroe)
Bijwerkingen weergegeven in tabelvorm
De frequenties van de bijwerkingen die met Kyleena zijn gerapporteerd worden samengevat in de onderstaande tabel. Binnen elke frequentiegroep zijn de bijwerkingen gerangschikt naar afnemende ernst. De frequenties worden als volgt gedefinieerd:
Zeer vaak (≥ 1/10),
Vaak (≥ 1/100, < 1/10),
Soms (≥ 1/1.000, < 1/100),
Zelden (≥ 1/10.000, < 1/1.000),
Zeer zelden (< 1/10.000).
Systeem/orgaanklasse | Zeer vaak | Vaak | Soms | Zelden |
Psychische stoornissen |
| Depressieve stemming/ depressie |
|
|
Zenuwstelselaandoeningen | Hoofdpijn | Migraine |
|
|
Vasculaire aandoeningen |
| Duizeligheid |
|
|
Maagdarmstelsel-aandoeningen | Buikpijn/bekkenpijn | Nausea |
|
|
Huid- en onderhuidaandoeningen | Acne/seborroe | Alopecia | Hirsutisme |
|
Voortplantingsstelsel- en borstaandoeningen | Veranderingen in bloedingen, waaronder meer of minder menstruatiebloedingen, spotting, soms optredende bloedingen en amenorroe | Infectie van het bovenste deel van het geboortekanaal | Uteriene perforatie |
|
Onderzoeken |
| Gewichtstoename |
|
|
* In klinisch onderzoek moesten ovariumcysten als bijwerking worden gerapporteerd wanneer er sprake was van ongewone, niet-functionele cysten en/ of cysten met een diameter > 3 cm op basis van ultrageluidonderzoek.
** Deze frequentie is gebaseerd op een grote, prospectieve, vergelijkende niet-interventionele cohortstudie bij vrouwen die een ander levonorgestrel-IUS of een koper-IUD gebruikten, welke toonde dat borstvoeding op het moment van insertie en insertie tot en met 36 weken na de bevalling onafhankelijke risicofactoren zijn voor perforatie (zie rubriek 4.4 onder Perforatie). In klinische studies met Kyleena waarin vrouwen die borstvoeding gaven, uitsloten werden, was de frequentie van perforatie “Zelden”.
Beschrijving van geselecteerde bijwerkingen
Bij gebruik van een levonorgestrel‑IUD zijn gevallen van overgevoeligheid, waaronder huiduitslag, urticaria en angio-oedeem gerapporteerd.
Als een vrouw zwanger wordt terwijl zij Kyleena gebruikt, is de relatieve waarschijnlijkheid dat deze zwangerschap ectopisch is, verhoogd (zie rubriek 4.4 onder ‘Ectopische zwangerschap’).
De draadjes voor het verwijderen kunnen tijdens de geslachtsgemeenschap voelbaar zijn voor de partner.
De volgende bijwerkingen zijn gemeld in verband met de procedures voor het inbrengen of verwijderen van Kyleena:
Pijn tijdens de procedure, bloeding tijdens de procedure, vasovagale reactie met duizeligheid of syncope in verband met het inbrengen. Door de ingreep kan een patiënte met epilepsie eerder een aanval krijgen.
Gevallen van sepsis (waaronder groep A-streptokokkensepsis) zijn gerapporteerd na IUD-insertie (zie rubriek 4.4 onder Bekkeninfectie).
Pediatrische patiënten
Het veiligheidsprofiel van Kyleena zal naar verwachting hetzelfde zijn bij adolescenten jonger dan 18 jaar als bij gebruiksters van 18 jaar en ouder. Voor gegevens over de veiligheid bij adolescenten, zie rubriek 5.1.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Bayer SA-NV
Kouterveldstraat 7A 301
B-1831 Diegem (Machelen)
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
BE502000
10. DATUM VAN HERZIENING VAN DE TEKST
Goedkeuringsdatum: 11/2025
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3521002 | KYLEENA 19,5MG SYSTEEM INTRA-UTERIEN 1 | G02BA03 | € 147,57 | - | Ja | - | - |