SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Olumiant 1 mg filmomhulde tabletten
Olumiant 2 mg filmomhulde tabletten
Olumiant 4 mg filmomhulde tabletten
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Olumiant 1 mg filmomhulde tabletten
Elke filmomhulde tablet bevat 1 mg baricitinib.
Olumiant 2 mg filmomhulde tabletten
Elke filmomhulde tablet bevat 2 mg baricitinib.
Olumiant 4 mg filmomhulde tabletten
Elke filmomhulde tablet bevat 4 mg baricitinib.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Filmomhulde tablet (tablet)
Olumiant 1 mg filmomhulde tabletten
Zeer lichtroze, 6,75 mm ronde tabletten, met aan de ene zijde ingeslagen “Lilly” en aan de andere zijde “1”.
Olumiant 2 mg filmomhulde tabletten
Lichtroze, 9 x 7,5 mm langwerpige tabletten, met aan de ene zijde ingeslagen “Lilly” en aan de andere zijde “2”.
Olumiant 4 mg filmomhulde tabletten
Medium roze, 8,5 mm ronde tabletten, met aan de ene zijde ingeslagen “Lilly” en aan de andere zijde “4”.
De tabletten hebben aan beide zijden een uitholling.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Reumatoïde artritis
Baricitinib is geïndiceerd voor gebruik bij volwassen patiënten die onvoldoende hebben gereageerd op één of meer disease‑modifying anti‑rheumatic drugs (DMARD’s) of daar intolerant voor zijn voor de behandeling van matige tot ernstige reumatoïde artritis. Baricitinib kan worden gebruikt als monotherapie of in combinatie met methotrexaat (zie rubriek 4.4, 4.5 en 5.1 voor de beschikbare gegevens over andere combinaties).
Atopische dermatitis
Baricitinib is geïndiceerd voor de behandeling van matige tot ernstige atopische dermatitis bij volwassen en pediatrische patiënten van 2 jaar en ouder die in aanmerking komen voor systemische therapie.
Alopecia areata
Baricitinib is geïndiceerd voor de behandeling van ernstige alopecia areata bij volwassen en adolescente patiënten van 12 jaar en ouder (zie rubriek 5.1).
Juveniele idiopathische artritis
Baricitinib is geïndiceerd voor de behandeling van actieve juveniele idiopathische artritis bij patiënten van 2 jaar en ouder die onvoldoende hadden gereageerd op of intolerantie hebben gehad voor een of meer eerdere conventionele synthetische of biologische DMARD's:
- polyarticulaire juveniele idiopathische artritis (polyarticulaire reumafactor positief [RF+] of negatief [RF-], uitgebreid oligoarticulair),
- enthesitis-gerelateerde artritis, en
- juveniele artritis psoriatica.
Baricitinib kan worden gebruikt als monotherapie of in combinatie met methotrexaat.
4.2 Dosering en wijze van toediening
De behandeling moet worden ingesteld door artsen met ervaring in de diagnostiek en behandeling van de aandoeningen waarvoor dit geneesmiddel is geïndiceerd.
Dosering
Reumatoïde artritis
De aanbevolen dosering baricitinib is 4 mg eenmaal daags. Een dosering van 2 mg eenmaal daags wordt aanbevolen voor patiënten met een hoger risico op veneuze trombo-embolie (VTE), ernstige ongewenste cardiovasculaire voorvallen (MACE) en maligniteiten, voor patiënten > 65 jaar en voor patiënten met een voorgeschiedenis van chronische of recidiverende infecties (zie rubriek 4.4). Een dosering van 4 mg eenmaal daags kan worden overwogen voor patiënten bij wie de ziekteactiviteit onvoldoende onder controle is met een dosering van 2 mg eenmaal daags. Een dosering van 2 mg eenmaal daags moet worden overwogen voor patiënten bij wie de ziekteactiviteit met 4 mg eenmaal daags stabiel onder controle is gekomen en die in aanmerking komen voor een verlaging van de dosering (zie rubriek 5.1).
Atopische dermatitis
Volwassenen
De aanbevolen dosering baricitinib is 4 mg eenmaal daags. Een dosering van 2 mg eenmaal daags wordt aanbevolen voor patiënten met een hoger risico op VTE, MACE en maligniteiten, voor patiënten ≥ 65 jaar en voor patiënten met een voorgeschiedenis van chronische of recidiverende infecties (zie rubriek 4.4). Een dosering van 4 mg eenmaal daags kan worden overwogen voor patiënten bij wie de ziekteactiviteit onvoldoende onder controle is met een dosering van 2 mg eenmaal daags. Een dosering van 2 mg eenmaal daags moet worden overwogen voor patiënten bij wie de ziekteactiviteit met 4 mg eenmaal daags stabiel onder controle is gekomen en die in aanmerking komen voor een verlaging van de dosering (zie rubriek 5.1).
Baricitinib kan worden gebruikt met of zonder topicale corticosteroïden. De werkzaamheid van baricitinib kan worden verhoogd als het gegeven wordt met topicale corticosteroïden (zie rubriek 5.1). Topicale calcineurineremmers kunnen worden gebruikt maar dienen te worden voorbehouden voor alleen de gevoelige gebieden, zoals het gezicht, de nek, intertrigineuze en genitale gebieden.
Stoppen met de behandeling moet worden overwogen bij patiënten die na 8 weken behandeling geen tekenen van therapeutisch voordeel hebben laten zien.
Kinderen en adolescenten (van 2 jaar en ouder)
De aanbevolen dosering baricitinib is 4 mg eenmaal daags voor patiënten die 30 kg of meer wegen. Voor patiënten die tussen 10 kg en 30 kg wegen, is de aanbevolen dosering 2 mg eenmaal daags. Een verlaging tot de helft van de dosering moet worden overwogen voor patiënten bij wie de ziekteactiviteit met de aanbevolen dosering stabiel onder controle is gekomen en die in aanmerking komen voor een verlaging van de dosering.
Baricitinib kan worden gebruikt met of zonder topicale corticosteroïden. Topicale calcineurineremmers kunnen worden gebruikt maar dienen te worden voorbehouden voor alleen de gevoelige gebieden, zoals het gezicht, de nek, intertrigineuze en genitale gebieden.
Stoppen met de behandeling moet worden overwogen bij patiënten die na 8 weken behandeling geen tekenen van therapeutisch voordeel hebben laten zien.
Alopecia areata
Volwassenen
De aanbevolen dosering baricitinib is 4 mg eenmaal daags. Een dosering van 2 mg eenmaal daags wordt aanbevolen voor patiënten met een hoger risico op VTE, MACE en maligniteiten, voor patiënten ≥ 65 jaar en voor patiënten met een voorgeschiedenis van chronische of terugkerende infecties (zie rubriek 4.4). Een dosering van 4 mg eenmaal daags kan worden overwogen voor patiënten bij wie de ziekteactiviteit onvoldoende onder controle is met een dosering van 2 mg eenmaal daags. Een dosering van 2 mg eenmaal daags moet worden overwogen voor patiënten bij wie de ziekteactiviteit met 4 mg eenmaal daags stabiel onder controle is gekomen en die in aanmerking komen voor een verlaging van de dosering (zie rubriek 5.1).
Zodra een stabiele respons is bereikt, wordt het aanbevolen de behandeling gedurende ten minste enkele maanden voort te zetten om terugval te voorkomen. De baten-risicoverhouding van de behandeling moet met regelmatige tussenpozen op individuele basis opnieuw worden beoordeeld.
Stoppen met de behandeling moet worden overwogen bij patiënten die na 36 weken behandeling geen tekenen van therapeutisch voordeel hebben laten zien.
Adolescenten (12 jaar en ouder)
De aanbevolen dosering baricitinib is 4 mg eenmaal daags voor patiënten die 30 kg of meer wegen. Zie rubriek 4.2 Pediatrische patiënten hieronder voor informatie over patiënten die minder dan 30 kg wegen. Een dosering van 2 mg eenmaal daags moet worden overwogen voor patiënten bij wie de ziekteactiviteit met 4 mg eenmaal daags stabiel onder controle is gekomen en die in aanmerking komen voor een verlaging van de dosering.
Zodra een stabiele respons is bereikt, wordt het aanbevolen de behandeling gedurende ten minste enkele maanden voort te zetten om terugval te voorkomen. De baten-risicoverhouding van de behandeling moet met regelmatige tussenpozen op individuele basis opnieuw worden beoordeeld.
Stoppen met de behandeling moet worden overwogen bij patiënten die na 36 weken behandeling geen tekenen van therapeutisch voordeel hebben laten zien.
Juveniele idiopathische artritis (van 2 tot 18 jaar)
De aanbevolen dosering baricitinib is 4 mg eenmaal daags voor patiënten die 30 kg of meer wegen. Voor patiënten die tussen 10 kg en 30 kg wegen, is de aanbevolen dosering 2 mg eenmaal daags.
Bij patiënten bij wie na 12 weken behandeling geen bewijs van therapeutisch voordeel wordt vastgesteld, dient te worden overwogen om de behandeling te staken.
Start van de behandeling
De behandeling moet niet worden gestart bij patiënten met een absolute lymfocytentelling (ALC) van minder dan 0,5 x 109 cellen/l, een absolute neutrofielentelling (ANC) van minder dan 1 x 109 cellen/l of met een hemoglobinewaarde van minder dan 5 mmol/l. De behandeling kan worden ingesteld zodra de waarden tot boven deze limieten hersteld zijn (zie rubriek 4.4).
Dosisverlaging
Bij patiënten die sterke organische aniontransporter 3 (OAT3)-remmers gebruiken, zoals probenecide, of met een creatinineklaring tussen 30 en 60 ml/min, moet de aanbevolen dosering voor pediatrische patiënten worden gehalveerd en is de aanbevolen dosering voor volwassen patiënten 2 mg (zie rubriek 4.5).
Speciale patiëntengroepen
Nierfunctiestoornissen
De aanbevolen dosering is 2 mg eenmaal daags bij volwassen patiënten met een creatinineklaring tussen 30 en 60 ml/min. Bij pediatrische patiënten met een creatinineklaring tussen 30 en 60 ml/min dient de aanbevolen dosering baricitinib te worden gehalveerd. Baricitinib wordt niet aanbevolen voor gebruik bij patiënten met een creatinineklaring < 30 ml/min (zie rubriek 5.2).
Leverfunctiestoornissen
Bij patiënten met een lichte tot matige leverfunctiestoornis hoeft de dosering niet te worden aangepast. Baricitinib wordt niet aanbevolen voor gebruik bij patiënten met een ernstige leverfunctiestoornis (zie rubriek 5.2).
Ouderen
De klinische ervaring bij patiënten > 75 jaar is zeer beperkt.
Pediatrische patiënten
De veiligheid en werkzaamheid van baricitinib bij kinderen jonger dan 2 jaar met atopische dermatitis en juveniele idiopathische artritis zijn nog niet vastgesteld. Er zijn geen gegevens beschikbaar. Zie rubriek 4.2 hierboven voor informatie over de dosering bij kinderen van 2 jaar en ouder.
De veiligheid en werkzaamheid van baricitinib bij kinderen jonger dan 12 jaar of die < 30 kg wegen met alopecia areata zijn nog niet vastgesteld. Er zijn geen gegevens beschikbaar. Zie rubriek 4.2 hierboven voor informatie over de dosering bij adolescenten van 12 jaar en ouder en met een gewicht van 30 kg of meer.
Voor pediatrische patiënten die geen tabletten kunnen doorslikken, kunnen de tabletten vóór toediening in water worden gedispergeerd (zie 'Alternatieve toediening voor kinderen' hieronder). Als alternatief kan een suspensie voor oraal gebruik worden gebruikt, indien beschikbaar.
Wijze van toediening
Voor oraal gebruik.
Baricitinib wordt eenmaal daags met of zonder voedsel ingenomen en kan op elk moment van de dag worden ingenomen.
Alternatieve toediening voor kinderen
Bij pediatrische patiënten die niet in staat zijn hele tabletten door te slikken, kan worden overwogen de tabletten in water te dispergeren. Er mag alleen water worden gebruikt om de tablet te dispergeren. Alleen het aantal tabletten dat nodig is voor de dosis mag worden gedispergeerd.
Als om welke reden dan ook niet de hele suspensie is toegediend, niet nog een tablet dispergeren en toedienen, maar wachten tot de volgende geplande dosis.
Voor instructies over het dispergeren van het geneesmiddel vóór toediening, zie rubriek 6.6.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
Zwangerschap (zie rubriek 4.6).
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De vaakst gemelde bijwerkingen met baricitinib zijn verhoogd LDL-cholesterol (26,0%), bovensteluchtweginfecties (16,9%), hoofdpijn (5,2%), herpes simplex (3,2%) en urineweginfecties (2,9%). Ernstige longontsteking (0,2%) en ernstige herpes zoster (0,2%) kwamen soms voor bij patiënten met reumatoïde artritis.
Tabel met bijwerkingen
Geschatte frequentie: zeer vaak (≥ 1/10), vaak (≥ 1/100, < 1/10), soms (≥ 1/1.000, < 1/100), zelden (≥ 1/10.000, < 1/1.000), zeer zelden (< 1/10.000). De frequenties in tabel 2 zijn gebaseerd op samengevoegde gegevens van klinische onderzoeken bij volwassenen en/of van na het in de handel brengen binnen de indicaties reumatoïde artritis, atopische dermatitis en alopecia areata, tenzij anders vermeld. Wanneer er opmerkelijke verschillen tussen de verschillende indicaties zijn waargenomen, wordt dit toegelicht in de voetnoten onder de tabel. Binnen elke frequentiegroep worden bijwerkingen weergegeven in de volgorde van afnemende ernst.
Tabel 2. Bijwerkingen
Systeem/ orgaanklasse | Zeer vaak | Vaak | Soms |
Infecties en parasitaire aandoeningen | Bovensteluchtweg-infecties | Pneumonied |
|
Bloed- en lymfestelsel-aandoeningen |
| Trombocytose > 600 x 109 cellen/la, d | Neutropenie < 1 x 109 cellen/la |
Immuunsysteem- aandoeningen |
|
| Opzwellen van het gezicht Urticaria |
Voedings- en stofwisselingsstoornissen | Hypercholesterolemiea |
| Hypertriglyceridemiea |
Zenuwstelsel-aandoeningen |
| Hoofdpijn |
|
Bloedvataandoeningen |
|
| Diepe veneuze tromboseb |
Ademhalingsstelsel-, |
|
| Longembolief |
Maagdarmstelsel-aandoeningen |
| Buikpijnd Misselijkheidd | Diverticulitis |
Lever- en galaandoeningen |
| ALAT verhoogd ≥ 3 x ULNa, d | ASAT verhoogd ≥ 3 x ULNa, e |
Huid- en onderhuid-aandoeningen |
| Rash |
|
Onderzoeken |
| Verhoogd creatinekinase > 5 x ULNa, c | Gewichtstoename |
a Omvat bij laboratoriummonitoring gedetecteerde veranderingen (zie tekst hieronder).
b De frequentie van herpes zoster en diepe veneuze trombose is gebaseerd op de klinische onderzoeken bij reumatoïde artritis.
c In klinische onderzoeken bij reumatoïde artritis kwamen acne en verhoogd creatinekinase > 5 x ULN soms voor.
d In klinische onderzoeken bij atopische dermatitis kwamen misselijkheid en ALAT ≥ 3 x ULN soms voor. In klinische onderzoeken bij alopecia areata kwam buikpijn soms voor. In klinische onderzoeken bij atopische dermatitis en alopecia areata kwamen longontsteking en trombocytose > 600 x 109 cellen/l soms voor.
e In klinische onderzoeken bij alopecia areata kwam ASAT ≥ 3 x ULN vaak voor.
f De frequentie van longembolie is gebaseerd op de klinische onderzoeken bij reumatoïde artritis en atopische dermatitis.
g Folliculitis werd waargenomen in klinische onderzoeken bij alopecia areata. Dit was meestal gelokaliseerd op de hoofdhuid waar hernieuwde haargroei optrad.
Beschrijving van geselecteerde bijwerkingen
Maagdarmstelselaandoeningen
In klinische onderzoeken bij reumatoïde artritis was de frequentie van misselijkheid tot en met week 52 met de combinatiebehandeling van methotrexaat en baricitinib bij behandelingsnaïeve patiënten hoger (9,3%) dan voor methotrexaat alleen (6,2%) of baricitinib alleen (4,4%). In de samengevoegde gegevens van klinische onderzoeken bij reumatoïde artritis, atopische dermatitis en alopecia areata kwam misselijkheid het vaakst voor tijdens de eerste 2 behandelingsweken.
Gevallen van buikpijn waren gewoonlijk licht, voorbijgaand, hielden geen verband met infectieuze of inflammatoire aandoeningen van het maagdarmstelsel en leidden niet tot onderbreking van de behandeling.
Infecties
In de samengevoegde gegevens van klinische onderzoeken bij reumatoïde artritis, atopische dermatitis en alopecia areata waren de meeste infecties licht tot matig van ernst. In onderzoeken met beide doseringen, werden infecties gemeld bij respectievelijk 31,0%, 25,7% en 26,7% van de patiënten in de 4 mg-, 2 mg- en placebogroep. In klinische onderzoeken bij reumatoïde artritis leidde de combinatie met methotrexaat tot een verhoogd aantal infecties in vergelijking met monotherapie met baricitinib. Herpes zoster kwam bij reumatoïde artritis voor met een frequentie vaak, zeer zelden bij atopische dermatitis en soms bij alopecia areata. In klinische onderzoeken bij atopische dermatitis kwamen huidinfecties die een behandeling met antibiotica vereisten minder vaak voor bij baricitinib dan met placebo.
De incidentie van ernstige infecties met baricitinib was gelijk aan placebo. De incidentie van ernstige infecties bleef stabiel tijdens langetermijnblootstelling. De algehele incidentie van ernstige infecties in het klinische onderzoeksprogramma was 3,2 per 100 patiëntjaren bij reumatoïde artritis, 2,1 bij atopische dermatitis en 0,8 bij alopecia areata. Ernstige longontsteking en ernstige herpes zoster kwamen soms voor bij patiënten met reumatoïde artritis.
Verhogingen van de levertransaminasen
Dosisafhankelijke verhogingen van ALAT en ASAT in het bloed werden gemeld in studies die langer dan 16 weken duurden. Verhogingen in gemiddelde ALAT/ASAT bleven stabiel in de tijd. De meeste gevallen van verhogingen ≥ 3 x ULN van het hepatisch transaminase waren asymptomatisch en voorbijgaand.
Bij patiënten met reumatoïde artritis resulteerde de combinatie van baricitinib met potentieel hepatotoxische geneesmiddelen, zoals methotrexaat, in een toegenomen frequentie van deze verhogingen.
Lipidenverhogingen
In de samengevoegde gegevens van klinische onderzoeken bij reumatoïde artritis, atopische dermatitis en alopecia areata ging de behandeling met baricitinib gepaard met dosisafhankelijke verhogingen van de lipidenparameters waaronder totaal cholesterol, LDL-cholesterol en hoge dichtheid lipoproteïne (HDL)-cholesterol. Er was geen verandering in de LDL/HDL-ratio. Verhogingen werden waargenomen na 12 weken en bleven daarna stabiel op een hogere waarde dan baseline, ook in het langdurige verlengingsonderzoek bij reumatoïde artritis. Spiegels van gemiddeld totaal cholesterol en LDL-cholesterol namen toe tot en met week 52 bij patiënten met atopische dermatitis en alopecia areata. In klinische onderzoeken bij reumatoïde artritis werd de behandeling met baricitinib in verband gebracht met dosisafhankelijke toenames in triglyceriden. Er was geen toename in triglyceridenspiegels in klinische onderzoeken bij atopische dermatitis en alopecia areata.
Verhogingen van het LDL-cholesterol verminderden bij behandeling met een statine naar waarden van voor de behandeling.
Creatinekinase (CK)
Behandeling met baricitinib werd in verband gebracht met dosisafhankelijke toenames van CK. Gemiddeld CK was verhoogd in week 4 en bleef daarna op een hogere waarde dan op baseline. Bij alle indicaties waren de meeste gevallen van CK-verhogingen ˃ 5 x ULN van voorbijgaande aard en de behandeling hoefde niet te worden gestopt.
Er traden in de klinische onderzoeken geen bevestigde gevallen van rabdomyolyse op.
Neutropenie
Gemiddelde neutrofielentellingen namen af na 4 weken en bleven in de tijd stabiel op een lagere waarde dan baseline. Er was geen duidelijke relatie tussen neutropenie en het optreden van ernstige infecties. In klinische onderzoeken werd de behandeling echter onderbroken als de ANC < 1 x 109 cellen/l was.
Trombocytose
Dosisafhankelijke verhogingen in gemiddelde trombocytenaantallen werden waargenomen en bleven stabiel in de tijd, op een hogere waarde dan baseline.
Pediatrische patiënten
Juveniele idiopathische artritis
In totaal werden 220 patiënten van 2 tot 18 jaar blootgesteld aan een van de onderzochte doses baricitinib in het klinisch onderzoeksprogramma voor juveniele idiopathische artritis, wat neerkomt op een blootstelling van 326 patiëntjaren.
Bij pediatrische patiënten die werden behandeld met baricitinib in de placebogecontroleerde, dubbelblinde, gerandomiseerde ontwenningsperiode van het klinisch onderzoek naar juveniele idiopathische artritis (n=82), kwam hoofdpijn zeer vaak voor (11%), neutropenie < 1.000 cellen/mm3 kwam vaak voor (2,4%, één patiënt) en longembolie kwam vaak voor (1,2%, één patiënt).
Pediatrische atopische dermatitis
De veiligheidsbeoordeling bij kinderen en adolescenten is gebaseerd op de veiligheidsgegevens van de fase III-studie BREEZE-AD-PEDS waarin 466 patiënten tussen 2 en 18 jaar een dosis baricitinib hadden gekregen. Over het algemeen was het veiligheidsprofiel bij deze patiënten vergelijkbaar met hetgeen dat was waargenomen bij de volwassen populatie. Neutropenie (< 1 x 109 cellen/liter) kwam vaker voor (1,7%) vergeleken met volwassenen.
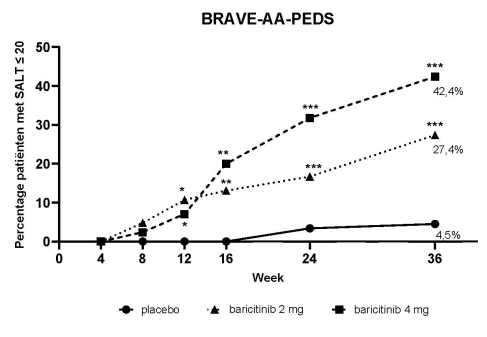
Adolescente alopecia areata
In totaal werden 245 patiënten van 12 tot 18 jaar blootgesteld aan een van de onderzochte doses baricitinib in de fase III-studie BRAVE-AA-PEDS. Van deze patiënten werden 85 patiënten behandeld met 4 mg in de placebogecontroleerde periode. Over het algemeen was het veiligheidsprofiel bij adolescente patiënten vergelijkbaar met het veiligheidsprofiel dat werd waargenomen bij de volwassen populatie. Acne (10,6%) en neutropenie (3,6%) (< 1 x 109 cellen/liter) kwamen vaker voor vergeleken met volwassenen.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten, www.fagg.be, Afdeling Vigilantie: Website: www.eenbijwerkingmelden.be, e-mail: adr@fagg-afmps.be.
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Eli Lilly Nederland B.V., Orteliuslaan 1000, 3528 BD Utrecht, Nederland.
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Olumiant 1 mg filmomhulde tabletten
EU/1/16/1170/017
EU/1/16/1170/018
EU/1/16/1170/019
Olumiant 2 mg filmomhulde tabletten
EU/1/16/1170/001
EU/1/16/1170/002
EU/1/16/1170/003
EU/1/16/1170/004
EU/1/16/1170/005
EU/1/16/1170/006
EU/1/16/1170/007
EU/1/16/1170/008
Olumiant 4 mg filmomhulde tabletten
EU/1/16/1170/009
EU/1/16/1170/010
EU/1/16/1170/011
EU/1/16/1170/012
EU/1/16/1170/013
EU/1/16/1170/014
EU/1/16/1170/015
EU/1/16/1170/016
10. DATUM VAN HERZIENING VAN DE TEKST: 27 APRIL 2026
AFLEVERINGSWIJZE Geneesmiddel op beperkt medisch voorschrift.
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3593324 | OLUMIANT 2MG FILMOMH TABL 28 X 2MG | L04AA37 | € 910,3 | - | Ja | € 12,8 | € 8,5 |
| 3593332 | OLUMIANT 2MG FILMOMH TABL 84 X 2MG | L04AA37 | € 2402,8 | - | Ja | € 15,9 | € 10,5 |
| 3593340 | OLUMIANT 4MG FILMOMH TABL 28 X 4MG | L04AA37 | € 910,3 | - | Ja | € 12,8 | € 8,5 |
| 3593357 | OLUMIANT 4MG FILMOMH TABL 84 X 4MG | L04AA37 | € 2402,8 | - | Ja | € 15,9 | € 10,5 |