1. NAAM VAN HET GENEESMIDDEL
Yasmin 0,03 mg/3 mg filmomhulde tabletten
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke filmomhulde tablet bevat 0,030 mg ethinylestradiol en 3 mg drospirenon.
Hulpstof met bekend effect: lactose 46 mg (als lactosemonohydraat 48,17 mg).
Voor de volledige lijst van hulpstoffen: zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Filmomhulde tablet.
Lichtgele, ronde tabletten met convexe zijden, één zijde met de letters “DO” in een regelmatige zeshoek.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Orale anticonceptie.
Bij de beslissing om Yasmin voor te schrijven moet rekening worden gehouden met de huidige risicofactoren van de individuele vrouw, in het bijzonder met de factoren voor veneuze trombo-embolie (VTE) en hoe het risico op VTE met Yasmin zich verhoudt tot het risico met andere gecombineerde hormonale anticonceptiva (zie rubrieken 4.3 en 4.4).
4.2 Dosering en wijze van toediening
Wijze van toediening
Oraal gebruik
Dosering
Hoe wordt Yasmin ingenomen?
De tabletten moeten elke dag op ongeveer hetzelfde tijdstip worden ingenomen, zonodig met wat vloeistof, in de volgorde die op de blisterverpakking staat aangegeven. Gedurende 21 opeenvolgende dagen moet dagelijks één tablet worden ingenomen. Elke volgende blisterverpakking wordt gestart na een tabletvrij interval van 7 dagen. Tijdens dit interval treedt doorgaans een onttrekkingsbloeding op. Deze bloeding begint meestal op de tweede of derde dag na de laatste tablet en is mogelijk niet voorbij voordat met de volgende blisterverpakking wordt begonnen.
Hoe beginnen met Yasmin?
- Geen voorafgaand gebruik van een hormonaal anticonceptivum (in de afgelopen maand)
De eerste tablet dient op dag 1 van de natuurlijke cyclus van de vrouw te worden ingenomen (d.i. op de eerste dag van de menstruatie).
- Overschakelen van een gecombineerd hormonaal anticonceptivum (gecombineerd oraal anticonceptivum (COAC), vaginale anticonceptiering of anticonceptiepleister)
De vrouw dient bij voorkeur met Yasmin te starten op de dag na de laatste werkzame tablet (de laatste tablet met de werkzame bestanddelen) van haar voorgaande COAC, maar niet later dan op de dag na het gebruikelijke tabletvrije of placebotablet interval van haar voorgaande COAC. Als een vaginale anticonceptiering of een anticonceptiepleister is gebruikt, dient de vrouw bij voorkeur te beginnen met Yasmin op de dag van verwijdering, maar niet later dan op de dag waarop de volgende ring of pleister zou moeten worden geplaatst.
- Overschakelen van een progestageenmethode (OAC met alleen een progestageen; injectiepreparaat, implantaat) of progestageen-afgevend intra-uterien systeem (IUS)
De vrouw mag overschakelen van een OAC met alleen een progestageen wanneer zij wil (van een implantaat of IUS op de dag van verwijdering en van een injectiepreparaat op de dag waarop de volgende injectie zou moeten worden gegeven), maar moet in al deze gevallen geadviseerd worden om tijdens de eerste 7 dagen van de tablet-inname aanvullend een barrièremiddel te gebruiken.
- Na een abortus in het eerste trimester
De vrouw mag direct beginnen. In dit geval hoeft ze geen aanvullende anticonceptieve maatregelen te nemen.
- Na een bevalling of na een abortus in het tweede trimester
Aangeraden wordt tussen de 21e en 28e dag na de bevalling of na een abortus in het tweede trimester te starten. Als een vrouw later begint, dan moet haar worden aangeraden om tijdens de eerste 7 dagen aanvullend een barrièremiddel te gebruiken. Als inmiddels echter geslachtsgemeenschap heeft plaatsgevonden, dan moet een zwangerschap worden uitgesloten of moet de eerste menstruatie worden afgewacht voordat de vrouw met het COAC begint.
Voor vrouwen die borstvoeding geven: zie rubriek 4.6.
Wat te doen na het vergeten van tabletten?
Als een vrouw minder dan 12 uur te laat is met het innemen van een tablet, is de anticonceptieve werking niet verminderd. De vrouw moet deze tablet innemen zodra zij eraan denkt en op het gebruikelijke tijdstip verdergaan met de resterende tabletten.
Als de vrouw meer dan 12 uur te laat is met het innemen van een tablet, kan de anticonceptieve werkzaamheid verminderd zijn. Bij het beleid van vergeten tabletten kunnen de volgende twee basisregels als leidraad dienen:
- Het innemen van tabletten mag nooit langer dan 7 achtereenvolgende dagen onderbroken worden.
- Tabletten moeten 7 dagen zonder onderbreking worden ingenomen om de hypothalamus-hypofyse-ovariumas voldoende te onderdrukken.
Dienovereenkomstig kunnen in de praktijk de volgende adviezen worden gegeven:
- Week 1
De vrouw moet de laatste vergeten tablet innemen zodra zij eraan denkt, zelfs als dit betekent dat zij twee tabletten op hetzelfde moment moet innemen. Zij gaat daarna op het gebruikelijke tijdstip verder met de resterende tabletten. Aanvullend dient gedurende de eerstvolgende 7 dagen na het vergeten een barrièremiddel, zoals bijvoorbeeld een condoom, te worden gebruikt. Als er geslachtsgemeenschap heeft plaatsgehad in de 7 dagen vóór het vergeten van de tabletten dan moet rekening worden gehouden met een mogelijke zwangerschap. De kans op zwangerschap wordt groter naarmate er meer tabletten zijn vergeten en deze tabletten korter na het tabletvrije interval zijn vergeten.
- Week 2
De vrouw moet de laatste vergeten tablet innemen zodra zij eraan denkt, zelfs als dit betekent dat zij twee tabletten op hetzelfde moment moet innemen. Zij gaat daarna op het gebruikelijke tijdstip verder met de resterende tabletten. Als de vrouw de tabletten in de 7 dagen voorafgaande aan de eerste vergeten tablet correct heeft ingenomen, is geen aanvullende anticonceptie nodig. Als de vrouw echter meer dan 1 tablet is vergeten, moet haar aangeraden worden om gedurende de eerstvolgende 7 dagen aanvullend een barrièremiddel te gebruiken.
- Week 3
Vanwege de naderende 7-daagse tabletvrije periode dreigt het gevaar van verminderde betrouwbaarheid. Door het aanpassen van het tabletinnameschema kan echter worden voorkomen dat de contraceptieve betrouwbaarheid daadwerkelijk vermindert. Bij het opvolgen van één van de volgende twee adviezen is dan ook geen aanvullende anticonceptie nodig, mits de vrouw de tabletten in de 7 dagen voorafgaande aan de eerste vergeten tablet allemaal correct heeft ingenomen. Als dit niet het geval is, moet zij het eerste van de hierna gegeven adviezen volgen en bovendien gedurende de eerstvolgende 7 dagen aanvullend een barrièremiddel gebruiken.
- De vrouw moet de laatste vergeten tablet innemen zodra zij eraan denkt, zelfs als dit betekent dat zij twee tabletten op hetzelfde moment moet innemen. Zij gaat daarna op het gebruikelijke tijdstip verder met de resterende tabletten. Zodra zij klaar is met de huidige blisterverpakking moet ze doorgaan met de volgende blisterverpakking, m.a.w. er mag geen onderbreking zijn tussen de blisterverpakkingen. De vrouw heeft waarschijnlijk geen onttrekkingsbloeding tot aan het einde van de tweede blisterverpakking maar er kan wel spotting of doorbraakbloeding optreden tijdens de innamedagen van deze blisterverpakking.
- De vrouw mag ook worden aangeraden om te stoppen met het innemen van tabletten uit de huidige blisterverpakking. Ze moet dan een tabletvrije periode van maximaal 7 dagen inlassen, inclusief de dagen waarop zij tabletten was vergeten, en vervolgens doorgaan met de volgende blisterverpakking.
Als een vrouw tabletten heeft vergeten en vervolgens geen onttrekkingsbloeding krijgt in de eerstvolgende normale tabletvrije periode dan moet rekening worden gehouden met een eventuele zwangerschap.
Advies in het geval van gastro-intestinale stoornissen
In het geval van ernstige gastro-intestinale stoornissen (bijv. overgeven of diarree), kan de absorptie gestoord zijn en dienen aanvullende anticonceptiemiddelen te worden gebruikt. Als braken optreedt binnen 3-4 uur na de inname van een tablet, moet er zo snel mogelijk een nieuwe (vervangende) tablet worden ingenomen. De nieuwe tablet moet binnen 12 uur na het gebruikelijke tijdstip van tabletinname worden genomen als dit mogelijk is. Als er echter meer dan 12 uren zijn verstreken, geldt het advies voor het vergeten van tabletten dat in rubriek 4.2 “Wat te doen na het vergeten van tabletten?” is gegeven. Als de vrouw haar normale schema van tabletinname niet wil veranderen, moet ze de extra tablet(ten) uit een andere blisterverpakking nemen.
Hoe kan een onttrekkingsbloeding worden uitgesteld?
Om een maandelijkse bloeding een keer uit te stellen dient de vrouw zonder een tabletvrije periode door te gaan met de volgende Yasmin-blisterverpakking. De maandelijkse bloeding kan zolang als gewenst is worden uitgesteld, maar niet langer dan tot het einde van de tweede blisterverpakking. Tijdens de verlenging kan de vrouw doorbraakbloeding of spotting krijgen. Na de gebruikelijke tabletvrije periode van 7 dagen wordt de reguliere inname van Yasmin hervat.
Als een vrouw de huidige begindag van haar menstruatie wenst te verschuiven naar een andere dag, kan men haar aanraden om haar eerstvolgende tabletvrije periode te verkorten met zoveel dagen als zij wenst. Hoe korter de tabletvrije periode wordt, des te groter wordt ook de kans op het uitblijven van de onttrekkingsbloeding en het optreden van doorbraakbloeding en spotting tijdens het gebruik van de volgende strip (vergelijkbaar met het uitstellen van de menstruatie).
Bijkomende informatie over speciale patiëntengroepen
Pediatrische patiënten
Yasmin is enkel geïndiceerd na de menarche. Gebaseerd op epidemiologisch onderzoek verzameld bij meer dan 2000 adolescente vrouwen jonger dan 18 jaar, zijn er geen gegevens die aantonen dan de veiligheid en doeltreffendheid in deze jonge leeftijdsgroep verschilt met hetgeen gekend is bij vrouwen ouder dan 18 jaar.
Ouderen
Yasmin is niet geïndiceerd voor gebruik na de menopauze.
Patiënten met leverfunctiestoornis
Yasmin is gecontra-indiceerd bij vrouwen met ernstige leverziektes. Zie ook rubrieken 4.3 en 5.2.
Patiënten met nierfunctiestoornis
Yasmin is gecontra-indiceerd bij vrouwen met een ernstige nierfunctiestoornis of acuut nierfalen. Zie ook rubrieken 4.3 en 5.2.
4.3 Contra-indicaties
Gecombineerde hormonale anticonceptiva (CHC's) mogen in de volgende situaties niet worden gebruikt. Als één van deze aandoeningen voor het eerst optreedt tijdens het gebruik van een CHC dan moet het gebruik hiervan onmiddellijk worden gestaakt.
- Aanwezigheid van of risico op veneuze trombo-embolie (VTE)
- Veneuze trombo-embolie – bestaande VTE (bij antistollingsmiddelen) of eerder doorgemaakte VTE (bijv. diepe veneuze trombose [DVT] of longembolie [PE])
- Bekende erfelijke of verworven predispositie voor veneuze trombo-embolie, bijvoorbeeld APC-resistentie, (waaronder factor V-Leiden), antitrombine‑III-deficiëntie, proteïne C-deficiëntie, proteïne S-deficiëntie
- Zware operatie met langdurige immobilisatie (zie rubriek 4.4)
- Een hoog risico van veneuze trombo-embolie door de aanwezigheid van meerdere risicofactoren (zie rubriek 4.4)
- Aanwezigheid van of risico op arteriële trombo-embolie (ATE)
- Arteriële trombo-embolie – bestaande arteriële trombo-embolie, eerder doorgemaakte arteriële trombo-embolie (bijv. myocardinfarct) of prodromale aandoening (bijv. angina pectoris)
- Cerebrovasculaire ziekte – bestaande beroerte, eerder doorgemaakte beroerte of prodromale aandoening (bijv. transient ischaemic attack (TIA))
- Bekende erfelijke of verworven predispositie voor arteriële trombo-embolie, bijvoorbeeld hyperhomocysteïnemie en antifosfolipiden-antistoffen (anticardiolipine-antistoffen, lupusanticoagulans)
- Voorgeschiedenis van migraine met focale neurologische symptomen
- Een hoog risico op arteriële trombo-embolie als gevolg van meerdere risicofactoren (zie rubriek 4.4) of door de aanwezigheid van een ernstige risicofactor, zoals:
- diabetes mellitus met vasculaire symptomen
- ernstige hypertensie
- ernstige dislipoproteïnemie
- Manifeste of eerder doorgemaakte ernstige leveraandoeningen zolang de leverfunctiewaarden niet genormaliseerd zijn.
- Ernstige nierinsufficiëntie of acuut nierfalen.
- Manifeste of eerder doorgemaakte levertumoren (benigne of maligne).
- Aanwezigheid van geslachtshormoonafhankelijke maligne aandoeningen (bijvoorbeeld van de geslachtsorganen of de mammae), of het vermoeden daarvan.
- Vaginale bloedingen waarvan de diagnose niet is gesteld.
- Overgevoeligheid voor de werkzame stoffen of voor een van de in rubriek 6.1 vermelde hulpstoffen.
Yasmin is gecontra-indiceerd voor concomitant gebruik met geneesmiddelen die ombitasvir/paritaprevir/ritonavir en dasabuvir bevatten, geneesmiddelen die glecaprevir/pibrentasvir of sofosbuvir/velpatasvir/voxilaprevir bevatten (zie rubriek 4.5).
4.8 Bijwerkingen
Voor ernstige ongewenste effecten bij gebruiksters van een COAC zie ook rubriek 4.4.
De volgende ongewenste geneesmiddelenreacties werden tijdens het gebruik van Yasmin gerapporteerd:
Systeem/orgaanklassen (MedDRA) | Frequentie van bijwerkingen | |||
Vaak | Soms | Zelden | Niet bekend | |
Immuunsysteem-aandoeningen |
|
| Overgevoeligheid, | Verergering van symptomen van erfelijk en verworven angio-oedeem |
Psychische aandoeningen | Neerslachtigheid | Verhoogd libido, Verlaagd libido |
|
|
Zenuwstelsel-aandoeningen | Hoofdpijn |
|
|
|
Evenwichtsorgaan- en ooraandoeningen |
|
| Hypoacusis |
|
Bloedvataandoeningen | Migraine | Hypertensie, | Veneuze trombo-embolie (VTE), Arteriële trombo-embolie (ATE) |
|
Maagdarmstelsel-aandoeningen | Nausea | Braken, |
|
|
Huid- en onderhuid-aandoeningen |
| Acne, | Erythema nodosum, |
|
Voortplantingsstelsel- en borstaandoeningen | Menstruatiestoornissen, | Vergroting van de borsten, | Afscheiding uit de borsten |
|
Algemene aandoeningen en toedieningsplaats-stoornissen |
| Vochtretentie, Gewichtstoename, Gewichtsverlies |
|
|
Beschrijving van geselecteerde bijwerkingen
Er is een verhoogd risico waargenomen op arteriële en veneuze trombotische en trombo-embolische voorvallen, waaronder myocardinfarct, beroerte, transiënte ischemische aanvallen, veneuze trombose en longembolie bij vrouwen die gecombineerde hormonale anticonceptiva gebruikten. Hier wordt in rubriek 4.4 dieper op ingegaan.
De volgende ernstige bijwerkingen, welke besproken zijn in rubriek 4.4 “Bijzondere waarschuwingen en voorzorgen bij gebruik”, zijn gerapporteerd bij gebruiksters van COAC’s:
- veneuze trombo-embolieën;
- arteriële trombo-embolieën;
- hypertensie;
- levertumoren;
- aandoeningen die kunnen optreden of verslechteren, waarvan geen eenduidig bewijs is dat er verband bestaat met het gebruik van COAC’s: ziekte van Crohn, colitis ulcerosa, epilepsie, uterusmyomen, porfyrie, systemische lupus erythematosus, herpes gestationis, chorea van Sydenham, hemolytisch uremisch syndroom, cholestatische geelzucht;
- chloasma;
- acute en chronische leverfunctiestoornissen kunnen het noodzakelijk maken dat het gebruik van een COAC wordt gestaakt totdat de parameters weer zijn genormaliseerd;
De frequentie van de diagnose borstkanker is heel licht toegenomen bij OAC-gebruiksters. Aangezien borstkanker zelden voorkomt bij vrouwen onder de 40 jaar, is het aantal extra gevallen klein vergeleken met het levenslange risico van borstkanker. Een oorzakelijk verband met COAC’s is onbekend. Voor verdere informatie, zie rubrieken 4.3 en 4.4.
Interacties
Doorbraakbloeding en/of mislukken van de anticonceptie kunnen te wijten zijn aan interacties tussen andere geneesmiddelen (enzyminductoren, bepaalde antibiotica) en orale anticonceptiva (zie rubriek 4.5).
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Bayer SA-NV
Kouterveldstraat 7A 301
B-1831 Diegem (Machelen)
8. NUMMERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
België: BE218066
Luxemburg: 2009050310
1x 21 tabletten 0547151
3x 21 tabletten 0287115
6x 21 tabletten 0547164
13x 21 tabletten 0547178
10. DATUM VAN HERZIENING VAN DE TEKST
Goedkeuringsdatum: 03/2025
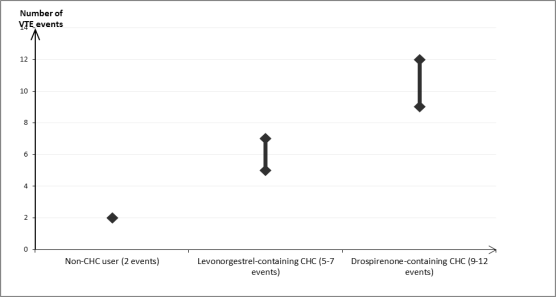
[1] Deze incidenties werden geschat op basis van alle epidemiologische onderzoeksgegevens samen, met gebruik van relatieve risico's voor de verschillende producten, vergeleken met levonorgestrelbevattende gecombineerde hormonale anticonceptiva.
[2] Middelste punt van het bereik ('mid-point of range') van 5‑7 per 10.000 vrouwjaren, op basis van een relatief risico voor levonorgestrelbevattende gecombineerde hormonale anticonceptiva versus niet-gebruik van ongeveer 2,3 tot 3,6
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 1596915 | YASMIN DRAG 3 X 21 | G03AA12 | € 34,22 | - | Ja | € 25,22 | € 25,22 |
| 2677441 | YASMIN DRAG 13 X 21 | G03AA12 | € 116,04 | - | Ja | € 77,04 | € 77,04 |
| 2677458 | YASMIN DRAG 6 X 21 | G03AA12 | € 59,04 | - | Ja | - | - |