1. NAAM VAN HET GENEESMIDDEL
Lindynette 20 gestodeen 75 microgram/ethinylestradiol 20 microgram omhulde tabletten
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke tablet bevat 75 microgram gestodeen en 20 microgram ethinylestradiol.
Hulpstoffen met bekend effect: elke tablet bevat 35,3068 mg lactose (als lactosemonohydraat), 19,6600 mg sucrose.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Omhulde tabletten.
Licht geel, ronde, biconvexe tabletten, beide zijden zijn zonder opdruk.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Anticonceptivum.
Bij de beslissing om Lindynette 20 voor te schrijven moet rekening worden gehouden met de huidige risicofactoren van de individuele vrouw, in het bijzonder met de risicofactoren voor veneuze trombo-embolie (VTE) en hoe het risico op VTE met Lindynette 20 zich verhoudt tot het risico met andere gecombineerde hormonale anticonceptiva (zie rubrieken 4.3 en 4.4).
4.2 Dosering en wijze van toediening
Start niet met Lindynette 20 of blijf Lindynette 20 niet gebruiken bij zwangerschap of bij een vermoeden van zwangerschap.
Dosering
Hoe Lindynette 20 innemen
Voor patiënten die een verpakking met 21 actieve tabletten gebruiken:
De tabletten 1-21 bevatten werkzame stoffen (actieve tabletten).
De tabletten dienen in de op de verpakking aangegeven volgorde dagelijks op ongeveerhetzelfde tijdstip te worden ingenomen. Gedurende 21 opeenvolgende dagen dient één tablet per dag te worden ingenomen. Elke volgende verpakking dient na een tabletvrije tussenpoos van 7 dagen, gedurende welke tijd een onttrekkingsbloeding gewoonlijk optreedt, begonnen te worden. Deze bloeding zal gewoonlijk op de 2e of 3e dag na het innemen van de laatste tablet beginnen en kan mogelijk pas stoppen nadat de volgende verpakking is gestart.
Hoe starten met Lindynette 20
Zonder eerder gebruik van hormonaal anticonceptivum in de afgelopen maand
Op de eerste dag van de normale cyclus van de vrouw wordt begonnen met het innemen van de tabletten. (d.w.z. op de eerste dag van de menstruele bloeding van de vrouw). Beginnen met de tabletten tussen de 2de en de 5de dag is toegestaan, maar tijdens de eerste cyclus het gebruik van een bijkomende, niet-hormonale, mechanische contraceptiemethode (condoom, spermadodend middel…) is aanbevolen gedurende de eerste 7 dagen.
Bij het vervangen van een andere anticonceptiepil van het combinatietype
De vrouw moet Lindynette 20 starten de dag na het gebruikelijke tabletvrije of placebotabletinterval van haar vorige gecombineerde orale anticonceptivum
Bij het overstappen van uitsluitend progestageenpreparaten (mini-pillen, injectie, implantaat, intra-uterien systeem)
De vrouw kan elke dag overstappen van pillen met uitsluitend progestogeen (bij het veranderen van een implantaat, op de dag waarop het implantaat wordt verwijderd of bij het overschakelen van injecties, wanneer de volgende injectie gegeven moet worden). In al deze gevallen wordt de vrouw geadviseerd gedurende de eerste 7 dagen waarop de pillen worden ingenomen ook gelijktijdig een barrièremethode te gebruiken.
Na een abortus gedurende het eerste trimester
De vrouw kan onmiddellijk beginnen met het innemen van de pillen. In dat geval is geen bijkomende contraceptiemethode nodig.
Na bevalling of abortus in het tweede trimester
Voor vrouwen die borstvoeding geven - zie rubriek 4.6.
Men dient de vrouw te adviseren op dag 21 – 28 na de bevalling te beginnen met het innemen van de tabletten, wanneer zij geen borstvoeding geeft, of na een abortus in het tweede trimester. De vrouw moet ook geadviseerd worden gedurende de eerste 7 dagen waarop de pillen worden ingenomen, gelijktijdig een andere contraceptieve methode te gebruiken. Maar als zij al gemeenschap heeft gehad, moet het bestaan van een zwangerschap worden uitgesloten alvorens zij de pillen begint in te nemen of dient zij te wachten op haar eerste menstruatie.
Gemiste tabletten
Het contraceptieve effect kan verminderen als de vrouw vergeet een tablet in te nemen, vooral als daardoor het tabletvrije interval toeneemt.
Als de vrouw minder dan 12 uur geleden een tablet had moeten innemen, moet ze de tablet innemen zodra ze er zich rekenschap van geeft, en moet ze de overblijvende tabletten op het gebruikelijke tijdstip innemen.
Als het meer dan 12 uur geleden is, kan de contraceptieve bescherming verminderen.
De vrouw moet de laatste gemiste tablet innemen zodra ze er zich rekenschap van geeft, ook als dat betekent dat ze 2 tabletten terzelfder tijd moet innemen. Daarna blijft ze verder de tabletten innemen op het gebruikelijke tijdstip. Tijdens de volgende 7 dagen moet ze tevens een barrièremethode toepassen.
Als er minder dan 7 dagen over zijn in de huidige verpakking, moet de vrouw met de volgende verpakking door te gaan tot deze verpakking leeg is, zonder tabletvrij interval. Dat voorkomt een langer tabletvrij interval (dat laatste zou het risico op voortijdige eisprong verhogen). Een dervingsbloeding is onwaarschijnlijk tot het einde van de tweede blisterverpakking, maar de vrouw kan wel spotting of doorbraakbloedingen vertonen op de dagen dat ze tabletten inneemt.
Als er geen bloeding optreedt na beëindiging van de tweede verpakking, moet de mogelijkheid van zwangerschap worden uitgesloten voor de vrouw verder gaat met de tabletten in de volgende verpakking.
Raad in geval van braken/diarree
Bij braken binnen 3-4 uur na het innemen van de tablet, kan absorptie mogelijk niet volledig zijn. In dit geval dient het hierboven beschreven advies met betrekking tot gemiste pillen te worden gevolgd. De vrouw moet de vereiste extra pil(len) uit een andere blisterverpakking nemen.
Bij langer durende of ernstige gastro-intestinale symptomen, moet de vrouw worden geadviseerd om een andere anticonceptiemethode te gebruiken en / of contact op te nemen met haar arts.
Hoe kan een menstruatie uitgesteld of veranderd worden
Om het bloedverlies uit te stellen, dient de vrouw door te gaan met een volgende verpakking Lindynette 20 zonder pilvrij interval. Men kan verlengen zolang men wil tot het einde van de tweede verpakking. Gedurende de verlenging kan de vrouw doorbraakbloeding of spotting ondervinden. Regelmatig innemen van Lindynette 20 wordt na de gebruikelijke pauze van 7 tabletvrije dagen hervat.
Om haar menstruatie te verschuiven naar een andere dag van de week dan waaraan de vrouw gewend is met haar huidige schema, kan men haar adviseren haar komende tabletvrije pauze met zoveel dagen in te korten als zij wil. Hoe korter de pauze, hoe groter het risico dat zij geen onttrekkingsbloeding zal hebben en tijdens de volgende verpakking doorbraakbloeding en spotting zal ondervinden (net als bij het uitstellen van een menstruatie).
Speciale populaties
Ouderen
Niet van toepassing. Lindynette 20 is niet geïndiceerd voor gebruik na de menopauze.
Leverfunctiestoornis
Lindynette 20 is gecontra-indiceerd bij vrouwen met leverfunctiestoornissen (zie rubriek 4.3).
Nierfunctiestoornis
Er zijn geen gegevens beschikbaar bij patiënten met nierfunctiestoornissen.
Pediatrische patiënten
Lindynette 20 is slechts aangewezen na de eerste menstruatie.
Wijze van toediening
Voor oraal gebruik.
4.3 Contra-indicaties
Gecombineerde orale anticonceptiva (COC’s) mogen niet worden gebruikt in geval van een van de onderstaande condities. Mocht een van die condities voor het eerst verschijnen tijdens het gebruik van het COC, moet het product onmiddellijk worden stopgezet:
- Aanwezigheid van of risico op veneuze trombo-embolie (VTE)
- Veneuze trombo-embolie – bestaande VTE (bij antistollingsmiddelen) of eerder doorgemaakte VTE (bijv. diepe veneuze trombose [DVT] of longembolie [PE])
- Bekende erfelijke of verworven predispositie voor veneuze trombo-embolie, bijvoorbeeld APC-resistentie, (waaronder factor V-Leiden), antitrombine‑III-deficiëntie, proteïne C-deficiëntie, proteïne S-deficiëntie
- Zware operatie met langdurige immobilisatie (zie rubriek 4.4)
- Een hoog risico van veneuze trombo-embolie door de aanwezigheid van meerdere risicofactoren (zie rubriek 4.4)
- Aanwezigheid van of risico op arteriële trombo-embolie (ATE)
- Arteriële trombo-embolie – bestaande arteriële trombo-embolie, eerder doorgemaakte arteriële trombo-embolie (bijv. myocardinfarct) of prodromale aandoening (bijv. angina pectoris)
- Cerebrovasculaire ziekte – bestaande beroerte, eerder doorgemaakte beroerte of prodromale aandoening (bijv. transient ischaemic attack (TIA))
- Bekende erfelijke of verworven predispositie voor arteriële trombo-embolie, bijvoorbeeld hyperhomocysteïnemie en antifosfolipiden-antistoffen (anticardiolipine-antistoffen, lupusanticoagulans)
- Voorgeschiedenis van migraine met focale neurologische symptomen
- Een hoog risico op arteriële trombo-embolie als gevolg van meerdere risicofactoren (zie rubriek 4.4) of door de aanwezigheid van een ernstige risicofactor, zoals:
- diabetes mellitus met vasculaire symptomen
- ernstige hypertensie
- ernstige dislipoproteïnemie
- Aanwezigheid of voorgeschiedenis van pancreatitis geassocieerd met ernstige hypertriglyceridemie
- Ernstige of recente leveraandoeningen, zolang leverfunctietests niet zijn genormaliseerd
- Bekende of vermoede steroïdafhankelijke tumoren van de borsten of geslachtsorganen
- Huidige of eerdere benigne of maligne levertumoren
- Niet-gediagnosticeerde vaginale bloeding
- Overgevoeligheid voor de werkzame stoffen of voor (één van) de in rubriek 6.1 vermelde hulpstoffen.
Lindynette 20 is gecontra-indiceerd voor gelijktijdig gebruik met geneesmiddelen die ombitasvir/paritaprevir/ritonavir en dasabuvir bevatten, geneesmiddelen die glecaprevir/pibrentasvir of sofosbuvir/velpatasvir/voxilaprevir bevatten (zie rubriek 4.5).
4.8 Bijwerkingen
Beschrijving van geselecteerde bijwerkingen
Er is een verhoogd risico waargenomen op arteriële en veneuze trombotische en trombo-embolische voorvallen, waaronder myocardinfarct, beroerte, transiënte ischemische aanvallen, veneuze trombose en longembolie bij vrouwen die gecombineerde hormonale anticonceptiva gebruikten. Hier wordt in rubriek 4.4 dieper op ingegaan.
De volgende ernstige bijwerkingen zijn gemeld bij vrouwen die COC’s gebruiken, zie rubriek 4.3 en 4.4.
- goedaardige levertumoren (bijv. focale nodulaire hyperplasie, hepatisch adenoom)
- intra-epitheliale cervixneoplasie en cervixkanker
- borstkanker
In het begin van de behandelingsperiode kan een groot aantal (10-13%) vrouwen bijwerkingen vertonen zoals hoofdpijn, gevoelige borsten, malaise en spotting. Die bijwerkingen zijn gewoonlijk van voorbijgaande aard en verdwijnen na 2-4 maanden.
De volgende bijwerkingen werden gerapporteerd door gebruiksters van COC’s, maar het verband met het gebruik van COC’s is niet bewezen, maar ook niet uitgesloten;
Infecties en parasitaire aandoeningen | |
Neoplasmata, benigne, maligne en niet-gespecificeerd (inclusief cysten en poliepen) | |
Bloed- en lymfestelselaandoeningen | |
Immuunsysteemaandoeningen | |
Voedings- en stofwisselingsstoornissen | |
Psychische stoornissen | |
Zenuwstelselaandoeningen | |
Oogaandoeningen | |
Evenwichtsorgaan- en ooraandoeningen | |
Bloedvataandoeningen | |
Maag-darmstelselaandoeningen | |
Lever- en galaandoeningen | |
Huid- en onderhuidaandoeningen | |
Nier- en urinewegaandoeningen | |
Voortplantingsstelsel- en borstaandoeningen | |
Onderzoeken | |
De volgende ernstige bijwerkingen zijn gemeld bij vrouwen die COC’s gebruiken, zie rubriek 4.3 en 4.4.
- Veneuze trombo-embolie (diepe veneuze trombose van de benen of het kleine bekken en longembolie)
- Arteriële trombo-embolie
- Baarmoederhalskanker
- Levertumoren
- Huid- en onderhuidaandoeningen: chloasma, erythema nodosum
Er worden iets meer gevallen van borstkanker gediagnosticeerd bij COC-gebruiksters. Aangezien borstkanker zeldzaam is bij vrouwen jonger dan 40 jaar, stijgt het aantal gevallen weinig in vergelijking met het totale risico van borstkanker. Het is niet bewezen dat er een verband bestaat met COC. Voor meer informatie zie rubrieken 4.3 en 4.4.
Interacties
Een doorbraakbloeding en/of falen van de contraceptie kunnen het gevolg zijn van interactie van andere geneesmiddelen (enzyminducerende geneesmiddelen) met orale anticonceptiva (zie rubriek 4.5).
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België:
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
Luxemburg:
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Gedeon Richter Plc.
Gyömrői út 19-21
H-1103 Boedapest
Hungarije
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
BE283997
10. DATUM VAN HERZIENING VAN DE TEKST
02/2025
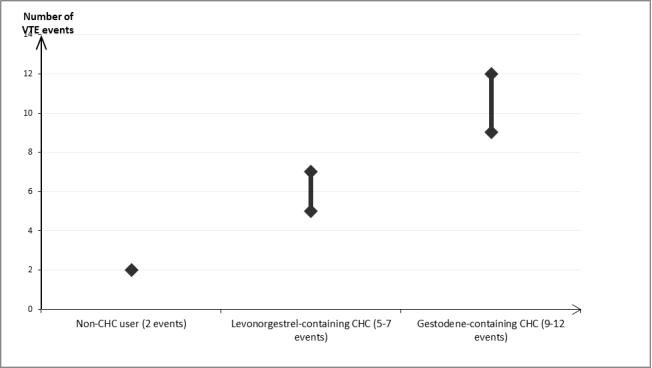
[1] Deze incidenties werden geschat op basis van alle epidemiologische onderzoeksgegevens samen, met gebruik van relatieve risico's voor de verschillende producten, vergeleken met levonorgestrelbevattende gecombineerde hormonale anticonceptiva.
[2] Middelste punt van het bereik ('mid-point of range') van 5‑7 per 10.000 vrouwjaren, op basis van een relatief risico voor levonorgestrelbevattende gecombineerde hormonale anticonceptiva versus niet-gebruik van ongeveer 2,3 tot 3,6
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 2257160 | LINDYNETTE 20 COMP 6 X 21 | G03AA10 | € 20,35 | - | Ja | € 2,35 | € 2,35 |
| 2257178 | LINDYNETTE 20 COMP 3 X 21 | G03AA10 | € 11,62 | - | Ja | € 2,62 | € 2,62 |
| 2314771 | LINDYNETTE 20 COMP 13 X 21 | G03AA10 | € 34,19 | - | Ja | - | - |