SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Xigduo 5 mg/850 mg, filmomhulde tabletten
Xigduo 5 mg/1000 mg, filmomhulde tabletten
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Xigduo 5 mg/850 mg, filmomhulde tabletten
Elke tablet bevat dapagliflozinepropaandiolmonohydraat, overeenkomend met 5 mg dapagliflozine en 850 mg metforminehydrochloride.
Xigduo 5 mg/1000 mg, filmomhulde tabletten
Elke tablet bevat dapagliflozinepropaandiolmonohydraat, overeenkomend met 5 mg dapagliflozine en 1000 mg metforminehydrochloride.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Filmomhulde tablet (tablet)
Xigduo 5 mg/850 mg, filmomhulde tabletten
Bruine, biconvexe, ovale (9,5 mm x 20 mm), filmomhulde tabletten met aan de ene zijde “5/850” in reliëf en aan de andere zijde “1067” in reliëf.
Xigduo 5 mg/1000 mg, filmomhulde tabletten
Gele, biconvexe, ovale (10,5 mm x 21,5 mm), filmomhulde tabletten met aan de ene zijde “5/1000” in reliëf en aan de andere zijde “1069” in reliëf.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Xigduo is geïndiceerd bij volwassenen voor de behandeling van type 2 diabetes mellitus als adjuvans op dieet en lichaamsbeweging:
- bij patiënten van wie de bloedglucose onvoldoende wordt gereguleerd met alleen de maximaal verdraagbare dosis metformine;
- in combinatie met andere geneesmiddelen voor de behandeling van diabetes bij patiënten van wie de bloedglucose onvoldoende wordt gereguleerd met metformine en deze andere geneesmiddelen;
- bij patiënten die al worden behandeld met de combinatie van dapagliflozine en metformine als afzonderlijke tabletten.
Voor onderzoeksresultaten betreffende combinatie van therapieën, effecten op de bloedglucoseregulatie en cardiovasculaire voorvallen en de onderzochte populaties, zie de rubrieken 4.4, 4.5 en 5.1.
4.2 Dosering en wijze van toediening
Dosering
Volwassenen met een normale nierfunctie (glomerulaire filtratiesnelheid [GFR] ≥ 90 ml/min)
De aanbevolen dosering is tweemaal daags één tablet. Iedere tablet bevat een vaste dosis dapagliflozine en metformine (zie rubriek 2).
Patiënten bij wie de bloedglucose onvoldoende wordt gereguleerd met een monotherapie van metformine of met een combinatietherapie van metformine en andere geneesmiddelen voor de behandeling van diabetes
Patiënten van wie de bloedglucose onvoldoende wordt gereguleerd met alleen metformine of metformine in combinatie met andere geneesmiddelen voor de behandeling van diabetes dienen een totale dagelijkse dosis Xigduo te krijgen die equivalent is aan 10 mg dapagliflozine plus de totale dagelijkse dosis metformine, of de dichtstbijzijnde therapeutisch geschikte dosis, die de patiënt al gebruikt. Wanneer Xigduo wordt gebruikt in combinatie met insuline of een insulineafscheidingsbevorderend middel, zoals een sulfonylureum, kan een lagere dosis insuline of sulfonylureum worden overwogen om het risico op hypoglykemie te verminderen (zie rubrieken 4.5 en 4.8).
Patiënten die overstappen van dapagliflozine en metformine als afzonderlijke tabletten
Patiënten die overstappen op Xigduo van afzonderlijke tabletten dapagliflozine (10 mg totale dagelijkse dosis) en metformine dienen dezelfde dagelijkse doses dapagliflozine en metformine te krijgen die de patiënt al gebruikt of de dichtstbijzijnde therapeutisch geschikte dosis metformine.
Bijzondere patiëntengroepen
Nierinsufficiëntie
Voor aanvang van de behandeling met metformine-bevattende geneesmiddelen dient de GFR te worden bepaald, en ten minste jaarlijks daarna. Bij patiënten met een verhoogd risico op verdere progressie van nierfunctiestoornissen en bij ouderen dient de nierfunctie vaker te worden bepaald, bijv. iedere 3‑6 maanden.
De maximale dagelijkse dosering metformine dient bij voorkeur te worden verdeeld over 2‑3 dagdoses. Factoren die het risico op lactaatacidose kunnen verhogen (zie rubriek 4.4) dienen beoordeeld te worden voordat initiatie met metformine bij patiënten met een GFR < 60 ml/min overwogen wordt.
Als er geen geschikte sterkte van Xigduo beschikbaar is, dienen de individuele bestanddelen gebruikt te worden in plaats van de vaste dosiscombinatie.
Tabel 1. Dosering bij patiënten met nierinsuffiëntie
GFR ml/min | Metformine | Dapagliflozine |
60‑89 | Maximale dagdosis is 3000 mg. | Maximale dagdosis is 10 mg. |
45‑59 | Maximale dagdosis is 2000 mg. | Maximale dagdosis is 10 mg. |
30‑44 | Maximale dagdosis is 1000 mg. | Maximale dagdosis is 10 mg. De glucoseverlagende werkzaamheid van dapagliflozine is verminderd. |
< 30 | Metformine is gecontra-indiceerd. | Maximale dagdosis is 10 mg. Vanwege de beperkte ervaring wordt het niet aanbevolen om een behandeling met dapagliflozine te starten bij patiënten met een GFR < 25 ml/min. De glucoseverlagende werkzaamheid van dapagliflozine is waarschijnlijk afwezig. |
Leverinsufficiëntie
Dit geneesmiddel dient niet gebruikt te worden bij patiënten met leverfunctiestoornissen (zie rubrieken 4.3, 4.4 en 5.2).
Ouderen (≥ 65 jaar)
Aangezien metformine gedeeltelijk wordt uitgescheiden door de nieren en oudere patiënten een grotere kans hebben op een verminderde nierfunctie, dient dit geneesmiddel met voorzichtigheid te worden gebruikt naarmate de leeftijd stijgt. De nierfunctie dient regelmatig te worden gecontroleerd om een metforminegerelateerde lactaatacidose te voorkomen, in het bijzonder bij oudere patiënten (zie rubrieken 4.3 en 4.4).
Pediatrische patiënten
De veiligheid en werkzaamheid van Xigduo bij kinderen en adolescenten in de leeftijd van 0 tot 18 jaar oud, zijn nog niet vastgesteld. Er zijn geen gegevens beschikbaar.
Wijze van toediening
Xigduo dient tweemaal daags te worden gegeven bij de maaltijd om de gastro-intestinale bijwerkingen van metformine te verminderen.
4.3 Contra-indicaties
Xigduo is gecontra-indiceerd bij patiënten:
- die overgevoelig zijn voor de werkzame stoffen of voor (één van) de in rubriek 6.1 vermelde hulpstof(fen);
- met alle vormen van acute metabole acidose (zoals lactaatacidose, diabetische ketoacidose);
- met diabetisch pre-coma;
- met ernstig nierfalen (GFR < 30 ml/min) (zie rubrieken 4.2, 4.4 en 5.2);
- met acute aandoeningen die mogelijk de nierfunctie beïnvloeden, zoals:
- dehydratie,
- ernstige infectie,
- shock;
- met een acute of chronische aandoening, die mogelijk hypoxie van weefsels kan veroorzaken, zoals:
- hartfalen of respiratoire insufficiëntie,
- een recent myocardinfarct,
- shock;
- met leverfunctiestoornissen (zie rubrieken 4.2, 4.4 en 5.2);
- met acute alcoholvergiftiging, alcoholisme (zie rubriek 4.5).
4.8 Bijwerkingen
Xigduo is bewezen bio-equivalent aan gelijktijdige toediening van dapagliflozine en metformine (zie rubriek 5.2). Er zijn geen therapeutische klinische studies uitgevoerd met Xigduo.
Dapagliflozine plus metformine
Samenvatting van het veiligheidsprofiel
De veiligheidsresultaten van een analyse van 5 placebogecontroleerde studies met dapagliflozine als add-on bij metformine waren vergelijkbaar met die van de vooraf gespecificeerde gepoolde analyse van 13 placebogecontroleerde studies met dapagliflozine (zie Dapagliflozine, Samenvatting van het veiligheidsprofiel, hieronder). Er werden geen bijkomende bijwerkingen waargenomen voor de dapagliflozine/metformine-groep ten opzichte van de gerapporteerde bijwerkingen van de individuele componenten. In de afzonderlijke gepoolde analyse van dapagliflozine als add-on bij metformine, werden 623 proefpersonen behandeld met dapagliflozine 10 mg als add-on bij metformine en 523 proefpersonen met placebo plus metformine.
Dapagliflozine
Samenvatting van het veiligheidsprofiel
In de klinische studies bij diabetes mellitus type 2 zijn meer dan 15.000 patiënten behandeld met dapagliflozine.
De primaire beoordeling van veiligheid en verdraagbaarheid werd uitgevoerd in een vooraf gespecificeerde, gepoolde analyse van 13 kortdurende (tot 24 weken) placebogecontroleerde studies met 2.360 proefpersonen behandeld met dapagliflozine 10 mg en 2.295 proefpersonen behandeld met placebo.
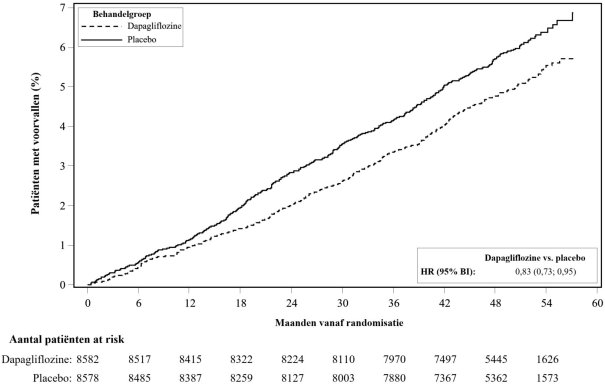
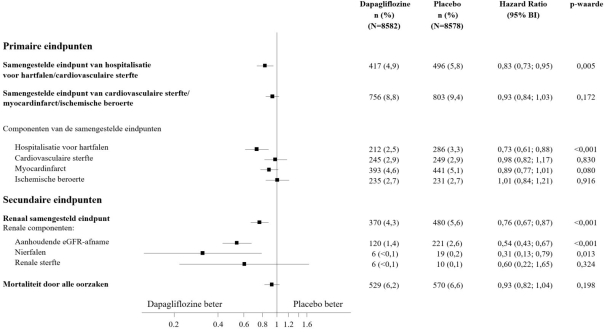
In de studie naar cardiovasculaire uitkomsten voor dapagliflozine (DECLARE, zie rubriek 5.1) ontvingen 8.574 patiënten dapagliflozine 10 mg en ontvingen 8.569 patiënten placebo gedurende een mediane blootstellingstijd van 48 maanden. In totaal waren er 30.623 patiëntjaren van blootstelling aan dapagliflozine.
De meest voorkomende gerapporteerde bijwerkingen in alle klinische studies waren genitale infecties.
Bijwerkingen in tabelvorm
De volgende bijwerkingen zijn vastgesteld op basis van de placebogecontroleerde klinische studies met dapagliflozine plus metformine, klinische studies met dapagliflozine, klinische studies met metformine en postmarketing ervaring. Geen enkele bijwerking werd dosisafhankelijk bevonden. De onderstaande bijwerkingen zijn geclassificeerd naar frequentie en Systeem/Orgaanklasse. De frequentiecategorieën zijn als volgt gedefinieerd: zeer vaak (≥ 1/10), vaak (≥ 1/100, < 1/10), soms (≥ 1/1.000, < 1/100), zelden (≥ 1/10.000, < 1/1.000), zeer zelden (< 1/10.000) en niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Tabel 2. Bijwerkingen uit klinische studies met dapagliflozine en metformine (directe afgifte) en post-marketing gegevens a.
Systeem/ Orgaanklasse | Zeer vaak | Vaak | Soms | Zelden | Zeer zelden |
Infecties en parasitaire |
| Vulvovaginitis, balanitis en gerelateerde genitale infecties*,b,c | Schimmel-infectie** |
| Necroti-serende fasciitis van het perineum (Fournier-gangreen)b,j |
Voedings- en stofwisselings-stoornissen | Hypoglykemie (bij gebruik met SU of insuline)b | Vitamine-B12- afname/ | Volume-depletie**, b, e | Diabetische ketoacidose b,j,k | Lactaatacidose |
Zenuwstelselaan-doeningen |
| Smaakstoornis§ |
|
|
|
Maagdarmstelselaandoeningen | Maagdarm- symptomen h,§ |
| Obstipatie ** |
|
|
Lever- en galaandoeningen |
|
|
|
| Leverfunctie- stoornissen§ |
Huid- en onderhuid-aandoeningen |
| Rashl |
|
| Urticaria§ |
Skeletspierstelsel- en bindweefsel-aandoeningen |
| Rugpijn* |
|
|
|
Nier- en urineweg-aandoeningen |
| Dysurie* | Nycturie** |
| Tubulo-interstitiële nefritis |
Voortplantings-stelsel- en borst-aandoeningen |
|
| Vulvovaginale pruritus** |
|
|
Onderzoeken |
| Verhoogd hematocriet g | Verhoogd bloed-creatinine gedurende initiële behandeling**,b |
|
|
a De tabel toont bijwerkingen vastgesteld uit gegevens tot 24 weken (korte termijn), ongeacht het gebruik van glykemische noodmedicatie, met uitzondering van gegevens met § gemarkeerd (zie hieronder).
b Zie de bijbehorende subrubriek hieronder voor verdere informatie.
c Vulvovaginitis, balanitis en gerelateerde genitale infecties omvatten bijvoorbeeld de vooraf gedefinieerde voorkeurstermen: vulvovaginale schimmelinfectie, vaginale infectie, balanitis, genitale schimmelinfectie, vulvovaginale candidiasis, vulvovaginitis, balanitis candida, genitale candidiase, genitale infectie, genitale infectie bij mannen, penisinfectie, vulvitis, bacteriële vaginitis, abces in de vulva.
dUrineweginfectie omvat de volgende voorkeurstermen, op volgorde van gemelde frequentie: urineweginfectie, cystitis, urineweginfectie met Escherichia, genito-urinaire infectie, pyelonefritis, trigonitis, uretritis, nierinfectie en prostatitis.
eVolumedepletie omvat bijvoorbeeld de vooraf gedefinieerde voorkeurstermen: dehydratie, hypovolemie, hypotensie.
fPolyurie omvat de voorkeurstermen: pollakisurie, polyurie, verhoogde urineproductie.
g Gemiddelde veranderingen ten opzichte van de baseline in hematocriet waren 2,30% voor dapagliflozine 10 mg versus -0,33% voor placebo. Hematocrietwaarden > 55% werden gemeld bij 1,3% van de proefpersonen die met dapagliflozine 10 mg werden behandeld versus 0,4% bij proefpersonen die placebo kregen.
h Gastro-intestinale symptomen zoals misselijkheid, overgeven, diarree, abdominale pijn en verminderde eetlust komen veelal voor bij aanvang van de therapie en verdwijnen spontaan in de meeste gevallen.
i Gemiddelde procentuele verandering ten opzichte van de baseline voor dapagliflozine 10 mg versus placebo was respectievelijk: totaal cholesterol 2,5% versus -0,0%; HDL-cholesterol 6,0% versus 2,7%; LDL-cholesterol 2,9% versus -1,0%; triglyceriden -2,7% versus -0,7%.
j Zie rubriek 4.4.
k Gerapporteerd in de studie naar cardiovasculaire uitkomsten bij patiënten met diabetes type 2 (DECLARE). Frequentie is gebaseerd op jaarlijks percentage.
l Bijwerking werd door postmarketing surveillance geïdentificeerd. Rash omvat de volgende voorkeurstermen, weergegeven op volgorde van frequentie in klinische studies: rash, gegeneraliseerde rash, jeukende rash, vlekkerige rash, maculopapilaire rash, pustuleuze rash, vesiculaire rash en erythemateuze rash. In actief- en placebogecontroleerde klinische studies (dapagliflozine, N=5936, alle controles, N=3403) was de frequentie van rash vergelijkbaar voor respectievelijk dapagliflozine (1,4%) en alle controles (1,4%).
* Gerapporteerd bij ≥ 2% proefpersonen die met dapagliflozine 10 mg werden behandeld en ≥ 1% meer proefpersonen die met dapagliflozine 10 mg werden behandeld ten opzichte van placebo en ten minste 3 proefpersonen meer die met dapagliflozine 10 mg werden behandeld ten opzichte van placebo.
** Gerapporteerd door de onderzoeker als mogelijk gerelateerd, waarschijnlijk gerelateerd of gerelateerd aan de studiebehandeling en gemeld bij ≥ 0,2% van de proefpersonen en ≥ 0,1% vaker en bij ten minste 3 proefpersonen meer die werden behandeld met dapagliflozine 10 mg ten opzichte van placebo.
§ Bijwerkingen en frequentie voor metformine zijn gebaseerd op informatie uit de Samenvatting van de productkenmerken van metformine, zoals beschikbaar in de Europese Unie.
Beschrijving van geselecteerde bijwerkingen
Dapagliflozine plus metformine
Hypoglykemie
In studies met dapagliflozine als add-on combinatietherapie met metformine werden milde episodes van hypoglykemie gerapporteerd met vergelijkbare frequenties voor de groep die werd behandeld met dapagliflozine 10 mg plus metformine (6,9%) en de groep die werd behandeld met placebo plus metformine (5,5%). Er werden geen ernstige gevallen van hypoglykemie gerapporteerd. Vergelijkbare waarnemingen zijn gedaan voor de combinatie van dapagliflozine plus metformine in geneesmiddel-naïeve patiënten.
In een studie met add-on van dapagliflozine aan metformine en een sulfonylureum, gedurende maximaal 24 weken, werden minder ernstige episodes van hypoglykemie gerapporteerd bij 12,8% van de proefpersonen die dapagliflozine 10 mg plus metformine en een sulfonylureum kregen en bij 3,7% van de proefpersonen die placebo plus metformine en een sulfonylureum kregen. Er werden geen ernstige episodes van hypoglykemie gerapporteerd.
Dapagliflozine
Vulvovaginitis, balanitis en verwante genitale infecties
In de gepoolde veiligheidsdata van 13 studies werden vulvovaginitis, balanitis en soortgelijke genitale infecties gemeld bij 5,5% en 0,6% van de proefpersonen die respectievelijk dapagliflozine 10 mg en placebo kregen. De meeste infecties waren mild tot matig en proefpersonen reageerden op een initiële standaardbehandeling; de infecties leidden zelden tot staken van de dapagliflozinebehandeling. Deze infecties kwamen vaker voor bij vrouwen (8,4% voor dapagliflozine en 1,2% voor placebo) en proefpersonen met een voorgeschiedenis hadden een grotere kans om een terugkerende infectie te krijgen.
In de DECLARE-studie was het aantal patiënten met een genitale infectie als ernstige bijwerking laag en gebalanceerd: 2 patiënten in zowel de dapagliflozine- als de placebogroep.
Bij dapagliflozine zijn gevallen van fimose/verworven fimose gemeld met gelijktijdige genitale infecties; in sommige gevallen moest de patiënt worden besneden.
Necrotiserende fasciitis van het perineum (fournier-gangreen)
Na het in de handel brengen zijn er gevallen van fournier-gangreen gemeld bij patiënten die SGLT2-remmers innemen, waaronder dapagliflozine (zie rubriek 4.4).
In de DECLARE-studie met 17.160 patiënten met diabetes mellitus type 2 en een mediane blootstellingstijd van 48 maanden zijn in totaal 6 gevallen van fournier-gangreen gemeld; één in de groep behandeld met dapagliflozine en vijf in de placebogroep.
Hypoglykemie
De frequentie van hypoglykemie was afhankelijk van het soort achtergrondtherapie dat in elke studie gebruikt werd.
In studies met dapagliflozine als add-on combinatietherapie met metformine en als add-on combinatietherapie met sitagliptine (met of zonder metformine) was de frequentie van milde episodes van hypoglykemie vergelijkbaar (< 5%) in de behandelgroepen, inclusief placebo tot aan 102 weken van behandeling. In alle studies kwamen soms ernstige gevallen van hypoglykemie voor en de frequentie hiervan was vergelijkbaar voor de groepen die behandeld werden met dapagliflozine of met placebo. In een studie met add-on combinatietherapie met insuline werden hogere percentages hypoglykemie waargenomen (zie rubriek 4.5).
In een add-on combinatiestudie met insuline tot 104 weken, werden episodes van ernstige hypoglykemie gerapporteerd bij 0,5% en 1,0% van de proefpersonen die werden behandeld met dapagliflozine 10 mg plus insuline in respectievelijk week 24 en week 104, en bij 0,5% van de proefpersonen die werden behandeld met placebo plus insuline in week 24 en week 104. In respectievelijk week 24 en week 104 werden milde episodes van hypoglykemie gerapporteerd bij 40,3% en 53,1% van de proefpersonen die dapagliflozine 10 mg plus insuline kregen en bij 34,0% en 41,6% van de proefpersonen die placebo plus insuline kregen.
In de DECLARE-studie werd geen verhoogd risico op ernstige hypoglykemie waargenomen bij dapagliflozinebehandeling vergeleken met placebo. Ernstige voorvallen van hypoglykemie werden gerapporteerd bij 58 (0,7%) van de patiënten behandeld met dapagliflozine en 83 (1,0%) van de patiënten behandeld met placebo.
Volumedepletie
In de gepoolde veiligheidsdata van 13 studies werden bijwerkingen die zouden kunnen wijzen op volumedepletie (inclusief meldingen van dehydratatie, hypovolemie of hypotensie) gerapporteerd bij 1,1% en 0,7% van de proefpersonen die respectievelijk dapagliflozine 10 mg en placebo kregen. Ernstige bijwerkingen deden zich voor bij < 0,2% van de proefpersonen en deze waren evenwichtig verspreid over dapagliflozine 10 mg en placebo (zie rubriek 4.4).
In de DECLARE-studie was het aantal patiënten met voorvallen die zouden kunnen wijzen op volumedepletie gebalanceerd tussen de behandelgroepen: 213 (2,5%) en 207 (2,4%) in respectievelijk de dapagliflozine- en placebogroep. Ernstige bijwerkingen werden gerapporteerd bij 81 (0,9%) en 70 (0,8%) van de patiënten in respectievelijk de dapagliflozine- en placebogroep. De voorvallen waren over het algemeen gebalanceerd tussen de behandelgroepen over subgroepen van leeftijd, gebruik van diuretica, bloeddruk en gebruik van ACEi/ARB. Bij patiënten met een eGFR < 60 ml/min/1,73 m2 op baseline, waren er 19 voorvallen van ernstige bijwerkingen die zouden kunnen wijzen op volumedepletie in de dapagliflozinegroep en 13 voorvallen in de placebogroep.
Diabetische ketoacidose
In de DECLARE-studie, met een mediane blootstelling van 48 maanden, werden voorvallen van DKA gerapporteerd bij 27 patiënten in de groep met dapagliflozine 10 mg en bij 12 patiënten in de placebogroep. De voorvallen waren gelijkmatig verdeeld over de studieperiode. Van de 27 patiënten met DKA-voorvallen in de dapagliflozinegroep, ontvingen er 22 gelijktijdige insulinebehandeling op het moment van het voorval. Precipiterende factoren voor DKA waren zoals verwacht in een populatie met diabetes mellitus type 2 (zie rubriek 4.4).
Urineweginfecties
In de gepoolde veiligheidsdata van 13 studies werden urineweginfecties vaker gerapporteerd voor dapagliflozine 10 mg dan voor placebo (respectievelijk 4,7% versus 3,5%; zie rubriek 4.4). De meeste gevallen van infectie waren licht tot matig en proefpersonen reageerden goed op een initiële kuur van een standaardbehandeling, de infecties leidden zelden tot staken van de dapagliflozinebehandeling. Deze infecties werden vaker gemeld bij vrouwen en proefpersonen met een voorgeschiedenis hadden een grotere kans om een terugkerende infectie te krijgen.
In de DECLARE-studie werden ernstige voorvallen van urineweginfecties minder vaak gerapporteerd voor dapagliflozine 10 mg vergeleken met placebo: 79 (0,9%) voorvallen versus 109 (1,3%) voorvallen, respectievelijk.
Verhoogd creatinine
Bijwerkingen gerelateerd aan verhoogd creatinine zijn gegroepeerd (bv. verminderde nierklaring creatinine, nierfunctiestoornis, verhoogd bloedcreatinine en verminderde glomerulaire filtratiesnelheid). Deze groepering van bijwerkingen is gemeld bij resp. 3,2% en 1,8% van de patiënten die met dapagliflozine 10 mg en met placebo behandeld werden. Bij patiënten met een normale nierfunctie of een lichte nierfunctiestoornis (baseline eGFR ≥ 60 ml/min/1,73m2) werd deze groepering van bijwerkingen gemeld bij resp. 1,3% en 0,8% van de patiënten die dapagliflozine 10 mg en placebo kregen. Deze bijwerkingen kwamen vaker voor bij patiënten met een baseline eGFR ≥ 30 en < 60 ml/min/1,73 m2 (18,5% bij dapagliflozine 10 mg versus 9,3% bij placebo).
Nadere evaluatie van de patiënten met bijwerkingen gerelateerd aan de nieren liet zien dat de meesten veranderingen in serumcreatinine hadden van ≤ 44 micromol/l (≤ 0,5 mg/dl) ten opzichte van baseline. De verhogingen in creatinine waren in het algemeen van voorbijgaande aard tijdens continue behandeling of reversibel na staken van de behandeling.
In de DECLARE-studie, waarin oudere patiënten en patiënten met nierinsufficiëntie (eGFR minder dan 60 ml/min/1,73 m2) waren opgenomen, nam de eGFR in de loop van de tijd in beide behandelgroepen af. Na 1 jaar was de gemiddelde eGFR iets lager, en na 4 jaar was de gemiddelde eGFR iets hoger in de dapagliflozinegroep vergeleken met de placebogroep.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
AstraZeneca AB
SE-151 85 Södertälje
Zweden
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Xigduo 5 mg/850 mg, filmomhulde tabletten
EU/1/13/900/001 Xigduo 5 mg/850 mg 14 tabletten
EU/1/13/900/002 Xigduo 5 mg/850 mg 28 tabletten
EU/1/13/900/003 Xigduo 5 mg/850 mg 56 tabletten
EU/1/13/900/004 Xigduo 5 mg/850 mg 60 tabletten
EU/1/13/900/005 Xigduo 5 mg/850 mg 60 x 1 tablet (eenheidsdosis)
EU/1/13/900/006 Xigduo 5 mg/850 mg 196 (2 x 98) tabletten (multipack)
Xigduo 5 mg/1000 mg, filmomhulde tabletten
EU/1/13/900/007 Xigduo 5 mg/1000 mg 14 tabletten
EU/1/13/900/008 Xigduo 5 mg/1000 mg 28 tabletten
EU/1/13/900/009 Xigduo 5 mg/1000 mg 56 tabletten
EU/1/13/900/010 Xigduo 5 mg/1000 mg 60 tabletten
EU/1/13/900/011 Xigduo 5 mg/1000 mg 60 x 1 tablet (eenheidsdosis)
EU/1/13/900/012 Xigduo 5 mg/1000 mg 196 (2 x 98) tabletten (multipack)
10. DATUM VAN HERZIENING VAN DE TEKST
03/2026
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3123528 | XIGDUO 5 MG/1000 MG FILMOMH TABL 56 | A10BD15 | € 47,7 | - | Ja | € 2 | € 1 |
| 3123544 | XIGDUO 5 MG/ 850 MG FILMOMH TABL 196 | A10BD15 | € 144,17 | - | Ja | € 2 | € 1 |
| 3123577 | XIGDUO 5 MG/ 850 MG FILMOMH TABL 56 | A10BD15 | € 47,7 | - | Ja | € 2 | € 1 |
| 3123585 | XIGDUO 5 MG/1000 MG FILMOMH TABL 196 | A10BD15 | € 144,17 | - | Ja | € 2 | € 1 |