1. NAAM VAN HET GENEESMIDDEL
Invokana 100 mg filmomhulde tabletten
Invokana 300 mg filmomhulde tabletten
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Invokana 100 mg filmomhulde tabletten
Elke tablet bevat canagliflozinehemihydraat, overeenkomend met 100 mg canagliflozine.
Hulpstof(fen) met bekend effect
Elke tablet bevat 39,26 mg lactose.
Invokana 300 mg filmomhulde tabletten
Elke tablet bevat canagliflozinehemihydraat, overeenkomend met 300 mg canagliflozine.
Hulpstof(fen) met bekend effect
Elke tablet bevat 117,78 mg lactose.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Filmomhulde tablet (tablet).
Invokana 100 mg filmomhulde tabletten
De tablet is geel, capsulevormig, ongeveer 11 mm lang, met onmiddellijke afgifte en filmomhuld, met aan de ene zijde ‘CFZ’ en aan de andere zijde ‘100’.
Invokana 300 mg filmomhulde tabletten
De tablet is wit, capsulevormig, ongeveer 17 mm lang, met onmiddellijke afgifte en filmomhuld, met aan de ene zijde ‘CFZ’ en aan de andere zijde ‘300’.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Invokana is geïndiceerd voor de behandeling van volwassenen en kinderen van 10 jaar en ouder met onvoldoende gereguleerde type 2-diabetes mellitus als aanvullend middel bij een dieet en lichaamsbeweging:
- als monotherapie wanneer metformine ongeschikt wordt geacht wegens intolerantie of contra‑indicaties
- naast andere geneesmiddelen voor de behandeling van diabetes
Voor onderzoeksresultaten met betrekking tot combinatie van behandelingen, effecten op bloedglucoseregulatie, cardiovasculaire en renale voorvallen en voor de onderzochte populaties, zie rubriek 4.4, 4.5 en 5.1.
4.2 Dosering en wijze van toediening
Dosering
De aanbevolen startdosering van canagliflozine is 100 mg eenmaal daags. Bij patiënten die canagliflozine 100 mg eenmaal daags verdragen en die een geschatte glomerulaire filtratiesnelheid (eGFR) hebben van ≥ 60 ml/min/1,73 m2 of een CrCl van ≥ 60 ml/min en die een striktere bloedglucoseregulatie nodig hebben, kan de dosis worden verhoogd tot 300 mg eenmaal daags (zie rubriek 4.4). Raadpleeg tabel 1 voor aanbevelingen over dosisaanpassing overeenkomstig de eGFR.
Men dient voorzichtig te zijn als de dosis wordt verhoogd bij patiënten met een leeftijd van ≥ 75 jaar, patiënten met een bekende cardiovasculaire aandoening of andere patiënten voor wie de aanvankelijke diurese die door canagliflozine wordt geïnduceerd, een risico betekent (zie rubriek 4.4). Bij patiënten met aantoonbare volumedepletie wordt aangeraden deze toestand te corrigeren voordat met canagliflozine wordt begonnen (zie rubriek 4.4).
Als canagliflozine wordt gebruikt als add‑on‑therapie bij insuline of een insulinesecretagoog (bijvoorbeeld een sulfonylureumderivaat), kan een lagere dosis van insuline of het insulinesecretagoog worden overwogen om het risico op hypoglykemie te verlagen (zie rubriek 4.5 en 4.8).
Bijzondere populaties
Ouderen
Men dient rekening te houden met de nierfunctie en het risico op volumedepletie (zie rubriek 4.4).
Nierinsufficiëntie
Voor de behandeling van diabetische nierschade als aanvulling op de standaardbehandeling (bijv. ACE‑remmers of ARB’s) moet eenmaal daags een dosis van 100 mg canagliflozine worden gebruikt (zie tabel 1). Overweeg de toevoeging van andere antihyperglykemische middelen, indien verdere bloedglucoseregulatie nodig is, omdat de werkzaamheid van canagliflozine voor verlaging van de bloedglucose minder is bij patiënten met matige tot ernstige nierinsufficiëntie en mogelijk afwezig is bij patiënten met ernstige nierinsufficiëntie. Raadpleeg tabel 1 voor aanbevelingen over dosisaanpassing overeenkomstig de eGFR.
Tabel 1: Aanbevelingen voor dosisaanpassing bij volwassenen en kinderen van 10 jaar en oudera | |
eGFR (ml/min/1,73 m2) | Totale dagelijkse dosis canagliflozine |
≥ 60 | Start met 100 mg. |
30 tot< 60b | Gebruik 100 mg. |
< 30b, c | Ga verder met 100 mg voor patiënten die al Invokana gebruikend. |
a Zie rubriek 4.4, 4.8, 5.1 en 5.2. | |
Leverinsufficiëntie
Er is geen dosisaanpassing nodig bij patiënten met een lichte of matige leverinsufficiëntie.
Canagliflozine is niet onderzocht bij patiënten met ernstige leverinsufficiëntie en gebruik bij deze patiënten wordt niet aangeraden (zie rubriek 5.2).
Pediatrische patiënten
Er is geen dosisaanpassing vereist voor de behandeling van type 2‑diabetes mellitus bij kinderen van 10 jaar en ouder (zie rubrieken 5.1 en 5.2). Bij kinderen met een lichaamsgewicht < 50 kg is voorzichtigheid geboden bij het optitreren van de dosis tot 300 mg, aangezien er beperkte veiligheidsgegevens beschikbaar zijn (zie rubriek 4.4).
De veiligheid en werkzaamheid van Invokana zijn niet vastgesteld bij kinderen jonger dan 10 jaar.
Wijze van toediening
Voor oraal gebruik
Invokana dient eenmaal per dag oraal te worden ingenomen, bij voorkeur voor de eerste maaltijd van de dag. Tabletten dienen in hun geheel te worden ingeslikt.
Als er een dosis is gemist, dient deze te worden ingenomen zodra de patiënt eraan denkt; men mag echter niet op een en dezelfde dag een dubbele dosis nemen.
4.3 Contra-indicaties
- Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De veiligheid van canagliflozine werd beoordeeld bij 22.645 volwassen patiënten met type 2‑diabetes, waaronder 13.278 patiënten behandeld met canagliflozine en 9.367 patiënten met de comparator in 15 dubbelblinde, gecontroleerde klinische fase III‑ en fase IV-studies. In totaal werden 10.134 volwassen patiënten behandeld in twee specifieke cardiovasculaire studies gedurende een blootstellingsduur van gemiddeld 149 weken (223 weken in CANVAS en 94 weken in CANVAS-R) en werden 8.114 volwassen patiënten behandeld in 12 dubbelblinde, gecontroleerde klinische fase III- en fase IV-studies gedurende een blootstellingsduur van gemiddeld 49 weken. In een specifieke studie naar nieruitkomsten hadden in totaal 4.397 volwassen patiënten met type 2-diabetes en diabetische nierschade een blootstellingsduur van gemiddeld 115 weken.
De primaire beoordeling van de veiligheid en tolerantie werd uitgevoerd in een gepoolde analyse (N = 2.313) van vier 26 weken durende placebogecontroleerde klinische studies (monotherapie en add‑on‑therapie met metformine, metformine en een sulfonylureumderivaat, en metformine en pioglitazon) bij volwassenen. De bijwerkingen die tijdens de behandeling het vaakst werden gemeld, waren hypoglykemie bij combinatie met insuline of een sulfonylureumderivaat, vulvovaginale candidiasis, urineweginfectie en polyurie of pollakisurie (d.w.z. frequent urineren). Bijwerkingen die leidden tot stopzetting bij ≥ 0,5% van alle met canagliflozine behandelde volwassen patiënten in deze studies waren vulvovaginale candidiasis (0,7% van de vrouwelijke patiënten) en balanitis of balanoposthitis (0,5% van de mannelijke patiënten). Aanvullende veiligheidsanalyses (met inbegrip van langetermijngegevens) van gegevens uit het hele canagliflozineprogramma (placebo- en actief gecontroleerde studies) werden uitgevoerd om gemelde bijwerkingen te beoordelen teneinde bijwerkingen vast te stellen (tabel 2) (zie rubriek 4.2 en 4.4).
Bijwerkingen in tabelvorm
De bijwerkingen in tabel 2 zijn gebaseerd op de gepoolde analyse van de hierboven beschreven placebogecontroleerde en actiefgecontroleerde studies. Bijwerkingen gerapporteerd tijdens wereldwijd postmarketinggebruik van canagliflozine zijn ook in deze tabel opgenomen. De onderstaande bijwerkingen zijn geclassificeerd naar frequentie en systeem/orgaanklasse. De frequentiecategorieën zijn als volgt gedefinieerd: zeer vaak (≥ 1/10), vaak (≥ 1/100, < 1/10), soms (≥ 1/1.000, < 1/100), zelden (≥ 1/10.000, < 1/1.000), zeer zelden (< 1/10.000) en niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Tabel 2: Bijwerkingen in tabelvorm (MedDRA) uit placebogecontroleerdee en actiefgecontroleerde studiese en uit postmarketingervaring | |
Systeem/orgaanklasse | Bijwerking |
Infecties en parasitaire aandoeningen | |
zeer vaak | Vulvovaginale candidiasisb,j |
vaak | Balanitis of balanoposthitisb,k, urineweginfectiec (pyelonefritis en urosepsis zijn postmarketing gemeld) |
niet bekend | Necrotiserende fasciitis van het perineum (fournier-gangreen)d |
Immuunsysteemaandoeningen | |
zelden | Anafylactische reactie |
Voedings- en stofwisselingsstoornissen | |
zeer vaak | Hypoglykemie in combinatie met insuline of sulfonylureumderivaatc |
soms | Dehydratiea |
zelden | Diabetische ketoacidoseb |
Zenuwstelselaandoeningen | |
soms | Duizeligheid houdings-afhankelijka, syncopea |
Bloedvataandoeningen | |
soms | Hypotensiea, orthostatische hypotensiea |
Maagdarmstelselaandoeningen | |
vaak | Constipatie, dorstf, nausea |
Huid- en onderhuidaandoeningen | |
soms | Fotosensitiviteit, rashg, urticaria |
zelden | Angio-oedeem |
Skeletspierstelsel- en bindweefselaandoeningen | |
soms | Botbreukh |
Nier- en urinewegaandoeningen | |
vaak | Polyurie of pollakisuriei |
soms | Nierfalen (voornamelijk in de context van volumedepletie) |
Onderzoeken | |
vaak | Dyslipidemiel, hematocriet verhoogdb,m |
soms | Bloed creatinine verhoogdb,n, bloed ureum verhoogdb,o, bloed kalium verhoogdb,p, bloed fosfaat verhoogdq |
Chirurgische en medische verrichtingen | |
soms | Amputaties van onderste ledematen (hoofdzakelijk van de teen en middenvoet), vooral bij patiënten met een hoog risico op hartziekteb |
a Gerelateerd aan volumedepletie; zie rubriek 4.4 en beschrijving van bijwerking hieronder. | |
Beschrijving van geselecteerde bijwerkingen
Diabetische ketoacidose
In een langetermijnstudie naar nieruitkomsten bij volwassen patiënten met type 2-diabetes en diabetische nierschade, waren de incidentiepercentages van vastgestelde voorvallen van diabetische ketoacidose (DKA) respectievelijk 0,21 (0,5%, 12/2.200) en 0,03 (0,1%, 2/2.197) per 100 patiëntjaren van follow-up voor 100 mg canagliflozine en placebo; van de 14 patiënten met DKA hadden 8 (7 met 100 mg canagliflozine en 1 met placebo) vóór behandeling een eGFR van 30 tot ˂ 45 ml/min/1,73 m2 (zie rubriek 4.4).
Amputatie van de onderste ledematen
Bij patiënten met type 2-diabetes die aan een vastgestelde cardiovasculaire aandoening leden of die ten minste 2 risicofactoren voor een cardiovasculaire aandoening hadden, werd canagliflozine in verband gebracht met een verhoogd risico op amputatie van de onderste ledematen. Dit werd waargenomen in het geïntegreerde CANVAS-programma bestaande uit CANVAS en CANVAS-R, twee grote, gerandomiseerde, placebogecontroleerde langetermijnstudies waarin 10.134 volwassen patiënten werden beoordeeld. De onbalans trad al binnen de eerste 26 weken van de behandeling op. Patiënten in CANVAS en CANVAS-R werden gedurende een gemiddelde periode van respectievelijk 5,7 en 2,1 jaar gevolgd. Ongeacht behandeling met canagliflozine of placebo was het amputatierisico het hoogst bij patiënten die op baseline een voorgeschiedenis hadden van een eerdere amputatie, perifere vasculaire ziekte en neuropathie. Het risico op amputatie van de onderste ledematen was niet dosisafhankelijk. De amputatieresultaten van het geïntegreerde CANVAS-programma zijn weergegeven in tabel 3.
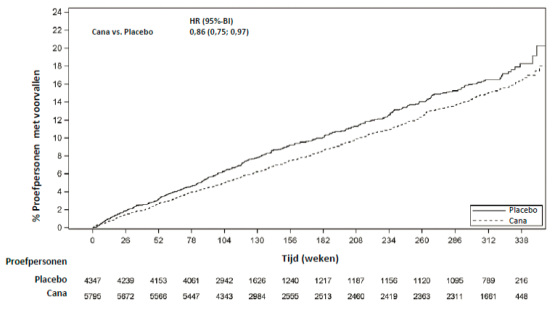
Er was geen verschil in risico op amputatie van de onderste ledematen gerelateerd aan het gebruik van 100 mg canagliflozine ten opzichte van placebo (respectievelijk 1,2 versus 1,1 voorvallen per 100 patiëntjaren [HR: 1,11; 95%-BI 0,79; 1,56]) in CREDENCE, een langetermijnstudie naar nieruitkomsten bij 4.397 volwassen patiënten met type 2-diabetes en diabetische nierschade (zie rubriek 4.4). In andere studies met canagliflozine bij type 2-diabetes, waarin een algemene diabetische populatie van 8.114 volwassen patiënten werd geïncludeerd, werd geen verschil in risico op amputatie van de onderste ledematen waargenomen ten opzichte van controlepatiënten.
Tabel 3: Geïntegreerde analyse van amputaties in CANVAS EN CANVAS-R | ||
| Placebo | canagliflozine |
Totaalaantal proefpersonen met amputaties, n (%) | 47 (1,1) | 140 (2,4) |
Incidentiepercentage (per 100 patiëntjaren) | 0,34 | 0,63 |
HR (95%-BI) t.o.v. placebo |
| 1,97 (1,41; 2,75) |
Kleine amputatie, n (%)* | 34/47 (72,3) | 99/140 (70,7) |
Grote amputatie, n (%)† | 13/47 (27,7) | 41/140 (29,3) |
Opmerking: de incidentie is gebaseerd op het aantal patiënten met ten minste één amputatie, niet op het totale aantal amputaties. De follow-up van een patiënt wordt berekend op basis van dag 1 tot de datum van de eerste amputatie. Sommige patiënten hadden meer dan één amputatie. Het percentage van kleine en grote amputaties is gebaseerd op het hoogste amputatieniveau bij elke patiënt. | ||
Van de proefpersonen in het CANVAS-programma die een amputatie hadden ondergaan, waren de teen en middenvoet de meest voorkomende plaatsen (71%) in beide behandelgroepen (tabel 3). Meerdere amputaties (van beide onderste ledematen in sommige gevallen) werden niet vaak en in vergelijkbare percentages waargenomen in beide behandelgroepen.
Infecties in de onderste ledematen, diabetische voetzweren, perifere arteriële ziekte en gangreen waren de meest voorkomende medische voorvallen die in verband werden gebracht met de noodzaak van een amputatie in beide behandelgroepen (zie rubriek 4.4).
Bijwerkingen gerelateerd aan volumedepletie
In de gepoolde analyse van de vier 26 weken durende placebogecontroleerde studies bij volwassenen was de incidentie van alle bijwerkingen gerelateerd aan volumedepletie (bijvoorbeeld houdingsafhankelijke duizeligheid, orthostatische hypotensie, hypotensie, dehydratie, en syncope) 1,2% voor canagliflozine 100 mg, 1,3% voor canagliflozine 300 mg, en 1,1% voor placebo. In de twee actief gecontroleerde studies was de incidentie met Invokana-behandeling vergelijkbaar met de controlegroepen.
In een van de specifieke cardiovasculaire langetermijnstudies (CANVAS), waarin volwassen patiënten in het algemeen ouder waren en een hoger percentage aan diabetescomplicaties hadden, waren de incidentiepercentages van bijwerkingen gerelateerd aan volumedepletie 2,3 met canagliflozine 100 mg, 2,9 met canagliflozine 300 mg en 1,9 met placebo, voorvallen per 100 patiëntjaren.
Om de risicofactoren voor deze bijwerkingen na te gaan werd een uitgebreidere gepoolde analyse uitgevoerd van volwassen patiënten (N = 12.441) uit 13 gecontroleerde fase III‑ en fase IV-studies met beide doses van canagliflozine. In deze gepoolde analyse hadden patiënten op lisdiuretica, patiënten met een baseline-eGFR van 30 ml/min/1,73 m2 tot < 60 ml/min/1,73 m2 en patiënten van ≥ 75 jaar in het algemeen hogere incidenties van deze bijwerkingen. Voor patiënten op lisdiuretica waren de incidentiepercentages 5,0 met canagliflozine 100 mg en 5,7 met canagliflozine 300 mg, tegenover 4,1 voorvallen per 100 patiëntjaren van blootstelling in de controlegroep. Voor patiënten met een baseline-eGFR van 30 ml/min/1,73 m2 tot < 60 ml/min/1,73 m2 waren de incidentiepercentages 5,2 met canagliflozine 100 mg en 5,4 met canagliflozine 300 mg, tegenover 3,1 voorvallen per 100 patiëntjaren van blootstelling in de controlegroep. Bij patiënten van ≥ 75 jaar waren de incidentiepercentages 5,3 met canagliflozine 100 mg en 6,1 met canagliflozine 300 mg, tegenover 2,4 voorvallen per 100 patiëntjaren van blootstelling in de controlegroep (zie rubriek 4.2 en 4.4).
In een langetermijnstudie naar nieruitkomsten bij volwassen patiënten met type 2-diabetes en diabetische nierschade was het incidentiepercentage van voorvallen gerelateerd aan volumedepletie 2,84 en 2,35 voorvallen per 100 patiëntjaren voor respectievelijk 100 mg canagliflozine en placebo. Een toename van het incidentiepercentage werd waargenomen bij een dalende eGFR. Bij proefpersonen met een eGFR van 30 tot < 45 ml/min/1,73 m2 was het incidentiepercentage voor volumedepletie hoger in de canagliflozinegroep (4,91 voorvallen per 100 patiëntjaren) vergeleken met de placebogroep (2,60 voorvallen per 100 patiëntjaren); in de subgroepen met eGFR ≥ 45 tot < 60 en eGFR 60 tot< 90 ml/min/1,73 m2 was het incidentiepercentage tussen de groepenechter vergelijkbaar.
In de specifieke cardiovasculaire studie en de uitgebreidere gepoolde analyse, alsmede in een specifieke studie naar nieruitkomsten bij volwassenen, was het aantal stopzettingen als gevolg van bijwerkingen gerelateerd aan volumedepletie en ernstige bijwerkingen gerelateerd aan volumedepletie met canagliflozine niet verhoogd.
Hypoglykemie bij add‑on‑therapie met insuline of insuline-secretagogen
De frequentie van hypoglykemie was laag (ongeveer 4%) in alle behandelgroepen, inclusief placebo, bij gebruik als monotherapie of als add‑on‑therapie bij metformine. Als canagliflozine werd toegevoegd aan behandeling met insuline, werd hypoglykemie waargenomen bij respectievelijk 49,3%, 48,2% en 36,8% van de volwassen patiënten behandeld met canagliflozine 100 mg, canagliflozine 300 mg en placebo, en kwam ernstige hypoglykemie voor bij 1,8%, 2,7% en 2,5% van de volwassen patiënten behandeld met respectievelijk canagliflozine 100 mg, canagliflozine 300 mg en placebo. Als canagliflozine werd toegevoegd aan behandeling met een sulfonylureumderivaat, werd hypoglykemie waargenomen bij respectievelijk 4,1%, 12,5% en 5,8% van de volwassen patiënten behandeld met canagliflozine 100 mg, canagliflozine 300 mg en placebo (zie rubriek 4.2 en 4.5).
Genitale schimmelinfecties
Vulvovaginale candidiasis (waaronder vulvovaginitis en vulvovaginale mycotische infectie) werd gemeld bij respectievelijk 10,4% en 11,4% van de volwassen vrouwelijke patiënten die werden behandeld met canagliflozine 100 mg en canagliflozine 300 mg, tegenover 3,2% bij vrouwelijke patiënten behandeld met placebo. De meeste meldingen van vulvovaginale candidiasis gebeurden tijdens de eerste vier maanden van de behandeling met canagliflozine. Onder vrouwelijke patiënten die canagliflozine gebruikten, kreeg 2,3% meer dan één infectie. In totaal stopte 0,7% van alle vrouwelijke patiënten met canagliflozine vanwege vulvovaginale candidiasis (zie rubriek 4.4). In het CANVAS-programma was de mediane infectieduur bij de canagliflozinegroep langer dan bij de placebogroep.
Candida‑balanitis of -balanoposthitis trad bij volwassen mannelijke patiënten op meteen percentage van 2,98 en 0,79 voorvallen per 100 patiëntjaren voor respectievelijk canagliflozine en placebo. Onder mannelijke patiënten die canagliflozine gebruikten, had 2,4% meer dan één infectie. Stoppen met canagliflozine door mannelijke patiënten vanwege candida-balanitis of -balanoposthitis vond plaats met een percentage van 0,37 voorvallen per 100 patiëntjaren. Phimosis werd gemeld meteen percentage van 0,39 en 0,07 voorvallen per 100 patiëntjaren voor respectievelijk canagliflozine en placebo. Een circumcisie werd uitgevoerd met een percentage van 0,31 en 0,09 voorvallen per 100 patiëntjaren voor respectievelijk canagliflozine en placebo (zie rubriek 4.4).
Urineweginfecties
In klinische studies bij volwassenen werden urineweginfecties vaker gemeld met canagliflozine 100 mg en 300 mg (respectievelijk 5,9% en 4,3%), tegenover 4,0% met placebo. De meeste infecties waren licht tot matig van aard en het aantal ernstige bijwerkingen nam niet toe. In deze studies reageerden proefpersonen op de standaardbehandelingen terwijl de behandeling met canagliflozine werd voortgezet.
Na het in de handel brengen zijn echter gevallen gemeld van gecompliceerde urineweginfecties, waaronder pyelonefritis en urosepsis, bij patiënten die werden behandeld met canagliflozine. Dit leidde vaak tot het onderbreken van de behandeling.
Botbreuk
In een cardiovasculaire studie (CANVAS) bij 4.327 behandelde volwassen proefpersonen met een vastgestelde cardiovasculaire aandoening of ten minste twee risicofactoren voor een cardiovasculaire aandoening waren de incidentiepercentages van alle toegekende botbreuken 1,6, 1,8 en 1,1 per 100 patiëntjaren van follow-up voor respectievelijk 100 mg canagliflozine, 300 mg canagliflozine en placebo, waarbij de onbalans in breuken aanvankelijk optrad binnen de eerste 26 weken van de behandeling.
In twee andere langetermijnstudies bij volwassenen en in studies bij volwassenen die bij de algemene diabetespopulatie werden uitgevoerd, werd geen verschil in het risico op breuken waargenomen met canagliflozine vergeleken met controle. In een tweede cardiovasculaire studie (CANVAS-R) onder 5.807 behandelde volwassen proefpersonen met een vastgestelde cardiovasculaire aandoening of ten minste twee risicofactoren voor een cardiovasculaire aandoening waren de incidentiepercentages van alle toegekende botbreuken 1,1 en 1,3 voorvallen per 100 patiëntjaren van follow-up voor respectievelijk canagliflozine en placebo.
In een langetermijnstudie naar nieruitkomsten bij 4.397 behandelde volwassen proefpersonen met type 2-diabetes en diabetische nierschade, waren de incidentiepercentages van alle vastgestelde botbreuken 1,2 voorvallen per 100 patiëntjaren van follow-up voor zowel 100 mg canagliflozine als placebo. In andere studies met canagliflozine bij type 2-diabetes, waarin een algemene diabetes-populatie van 7.729 volwassen patiënten werd geïncludeerden waarin botbreuken waren vastgesteld, waren de incidentiepercentages van alle vastgestelde botbreuken 1,2 en 1,1 per 100 patiëntjaren van follow-up voor respectievelijk canagliflozine en controle. Na 104 weken behandeling had canagliflozine geen ongunstig effect op de botmineraaldichtheid.
Bijzondere populaties
Ouderen
In een gepoolde analyse van 13 placebo‑gecontroleerde en actief‑gecontroleerde studies was het veiligheidsprofiel van canagliflozine bij oudere patiënten in het algemeen consistent met dat bij jongere patiënten. Patiënten van ≥ 75 jaar hadden een hogere incidentie van bijwerkingen gerelateerd aan volumedepletie (zoals houdingsafhankelijke duizeligheid, orthostatische hypotensie, hypotensie), met incidentiepercentages van 5,3, 6,1 en 2,4 voorvallen per 100 patiëntjaren van blootstelling aan respectievelijk canagliflozine 100 mg, canagliflozine 300 mg en in de controlegroep. Afnames van de eGFR (‑3,4 en ‑4,7 ml/min/1,73 m2) werden gemeld met respectievelijk canagliflozine 100 mg en canagliflozine 300 mg, tegenover ‑4,2 ml/min/1,73 m2 in de controlegroep. De gemiddelde baseline-eGFR bedroeg 62,5, 64,7 en 63,5 ml/min/1,73 m2 voor respectievelijk canagliflozine 100 mg, canagliflozine 300 mg en de controlegroep (zie rubriek 4.2 en 4.4).
Nierinsufficiëntie bij volwassen patiënten met onvoldoende gereguleerde type 2-diabetes mellitus
Volwassen patiënten met op baseline een eGFR van < 60 ml/min/1,73 m2 hadden een hogere incidentie van bijwerkingen gerelateerd aan volumedepletie (bijvoorbeeld houdingsafhankelijke duizeligheid, orthostatische hypotensie, hypotensie), met incidentiepercentages van respectievelijk 5,3, 5,1 en 3,1 voorvallen per 100 patiëntjaren van blootstelling aancanagliflozine 100 mg, canagliflozine 300 mg en placebo (zie rubriek 4.2 en 4.4).
Het algehele incidentiepercentage van verhoogde serumkaliumconcentratie was hoger bij patiënten met matige nierinsufficiëntie, met incidentiepercentages van respectievelijk 4,9, 6,1 en 5,4 voorvallen per 100 patiëntjaren van blootstelling aan canagliflozine 100 mg, canagliflozine 300 mg en placebo. In het algemeen waren de verhogingen van voorbijgaande aard en was er geen specifieke behandeling nodig.
Met beide doses van canagliflozine werden bij patiënten met matige nierinsufficiëntie verhogingen van het serumcreatinine van 9,2 µmol/l en van BUN van ongeveer 1,0 mmol/lwaargenomen.
De incidentiepercentages van grotere afnames van de eGFR (> 30%) op enig moment tijdens de behandeling waren 7,3, 8,1 en 6,5 voorvallen per 100 patiëntjaren van blootstelling aan respectievelijk canagliflozine 100 mg, canagliflozine 300 mg en placebo. Bij de laatste post-baseline waarde waren de incidentiepercentages van dergelijke afnames 3,3 voor patiënten behandeld met canagliflozine 100 mg, 2,7 met canagliflozine 300 mg en 3,7 voorvallen per 100 patiëntjaren van blootstelling met placebo (zie rubriek 4.4).
Patiënten behandeld met canagliflozine maakten, ongeacht de baseline-eGFR, een initiële afname van de gemiddelde eGFR door. Daarna handhaafde de eGFR zich of steeg de waarde geleidelijk tijdens het voortzetten van de behandeling. Na stopzetting van de behandeling keerde de gemiddelde eGFR terug naar de waarde bij baseline, wat erop duidt dat hemodynamische veranderingen mogelijk een rol spelen bij deze veranderingen in nierfunctie.
Nierinsufficiëntie bij volwassen patiënten met diabetische nierschade bij type 2-diabetes mellitus
In een langetermijnstudie naar nieruitkomsten bij volwassen patiënten met type 2-diabetes en diabetische nierschade was de incidentie van niergerelateerde voorvallen in beide groepen frequent maar minder frequent in de canagliflozinegroep (5,71 voorvallen per 100 patiëntjaren) vergeleken met de placebogroep (7,91 voorvallen per 100 patiëntjaren). Ernstige en hevige niergerelateerde voorvallen kwamen ook minder vaak voor in de canagliflozinegroep versus placebo. De incidentiepercentages van niergerelateerde voorvallen voor alle drie de eGFR-groepen waren lager bij canagliflozine ten opzichte van placebo; het hoogste incidentiepercentage van niergerelateerde voorvallen werd gezien in de eGFR-groep van 30 tot< 45 ml/min/1,73 m2 (9,47 versus 12,80 voorvallen per 100 patiëntjaren voor respectievelijk canagliflozine versus placebo).
In de langetermijnstudie naar nieruitkomsten werd geen verschil in serumkalium, geen toename van bijwerkingen van hyperkaliëmie en geen absolute (> 6,5 mEq/l) of relatieve (> bovengrens van standaard en > 15% toename ten opzichte van baseline) stijging van serumkalium waargenomen bij 100 mg canagliflozine ten opzichte van placebo.
In het algemeen werd er geen onbalans tussen behandelgroepen waargenomen voor afwijkingen in fosfaat, zowel over het geheel gezien als in elke eGFR-categorie (45 tot< 60 of 30 tot< 45 ml/min/1,73 m2 [CrCl 45 tot < 60 of 30 tot < 45 ml/min]).
Pediatrische populatie
In de DIA3018-studie werden 171 kinderen van 10 jaar en ouder met type 2‑diabetes mellitus als volgt behandeld: 84 deelnemers kregen canagliflozine en 87 kregen placebo (zie rubriek 5.1). Algemeen genomen waren de frequentie, het type en de ernst van de bijwerkingen bij kinderen van 10 jaar en ouder vergelijkbaar met die waargenomen in de volwassen populatie. De volgende tijdens de behandeling optredende bijwerkingen kwamen vaker voor bij canagliflozine vergeleken met placebo bij kinderen: hoofdpijn, nasofaryngitis, infectie van de urinewegen en braken. Genitale mycotische of bacteriële infecties werden in kleine aantallen gemeld bij degenen die canagliflozine kregen en geen bij placebo. Geen van de tijdens de behandeling optredende bijwerkingen waren ernstig of zwaar.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg worden verzocht alle vermoedelijke bijwerkingen te melden:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
Luxemburg
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Website: www.guichet.lu/pharmacovigilance
Nederland
Nederlands Bijwerkingen Centrum Lareb
Website: www.lareb.nl
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Janssen‑Cilag International NV
Turnhoutseweg 30
B‑2340 Beerse
België
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Invokana 100 mg filmomhulde tabletten
EU/1/13/884/001 (10 filmomhulde tabletten)
EU/1/13/884/002 (30 filmomhulde tabletten)
EU/1/13/884/003 (90 filmomhulde tabletten)
EU/1/13/884/004 (100 filmomhulde tabletten)
Invokana 300 mg filmomhulde tabletten
EU/1/13/884/005 (10 filmomhulde tabletten)
EU/1/13/884/006 (30 filmomhulde tabletten)
EU/1/13/884/007 (90 filmomhulde abletten)
EU/1/13/884/008 (100 filmomhulde tabletten)
10. DATUM VAN HERZIENING VAN DE TEKST
08/2025
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau (http://www.ema.europa.eu).
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3091212 | INVOKANA 100 MG FILMOMH TABL 30 X 100 MG | A10BK02 | € 62,95 | - | Ja | € 2 | € 1 |
| 3091220 | INVOKANA 100 MG FILMOMH TABL 90 X 100 MG | A10BK02 | € 137,25 | - | Ja | € 2 | € 1 |
| 3091238 | INVOKANA 300 MG FILMOMH TABL 90 X 300 MG | A10BK02 | € 200,38 | - | Ja | € 2 | € 1 |
| 3091246 | INVOKANA 300 MG FILMOMH TABL 30 X 300 MG | A10BK02 | € 89,89 | - | Ja | € 2 | € 1 |
 1
1