1. NAAM VAN HET GENEESMIDDEL
Ultibro Breezhaler 85 microgram/43 microgram inhalatiepoeder in harde capsules
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke capsule bevat 143 microgram indacaterolmaleaat, gelijk aan 110 microgram indacaterol, en 63 microgram glycopyrroniumbromide, gelijk aan 50 microgram glycopyrronium.
Elke afgeleverde dosis (de dosis die het mondstuk van de inhalator verlaat) bevat 110 microgram indacaterolmaleaat, gelijk aan 85 microgram indacaterol, en 54 microgram glycopyrroniumbromide, gelijk aan 43 microgram glycopyrronium.
Hulpstof(fen) met bekend effect
Elke capsule bevat 23,5 mg lactose (als monohydraat).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Inhalatiepoeder in harde capsule (inhalatiepoeder).
Capsules met een doorzichtige gele bovenste helft en een natuurlijk doorzichtige onderste helft die een wit tot nagenoeg wit poeder bevatten, met de productcode “IGP110.50” in het blauw bedrukt onder twee blauwe balken op de onderste helft en het bedrijfslogo (![]() ) in zwart bedrukt op de bovenste helft.
) in zwart bedrukt op de bovenste helft.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Ultibro Breezhaler is geïndiceerd als onderhoudstherapie voor bronchodilatatie om symptomen te verlichten bij volwassen patiënten met chronisch obstructieve longziekte (COPD).
4.2 Dosering en wijze van toediening
Dosering
De aanbevolen dosis is inhalatie van de inhoud van één capsule eenmaal daags met behulp van de Ultibro Breezhaler-inhalator.
Het wordt aanbevolen Ultibro Breezhaler elke dag op hetzelfde tijdstip toe te dienen. Als een dosis wordt overgeslagen moet deze zo snel mogelijk worden ingenomen op dezelfde dag. De patiënten moeten worden geïnstrueerd dat ze niet meer dan één dosis per dag mogen innemen.
Bijzondere patiëntgroepen
Ouderen
Ultibro Breezhaler kan bij oudere patiënten (75 jaar of ouder) in de aanbevolen dosering worden gebruikt.
Gestoorde nierfunctie
Ultibro Breezhaler kan in de aanbevolen dosis worden gebruikt bij patiënten met een licht tot matig gestoorde nierfunctie. Bij patiënten met een ernstig gestoorde nierfunctie of terminale nierziekte die dialyse nodig hebben, mag Ultibro Breezhaler alleen gebruikt worden als de verwachte voordelen opwegen tegen het mogelijke risico (zie rubriek 4.4 en 5.2).
Gestoorde leverfunctie
Ultibro Breezhaler kan in de aanbevolen dosis worden gebruikt bij patiënten met een licht tot matige leverfunctiestoornis. Er zijn geen gegevens beschikbaar over het gebruik van Ultibro Breezhaler bij patiënten met een ernstige leverfunctiestoornis, daarom is voorzichtigheid geboden bij deze patiënten (zie rubriek 5.2).
Pediatrische patiënten
Er is geen relevante toepassing van Ultibro Breezhaler bij pediatrische patiënten (tot 18 jaar) voor de indicatie COPD. De veiligheid en werkzaamheid van Ultibro Breezhaler bij kinderen zijn niet vastgesteld. Er zijn geen gegevens beschikbaar.
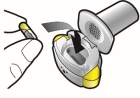
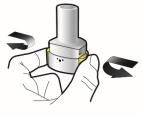
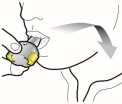
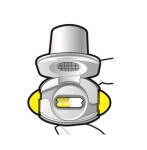
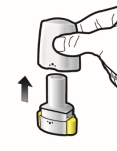
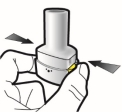
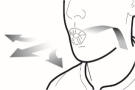
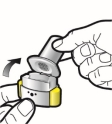
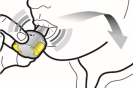
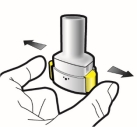
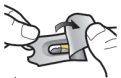
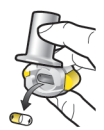
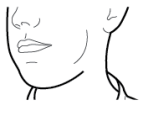
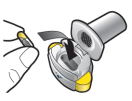
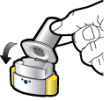
Wijze van toediening
Alleen voor inhalatie. De capsules mogen niet worden ingeslikt.
De capsules mogen alleen worden toegediend met de Ultibro Breezhaler-inhalator (zie rubriek 6.6). De inhalator die wordt geleverd bij elk nieuw medisch voorschrift dient te worden gebruikt.
De patiënten moeten instructies krijgen over hoe ze het geneesmiddel correct moeten toedienen. Patiënten die geen verbetering van de ademhaling ervaren, moet gevraagd worden of ze het geneesmiddel inslikken in plaats van te inhaleren.
Voor instructies over het gebruik van het geneesmiddel voorafgaand aan toediening, zie rubriek 6.6.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stoffen of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
De weergave van het veiligheidsprofiel is gebaseerd op de ervaring met Ultibro Breezhaler en de individuele werkzame bestanddelen.
Samenvatting van het veiligheidsprofiel
De ervaring met de veiligheid met Ultibro Breezhaler bestond uit blootstelling tot 15 maanden in de aanbevolen therapeutische dosis.
Ultibro Breezhaler liet vergelijkbare bijwerkingen zien als de individuele bestanddelen. Aangezien Ultibro Breezhaler indacaterol en glycopyrronium bevat, kunnen het type en de ernst van de bijwerkingen geassocieerd met elk van deze bestanddelen verwacht worden bij de combinatie.
Het veiligheidsprofiel wordt gekarakteriseerd door typische anticholinerge en bèta‑adrenerge symptomen gerelateerd aan de individuele bestanddelen van de combinatie. Andere veel voorkomende bijwerkingen gerelateerd aan het geneesmiddel (ten minste 3% van de patiënten met Ultibro Breezhaler en tevens meer dan bij placebo) waren hoest, nasofaryngitis en hoofdpijn.
Samenvatting van bijwerkingen in tabelvorm
De bijwerkingen die gevonden werden tijdens klinische studies en uit postmarketingbronnen worden weergegeven volgens de MedDRA-systeem/orgaanklassen (tabel 1). Binnen elke systeem/orgaanklasse worden de bijwerkingen gerangschikt in volgorde van frequentie, met de meest voorkomende reacties eerst. Binnen elke frequentiecategorie worden de bijwerkingen gepresenteerd in dalende volgorde van ernst. Bovendien is de overeenstemmende frequentiecategorie voor elke bijwerking gebaseerd op de volgende conventie: zeer vaak (≥1/10); vaak (≥1/100, <1/10); soms (≥1/1.000, <1/100); zelden (≥1/10.000, <1/1.000); zeer zelden (<1/10.000); niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Tabel 1 Bijwerkingen
Bijwerkingen | Frequentiecategorie |
Infecties en parasitaire aandoeningen | |
Bovenste luchtweginfectie | Zeer vaak |
Nasofaryngitis | Vaak |
Urineweginfectie | Vaak |
Sinusitis | Vaak |
Rinitis | Vaak |
Immuunsysteemaandoeningen | |
Overgevoeligheid | Vaak |
Angio‑oedeem2 | Soms |
Voedings- en stofwisselingsstoornissen | |
Hyperglykemie en diabetes mellitus | Vaak |
Psychische stoornissen | |
Slapeloosheid | Soms |
Zenuwstelselaandoeningen | |
Duizeligheid | Vaak |
Hoofdpijn | Vaak |
Paresthesie | Zelden |
Oogaandoeningen | |
Glaucoom1 | Soms |
Hartaandoeningen | |
Ischemische hartziekte | Soms |
Atriumfibrillatie | Soms |
Tachycardie | Soms |
Palpitaties | Soms |
Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen | |
Hoest | Vaak |
Orofaryngeale pijn waaronder irritatie van de keel | Vaak |
Paradoxale bronchospasmen | Soms |
Dysfonie2 | Soms |
Bloedneus | Soms |
Maagdarmstelselaandoeningen | |
Dyspepsie | Vaak |
Tandcariës | Vaak |
Gastro-enteritis | Soms |
Droge mond | Soms |
Huid- en onderhuidaandoeningen | |
Jeuk/uitslag | Soms |
Skeletspierstelsel- en bindweefselaandoeningen | |
Skeletspierpijn | Soms |
Spierspasme | Soms |
Myalgie | Soms |
Pijn in extremiteiten | Soms |
Nier- en urinewegaandoeningen | |
Blaasobstructie en urineretentie | Vaak |
Algemene aandoeningen en toedieningsplaatsstoornissen | |
Pyrexie1 | Vaak |
Thoracale pijn | Vaak |
Oedeem perifeer | Soms |
Vermoeidheid | Soms |
1 Bijwerking waargenomen met Ultibro Breezhaler maar niet met de individuele bestanddelen.
2 Meldingen uit postmarketingervaring; frequenties zijn echter berekend op basis van klinische studiegegevens.
Beschrijving van geselecteerde bijwerkingen
Hoest kwam vaak voor, maar was meestal van lichte aard.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Ierland
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/13/862/001-008
10. DATUM VAN HERZIENING VAN DE TEKST
24.07.2025
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau http://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 3085636 | ULTIBRO BREEZHALER 85MCG/43MCG INHAL PDR CAPS 90 | R03AL04 | € 129,09 | - | Ja | € 15,9 | € 10,5 |
| 3085644 | ULTIBRO BREEZHALER 85MCG/43MCG INHAL PDR CAPS 30 | R03AL04 | € 42,28 | - | Ja | € 10,6 | € 6,3 |