1. NAAM VAN HET GENEESMIDDEL
Onbrez Breezhaler 150 microgram inhalatiepoeder in harde capsules
Onbrez Breezhaler 300 microgram inhalatiepoeder in harde capsules
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Onbrez Breezhaler 150 microgram inhalatiepoeder in harde capsules
Eén capsule bevat indacaterolmaleaat overeenkomend met 150 microgram indacaterol.
De afgeleverde dosis die het mondstuk van de inhalator verlaat is indacaterolmaleaat overeenkomend met 120 microgram indacaterol.
Hulpstof(fen) met bekend effect
Eén capsule bevat 24,8 mg lactose (als monohydraat).
Onbrez Breezhaler 300 microgram inhalatiepoeder in harde capsules
Eén capsule bevat indacaterolmaleaat overeenkomend met 300 microgram indacaterol.
De afgeleverde dosis die het mondstuk van de inhalator verlaat is indacaterolmaleaat overeenkomend met 240 microgram indacaterol.
Hulpstof(fen) met bekend effect
Eén capsule bevat 24,6 mg lactose (als monohydraat).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Inhalatiepoeder in harde capsule
Onbrez Breezhaler 150 microgram inhalatiepoeder in harde capsules
Doorzichtige (kleurloze) capsules die een wit poeder bevatten, met “IDL 150” in het zwart geprint boven een zwarte balk en het bedrijfslogo in het zwart geprint onder de zwarte balk.
Onbrez Breezhaler 300 microgram inhalatiepoeder in harde capsules
Doorzichtige (kleurloze) capsules die een wit poeder bevatten, met “IDL 300” in het blauw geprint boven een blauwe balk en het bedrijfslogo in het blauw geprint onder de blauwe balk.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Onbrez Breezhaler is geïndiceerd als een bronchodilatator voor de onderhoudsbehandeling van luchtwegobstructies bij volwassenen met chronisch obstructieve longziekte (COPD).
4.2 Dosering en wijze van toediening
Dosering
De aanbevolen dosis is de inhalatie van de inhoud van één 150 microgram capsule eenmaal daags, met behulp van de Onbrez Breezhaler inhalator. De dosis mag alleen worden verhoogd op medisch advies.
De inhalatie van de inhoud van één 300 microgram capsule eenmaal daags met behulp van de Onbrez Breezhaler inhalator blijkt additioneel klinisch voordeel te geven met betrekking tot kortademigheid, met name bij patiënten met ernstige COPD. De maximale dosis is 300 microgram eenmaal daags.
Onbrez Breezhaler dient elke dag op hetzelfde tijdstip te worden gebruikt.
Als een dosis wordt gemist dient de volgende dosis de volgende dag op het gebruikelijke tijdstip te worden gebruikt.
Speciale patiëntengroepen
Ouderen
De maximale plasmaconcentratie en algehele systemische blootstelling nemen toe met de leeftijd, maar er is geen dosisaanpassing nodig bij ouderen (65 jaar en ouder).
Leverfunctiestoornis
Er is geen dosisaanpassing nodig bij patiënten met milde of matige leverfunctiestoornissen. Er zijn geen gegevens beschikbaar over het gebruik van Onbrez Breezhaler bij patiënten met een ernstige leverfunctiestoornis.
Nierfunctiestoornis
Er is geen dosisaanpassing nodig bij patiënten met een nierfunctiestoornis.
Pediatrische patiënten
Er is geen relevante toepassing van Onbrez Breezhaler bij pediatrische patiënten (jonger dan 18 jaar).
Wijze van toediening
Uitsluitend voor inhalatie. Onbrez Breezhaler capsules dienen niet te worden ingeslikt.
De capsules dienen alleen direct voor het gebruik uit de blisterverpakking te worden gehaald.
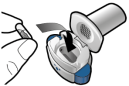
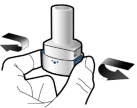
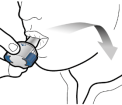
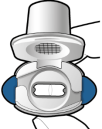
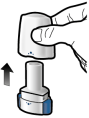
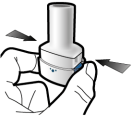
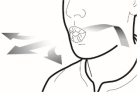
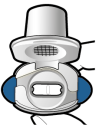
De capsules dienen alleen met de Onbrez Breezhaler inhalator te worden gebruikt (zie rubriek 6.6). De Onbrez Breezhaler inhalator die bij elk nieuw voorschrift geleverd wordt, moet worden gebruikt.
Patiënten moet worden uitgelegd hoe zij het product correct gebruiken. Patiënten die geen verbetering ervaren bij het ademhalen, moet worden gevraagd of ze het geneesmiddel inslikken in plaats van het te inhaleren.
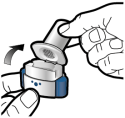
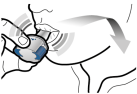
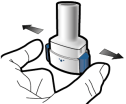
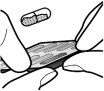
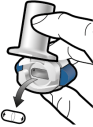
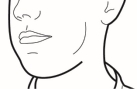
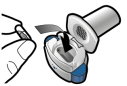
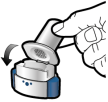
Voor instructies over het gebruik van het geneesmiddel voorafgaand aan toediening, zie rubriek 6.6.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De bijwerkingen die het vaakst voorkomen bij de aanbevolen doses waren nasofaryngitis (14,3%), infectie van de bovenste luchtwegen (14,2%), hoest (8,2%), hoofdpijn (3,7%) en spierspasmen (3,5%). Deze waren bij de grote meerderheid mild of matig en werden minder frequent bij voortzetting van de behandeling.
Bij de aanbevolen doses laat het bijwerkingenprofiel van Onbrez Breezhaler bij patiënten met COPD klinisch niet-significante systemische effecten van bèta-2-adrenerge stimulatie zien. Gemiddelde veranderingen in hartslag waren minder dan één hartslag per minuut. Tachycardie kwam niet vaak voor en werd in een vergelijkbare frequentie als bij placebobehandeling gemeld. Relevante QTcF-verlenging was niet detecteerbaar in vergelijking met placebo. De frequentie van opmerkelijke QTcF-intervallen [d.w.z. >450 ms (mannen) en >470 ms (vrouwen)] en meldingen van hypokaliëmie waren vergelijkbaar met placebo. De gemiddelde maximale veranderingen in bloedglucosespiegels waren vergelijkbaar voor Onbrez Breezhaler en placebo.
Tabel met samenvatting van bijwerkingen
Het Onbrez Breezhaler Fase III klinisch ontwikkelingsprogramma omvatte patiënten met een klinische diagnose van matige tot ernstige COPD. 4.764 patiënten kregen indacaterol tot maximaal één jaar in doses tot twee keer de maximaal aanbevolen dosis. Van deze patiënten werden er 2.611 behandeld met eenmaal daags 150 microgram en werden 1.157 patiënten behandeld met eenmaal daags 300 microgram. Ongeveer 41% van de patiënten had ernstige COPD. De gemiddelde leeftijd van de patiënten was 64 jaar. 48% van de patiënten was 65 jaar of ouder, en de meerderheid (80%) was blank.
Bijwerkingen in Tabel 1 zijn gerangschikt volgens de MedDRA systeem/orgaanklassen in de COPD veiligheidsgegevensbank. Binnen elke systeemorgaanklasse zijn de bijwerkingen gerangschikt in afnemende volgorde volgens de volgende afspraak: Zeer vaak (1/10); vaak (1/100, <1/10); soms (≥1/1.000, <1/100); zelden (≥1/10.000, <1/1.000); zeer zelden (<1/10.000), niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Tabel 1 Bijwerkingen
Bijwerkingen | Categorie van frequentie |
Infecties en parasitaire aandoeningen | |
Nasofaryngitis | Zeer vaak |
Bovenste luchtweginfectie | Zeer vaak |
Sinusitis | Vaak |
Immuunsysteemaandoeningen | |
Overgevoeligheid1 | Soms |
Voedings- en stofwisselingsstoornissen | |
Diabetes mellitus en hyperglykemie | Vaak |
Zenuwstelselaandoeningen | |
Hoofdpijn | Vaak |
Duizeligheid | Vaak |
Paresthesie | Soms |
Hartaandoeningen | |
Ischemische hartziekte | Vaak |
Hartkloppingen | Vaak |
Atriale fibrillatie | Soms |
Tachycardie | Soms |
Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen | |
Hoest | Vaak |
Orofaryngeale pijn waaronder irritatie van de keel | Vaak |
Rhinorroe | Vaak |
Paradoxale bronchospasmen | Soms |
Huid- en onderhuidaandoeningen | |
Jeuk/uitslag | Vaak |
Skeletspierstelsel- en bindweefselaandoeningen | |
Spierspasme | Vaak |
Skeletspierstelselpijn | Vaak |
Myalgie | Soms |
Algemene aandoeningen en toedieningsplaatsstoornissen | |
Borstpijn | Vaak |
Perifeer oedeem | Vaak |
1 Gevallen van overgevoeligheid werden uit postmarketingervaring gerapporteerd samen met het gebruik van Onbrez Breezhaler. Deze werden vrijwillig gemeld uit een populatie van onbekende grootte en het is daarom niet altijd mogelijk hun frequentie betrouwbaar te schatten of een causaal verband met geneesmiddelgebruik vast te stellen. De frequentie werd daarom berekend uit ervaring in klinische onderzoeken. | |
Bij 600 microgram eenmaal daags was het veiligheidsprofiel van Onbrez Breezhaler in het algemeen vergelijkbaar met dat van de aanbevolen doses. Een bijkomende bijwerking was tremor (vaak).
Beschrijving van geselecteerde bijwerkingen
In Fase III klinische studies namen gezondheidszorgprofessionals tijdens klinische visites waar dat gemiddeld 17 tot 20% van de patiënten een sporadisch optredende hoest hadden die meestal binnen 15 seconden na inhalatie optrad en die typisch 5 seconden duurde (ongeveer 10 seconden bij patiënten die roken). Het werd vaker waargenomen bij vrouwelijke patiënten dan bij mannelijke patiënten en vaker bij rokers dan bij ex-rokers. Deze postinhalatie hoest leidde er niet toe dat patiënten stopten met de onderzoeken bij de aanbevolen doses (hoest is een symptoom bij COPD en slechts 8,2% van de patiënten meldde hoest als ongewenst effect). Er is geen bewijs dat de postinhalatie hoest is geassocieerd met bronchospasme, exacerbaties, verslechtering van de ziekte of verlies van werkzaamheid.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Ierland
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Onbrez Breezhaler 150 microgram inhalatiepoeder in harde capsules
EU/1/09/593/001‑005
Onbrez Breezhaler 300 microgram inhalatiepoeder in harde capsules
EU/1/09/593/006-010
10. DATUM VAN HERZIENING VAN DE TEKST
18.11.2025
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 2681260 | ONBREZ BREEZHALER 300 MCG INHAL POEDER CAPS 30 | R03AC18 | € 34,29 | - | Ja | € 8,72 | € 5,19 |