SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Lysomucil 10%, oplossing
Lysomucil 20%, oplossing
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
1 ampul (3 ml) Lysomucil 10% bevat 300 mg acetylcysteïne.
1 injectieflacon (25 ml) Lysomucil 20% bevat 5 g acetylcysteïne.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie of infusie; verneveloplossing; endotracheopulmonaire instillatie, oplossing; neusdruppels, oplossing; oordruppels, oplossing.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
A. Symptomatische behandeling
Lysomucil 10%, oplossing is geïndiceerd als mucolyticum voor de behandeling van acute en chronische respiratoire aandoeningen die gepaard gaan met excessieve mucusproductie bij volwassenen, adolescenten en kinderen ouder dan 2 jaar.
B. Behandeling van paracetamolintoxicatie door parenterale toediening
Lysomucil 10%, oplossing en Lysomucil 20%, oplossing zijn geïndiceerd voor gebruik bij volwassenen, zuigelingen, kinderen jonger dan 1 jaar, kinderen en adolescenten.
4.2 Dosering en wijze van toediening
Dosering
A. Symptomatische behandeling
Behandeling met aërosol
- Eén ampul van de 10% oplossing per aërosoltoediening, 1 tot 2 maal per dag gedurende 5 tot 10 dagen.
- De dosering, evenals de frequentie van de toedieningen kunnen aanzienlijk worden verhoogd, rekening houdend met de klinische vormen en de therapeutische resultaten en dit zonder strikt onderscheid tussen doses voor kinderen en volwassenen.
- Het is raadzaam niet meer dan 10 ml aan 10% te geven per 4 uur.
Intranasale en auriculaire instillatie
2 tot 3 druppels van de 10% oplossing in elke holte, 2 tot 3 maal per dag.
Intratracheobronchiale instillatie
10 tot 20 druppels tot een volledige ampul van de 10% oplossing, 1 tot 2 maal per dag naargelang de behoefte. De toediening dient volgens de ad hoc methode te gebeuren (verblijfsondes, bronchoscopie, enz...).
B. Paracetamol-intoxicaties
Bij een inname van < 150 mg/kg is geen therapie nodig (maar wel voor kinderen < 6 jaar indien de inname > 100 mg/kg voor ≥ 2 dagen).
Er is wel therapie nodig in de volgende gevallen:
- Bij een paracetamol overdosis, ongeacht de plasmaconcentratie van paracetamol in gevallen waar de overdosis gespreid is (ingenomen over een periode van 1 uur of meer) of waar er twijfel bestaat over de tijd van inname van paracetamol (acetylcysteïne therapie moet onmiddellijk worden gestart).
- Bij een paracetamol overdosis met een plasmaconcentratie op of boven de enkele behandelingslijn die de punten van 100 mg/L op 4 uur en 15 mg/L op 15 uur verbindt op de Nomogram, onafhankelijk van de risicofactoren voor hepatotoxiciteit (behandeling met acetylcysteïne moet worden gestart binnen 0-8 uur na paracetamol inname).
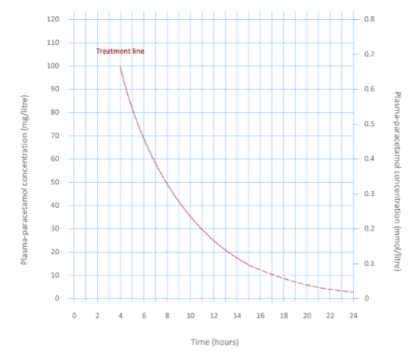
Nomogram paracetamol-intoxicatie
Voor de bestrijding van de hepatotoxische effecten van intoxicaties met paracetamol worden hoge doses gebruikt.
Twee methoden werden gevalideerd: via intraveneuze en via orale weg.
De intraveneuze toediening van acetylcysteïne biedt verscheidene voordelen:
- deze is steeds mogelijk, ook in geval van coma of braken;
- deze laat toe actieve kool per os toe te dienen, zonder risico op interferentie met het acetylcysteïne.
De specifieke farmaceutische vorm van acetylcysteïne geformuleerd aan een concentratie van 200 mg/ml (= Lysomucil 20% oplossing) is meer geschikt als antidotum dan de formulering van 100 mg/ml (=Lysomucil 10% oplossing). Maar beiden zijn geïndiceerd voor de behandeling van paracetamolintoxicaties.
De periode tussen de inname van een overdosis paracetamol en de start van de behandeling is essentieel voor het therapeutische succes van de behandeling van paracetamolintoxicaties. De behandeling moet opgestart worden binnen de 0 tot 8 uur na de inname van paracetamol. Het opstarten van de behandeling na 8 uur na inname verhoogt het risico op ernstige leverbeschadiging aanzienlijk.
De toediening van acetylcysteïne 15 uur na een overdosis met paracetamol is als behandeling veelal niet effectief, hoewel er in de literatuur bewijs bestaat over een succesvolle behandeling 16 tot 24 uur na de inname van paracetamol.
Acetylcysteïne moet toegediend worden via intraveneuze infusie, bij voorkeur door gebruik te maken van een 5% glucose oplossing als infusievloeistof. Een fysiologische zoutoplossing van 0,9% mag worden gebruikt indien de 5% glucose oplossing niet geschikt is.
De volledige behandeling met acetylcysteïne omvat 3 opeenvolgende intraveneuze infusies. De dosissen moeten achtereenvolgend worden toegediend zonder een pauze tussen de infusies. De patiënt moet een totale dosis van 300 mg/kg lichaamsgewicht toegediend krijgen over een periode van 21 uur. Een voortgezette behandeling met acetylcysteïne (toegediend met de dosis en snelheid zoals gebruikt bij de derde infusie) kan noodzakelijk zijn, afhankelijk van de klinische evaluatie van de individuele patiënt.
Lysomucil 10%, oplossing
Wanneer de formulering aan de lagere concentratie van acetylcysteïne (100 mg/mL) wordt gebruikt, wordt onderstaande behandelingsschema aangeraden.
Voor patiënten met een lichaamsgewicht ≥ 40 kg:
Ladingsdosis: 150 mg/kg in 200 ml oplossing gedurende 1 uur.
Tweede infusie: 50 mg/kg in 500 ml oplossing gedurende 4 uur.
Derde infusie: 100 mg/kg in 1000 ml oplossing gedurende 16 uur.
Voor patiënten met een lichaamsgewicht ≥ 20 kg en < 40 kg:
Ladingsdosis: 150 mg/kg in 100 ml oplossing gedurende 1 uur.
Tweede infusie: 50 mg/kg in 250 ml oplossing gedurende 4 uur.
Derde infusie: 100 mg/kg in 500 ml oplossing gedurende 16 uur.
Voor patiënten met een lichaamsgewicht <20 kg:
Ladingsdosis: 150 mg/kg in 3 ml/kg oplossing gedurende 1 uur.
Tweede infusie: 50 mg/kg in 7 ml/kg oplossing gedurende 4 uur.
Derde infusie: 100 mg/kg in 14 ml/kg oplossing gedurende 16 uur.
Lysomucil 20%, oplossing
Volwassenen
Toediening
- Weeg de patiënt om de correcte gewichtsklasse te bepalen. De dosering moet worden berekend door gebruik te maken van het huidige gewicht van de patiënt. Het gewicht moet geplafondeerd worden op 110 kg wanneer de dosering voor obese patiënten wordt berekend.
- Raadpleeg de doseringstabel voor volwassenen om het gepaste volume acetylcysteïne (ampule volume) te bepalen dat moet worden toegediend aan de infusievloeistof voor elk van de 3 infusieperiodes.
Eerste infusie
Voeg het gepaste volume van acetylcysteïne injectie toe aan 200 ml van de infusievloeistof en infuseer gedurende 1 uur.
Tweede infusie
Voeg het gepaste volume van acetylcysteïne injectie toe aan 500 ml van de infusievloeistof en infuseer gedurende de volgende 4 uur.
Derde infusie
Voeg het gepaste volume van acetylcysteïne injectie toe aan 1 liter van de infusievloeistof en infuseer gedurende de volgende 16 uur.
Doseringstabel voor volwassenen
Volwassen acetylcysteïne dosis (elke flacon = 200 mg/mL acetylcysteïne) | ||||||
Regime | Eerste infusie | Tweede infusie | Derde infusie | |||
Infusievloeistof | 200 ml 5 % glucose of | 500 ml 5 % glucose of | 1000 ml 5 % glucose of | |||
Infusieduur | 1 uur | 4 uur | 16 uur | |||
Dosis acetylcysteïne | 150 mg/kg acetylcysteïne | 50 mg/kg acetylcysteïne | 100 mg/kg acetylcysteïne | |||
Lichaamsgewicht van patiënt1 | Flacon volume2 | Infusie- | Flacon volume | Infusie- | Flacon volume | Infusie- |
kg | ml | ml/uur | ml | ml/uur | ml | ml/uur |
40-49 | 34 | 234 | 12 | 128 | 23 | 64 |
50-59 | 42 | 242 | 14 | 129 | 28 | 64 |
60-69 | 49 | 249 | 17 | 129 | 33 | 65 |
70-79 | 57 | 257 | 19 | 130 | 38 | 65 |
80-89 | 64 | 264 | 22 | 131 | 43 | 65 |
90-99 | 72 | 272 | 24 | 131 | 48 | 66 |
100-109 | 79 | 279 | 27 | 132 | 53 | 66 |
> 110 (maximale dosis) | 83 | 283 | 28 | 132 | 55 | 66 |
1 De berekeningen van de dosis gebeurde op basis van het gewicht in het midden van elke gewichtsklasse. Als de patiënt minder dan 40 kg weegt, raadpleeg dan de pediatrische doseringstabel
2 Het flacon volume werd afgerond naar het dichstbijliggende gehele getal
Kinderen
Kinderen moeten met dezelfde dosis en dosisregimes behandeld worden als volwassen. Maar de hoeveelheid intraveneus toegediende vloeistof moet worden aangepast naar leeftijd en gewicht, daar overvulling een potentieel gevaar is.
De dosissen moeten achtereenvolgend worden toegediend door gebruik te maken van een gepaste intraveneuze infusiepomp.
Voorbereiding en toediening van pediatrische infusies
- Weeg het kind om de correcte gewichtsklasse te bepalen
- Lees van de pediatrische doseringstabel af wat het totale infusievolume is dat vereist is voor elke dosering, volgens het gewicht van het kind, en maak de oplossingen volgens onderstaande aanwijzingen.
De volledige behandeling met acetylcysteïne omvat 3 opeenvolgende intraveneuze infusies.
Eerste infusie
- Bereid een 50 mg/ml oplossing door 10 ml van de ampule met acetylcysteïne (200 mg/ml) te verdunnen met 30 ml van een 5% glucose oplossing of van een 0,9% natriumchloride oplossing zodat een totaal volume van 40 ml wordt bekomen.
- Bereid het gepaste volume voor het gewicht van het kind
- De dosis wordt toegediend via infusie gedurende 1 uur aan de infusiesnelheid die in onderstaande tabel wordt weergegeven.
Tweede infusie
- Bereid een 6,25 mg/ml oplossing door 10 ml van de ampule met acetylcysteïne (200 mg/ml) te verdunnen met 310 ml van een 5% glucose oplossing of van een 0,9% natriumchloride oplossing zodat een totaal volume van 320 ml wordt bekomen.
- Bereid het gepaste volume voor het gewicht van het kind
- De dosis wordt toegediend via infusie gedurende 4 uur aan de infusiesnelheid die in onderstaande tabel wordt weergegeven.
Derde infusie
- Bereid een 6,25 mg/ml oplossing door 10 ml van de ampule met acetylcysteïne (200 mg/ml) te verdunnen met 310 ml van een 5% glucose oplossing of van een 0,9% natriumchloride oplossing zodat een totaal volume van 320 ml wordt bekomen.
- Bereid het gepaste volume voor het gewicht van het kind
- De dosis wordt toegediend via infusie gedurende 16 uur aan de infusiesnelheid die in onderstaande tabel wordt weergegeven.
Bijvoorbeeld, voor een kind dat 12 kg weegt, zou de eerste infusie 38 ml zijn geïnfuseerd aan een snelheid van 38 ml/uur gedurende 1 uur, de tweede infusie zou 100 ml zijn geïnfuseerd aan een snelheid van 25 ml/uur gedurende 4 uur en de derde infusie zou 208 ml zijn geïnfuseerd aan een snelheid van 13 ml/uur gedurende 16 uur.
Pediatrische doseringstabel
Pediatrische acetylcysteïne dosis (elke ampule = 200 mg/mL acetylcysteïne) | ||||||
Regime | Eerste infusie | Tweede infusie | Derde infusie | |||
Infusie | 50 mg/ml voor 1 uur | 6,25 mg/ml voor 4 uur | 6,25 mg/ml voor 16 uur | |||
Infusiesnelheid | 3 ml/kg/u | 2 ml/kg/u | 1 ml/kg/u | |||
Lichaamsgewicht van patiënt1 | Infusie- | Totaal infusie-volume2 | Infusie- | Totaal infusie-volume2 | Infusie- | Totaal infusie-volume2 |
kg | ml/uur | ml | ml/uur | ml | ml/uur | ml |
1 | 3 | 3 | 2 | 8 | 1 | 16 |
2 | 6 | 6 | 4 | 16 | 2 | 32 |
3 | 9 | 9 | 6 | 24 | 3 | 48 |
4 | 12 | 12 | 8 | 32 | 4 | 64 |
5 | 15 | 15 | 10 | 40 | 5 | 80 |
6 | 18 | 18 | 12 | 48 | 6 | 96 |
7 | 21 | 21 | 14 | 56 | 7 | 112 |
8 | 24 | 24 | 16 | 64 | 8 | 128 |
9 | 27 | 27 | 18 | 72 | 9 | 144 |
10-14 | 38 | 38 | 25 | 100 | 13 | 208 |
15-19 | 53 | 53 | 35 | 140 | 18 | 288 |
20-24 | 68 | 68 | 45 | 180 | 23 | 368 |
25-29 | 83 | 83 | 55 | 220 | 28 | 448 |
30-34 | 98 | 98 | 65 | 260 | 33 | 528 |
35-39 | 113 | 113 | 75 | 300 | 38 | 608 |
1 De berekeningen van de dosis gebeurde op basis van het gewicht in het midden van elke gewichtsklasse. Als de patiënt meer dan 40 kg weegt, raadpleeg dan de doseringstabel voor volwassenen
2 De getallen werden afgerond naar het dichstbijliggende gehele getal
Wijze van toediening
Bij het openen van de Lysomucil 10% ampul of de Lysomucil 20% injectieflacon komt een zwavelgeur vrij die evenwel geen bezwaar vormt voor de toediening van Lysomucil. Aangezien deze producten gedurende 24 uur stabiel blijven na opening, mag de ampul of de injectieflacon slechts op het ogenblik van het gebruik worden geopend.
A. Aërosoltherapie
De verstuiving van acetylcysteïne moet gebeuren met een aërosolapparaat dat een maximale hoeveelheid partikels met de gewenste grootte (3-20 micron) kan produceren. Een fles met perslucht of een compressor kunnen worden gebruikt.
Het verdunnen van de ampul of de oplossing is niet noodzakelijk, maar wel mogelijk (bv. 1 ampul van de 10% oplossing + 7 ml fysiologische zoutoplossing om een uiteindelijk volume van 10 ml te bekomen).
Voor de toediening van het product, verdient het aanbeveling een uitrusting in glas of plastic te gebruiken. Wanneer apparaten met metalen of rubberen onderdelen worden gebruikt, moeten deze na gebruik met water worden gewassen.
Kleine huishoudelijke apparaten, zoals peervormige verstuifpompjes of handverstuivers mogen niet worden gebruikt.
B. Instillatie
- Acetylcysteïne kan rechtstreeks in de neus of de oren worden aangebracht.
- Bovendien kan acetylcysteïne rechtstreeks in een bepaald segment van het ademhalingsstelsel worden toegediend door inbrengen van een verblijfsonde of een kleine katheter in de trachea. De oplossing wordt toegediend met behulp van een spuit die op de sonde of de katheter wordt vastgemaakt.
C. Parenteraal
- Met een infuus: de oplossing met acetylcysteïne verdunnen hetzij in een fysiologische zout-oplossing, hetzij in een oplossing met 5% glucose of 5% dextrose.
Voor onverenigbaarheden zie de rubriek "Interacties met andere geneesmiddelen en andere vormen van interacties".
- Intraveneuze injectie: langzaam intraveneus of in het aansluitstuk van de perfusie.
- Intramusculair: diepe injectie.
4.3 Contra-indicaties
Symptomatische behandeling
- Overgevoeligheid voor de werkzame stof of voor één van de in rubriek 6.1 vermelde hulpstoffen.
- Toediening via aërosol is gecontra-indiceerd bij patiënten met ernstige bronchospasmen.
- Kinderen jonger dan 2 jaar
Behandeling van paracetamolintoxicatie door parenterale toediening
Er zijn geen contra-indicaties voor de behandeling van paracetamolintoxicaties met acetylcysteïne.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De meest voorkomende bijwerkingen zijn gastro-intestinale effecten, overgevoeligheids/anafylactoïde reacties: urticaria, rash, pruritus en dyspneu zijn de meest voorkomende symptomen
Bij gebruik als antidotum:
Meer ernstige overgevoeligheids/anafylactoïde reacties werden gemeld waarbij de patiënt angio-oedeem, bronchospasmen, tachycardie en hypotensie ontwikkelt.
Zeer zeldzame gevallen van fataliteiten met intraveneus acetylcysteïne als antidotum voor paracetamolintoxicatie werden gemeld.
Tabel met bijwerkingen
Het percentage van de gevallen waarbij een bepaald ongewenst effect mogelijk is, is hierna weergegeven: zeer vaak (≥ 1/10); vaak (≥ 1/100, < 1/10); soms (≥ 1/1000, < 1/100); zelden (≥ 1/10000, < 1/1000); zeer zelden (< 1/10000) en niet bekend (kan niet geschat worden op basis van beschikbare gegevens).
Systeem orgaan- klassen | Bijwerkingen | ||||
Vaak | Soms | Zelden | Zeer zelden | Niet bekend | |
Immuun-systeemaan- |
|
|
| Overgevoeligheid* | Anafylactische shock, |
Zenuwstelsel-aandoeningen |
|
|
| Duizeligheid |
|
Hart- |
|
|
| Tachycardie |
|
Ademhaling-stelsel-, borstkas- en mediastinum-aandoeningen |
| Rhinorree | Broncho-spasmen |
| Dyspneu |
Maagdarm- | Nausea | Stomatitis | Braken | Diarree |
|
Huid- en onderhuid -aandoeningen |
| Urticaria | Rash |
| Angio-oedeem |
Algemene aandoeningen en toedienings-plaatsstoor-nissen |
|
|
|
| Gezichts-oedeem |
Onderzoeken |
|
|
|
| Verlengde protrombine- tijd |
*Overgevoeligheidsreacties werden hoofdzakelijk na IV gebruik van hoge doses acetylcysteïne als antidoot bij paracetamolintoxicatie beschreven (dit zijn waarschijnlijk pseudo-allergische reacties met als verondersteld mechanisme de vrijgave van histamine). Mogelijke allergische reacties: jeuk, netelroos, rash met roodheid van de huid (erythemateuze rash) en zwelling van het gezicht.
Beschrijving van geselecteerde bijwerkingen
In zeer zeldzame gevallen werd het optreden van ernstige huidreacties zoals het Stevens-Johnson syndroom en Lyell’s syndroom gerapporteerd, tijdsgerelateerd met de toediening van acetylcysteïne.
In de meeste gevallen kon er minstens één medeverdacht geneesmiddel geïdentificeerd worden. Het wordt daarom aanbevolen om, als er nieuwe veranderingen van de huid of de mucus membranen optreden, onmiddellijk medische hulp te zoeken en de behandeling met acetylcysteïne onmiddellijk stop te zetten.
Een daling van de bloedplaatjesaggregatie in aanwezigheid van acetylcysteïne werd in verschillende studies bevestigd. De klinische betekenis werd nog niet bepaald.
Melding van mogelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie
Website: www.eenbijwerkingmelden.be
E-Mail: adr@fagg-afmps.be
7. HOUDER VAN VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Zambon N.V.
Burgemeester E. Demunterlaan 3
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 0055376 | LYSOMUCIL 10% AMP 20 X 300 MG/3 ML | R05CB01 | € 13,62 | - | Ja | € 2 | € 1 |