1. NAAM VAN HET GENEESMIDDEL
Sandostatine Long Acting Repeatable 10 mg, poeder en oplosmiddel voor suspensie voor injectie
Sandostatine Long Acting Repeatable 20 mg, poeder en oplosmiddel voor suspensie voor injectie
Sandostatine Long Acting Repeatable 30 mg, poeder en oplosmiddel voor suspensie voor injectie
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Eén flacon Sandostatine Long Acting Repeatable, poeder voor suspensie voor injectie, bevat octreotide acetaat, overeenkomend met 10 / 20 / 30 mg octreotide.
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Poeder en oplosmiddel voor suspensie voor injectie
Poeder: wit tot witgelig getint poeder
Oplossing voor suspensie voor injectie: heldere, kleurloze tot lichtgele of lichtbruine oplossing
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Behandeling van patiënten met acromegalie, bij wie chirurgie niet geëigend of onvoldoende effectief is, of in de tussentijdse periode totdat radiotherapie volledig werkzaam is (zie rubriek 4.2).
Behandeling van patiënten met symptomen die geassocieerd zijn met functionele gastro-enteropancreatische (GEP) endocriene tumoren, bijv. carcinoïde tumoren met kenmerken van het carcinoïdsyndroom (zie rubriek 5.1).
Behandeling van patiënten met gevorderde neuro-endocriene tumoren van de middendarm of van onbekende primaire tumorlocatie waarbij herkomst van niet-middendarm locaties is uitgesloten.
Behandeling van TSH-producerende hypofyseadenomen:
- als secretie niet is genormaliseerd na chirurgie en/of radiotherapie;
- bij patiënten bij wie chirurgie niet geëigend is;
- bij bestraalde patiënten, totdat radiotherapie effectief is.
4.2 Dosering en wijze van toediening
Dosering
Acromegalie
Het wordt aanbevolen om de behandeling te starten met de toediening van 20 mg Sandostatine Long Acting Repeatable, met een interval van 4 weken gedurende 3 maanden. Patiënten die al worden behandeld met s.c. Sandostatine kunnen de behandeling met Sandostatine Long Acting Repeatable beginnen op de dag na de laatste dosis van s.c. Sandostatine. Latere aanpassing van de dosering dient te worden gebaseerd op de serumconcentraties groeihormoon (GH) en insulin-like growth factor 1/somatomedine C (IGF-1), en klinische symptomen.
Voor patiënten bij wie, binnen deze periode van 3 maanden, klinische symptomen en biochemische parameters (GH, IGF-1) niet volledig onder controle zijn (GH-concentraties nog boven 2,5 microgram/l), kan de dosis worden verhoogd tot 30 mg per 4 weken. Indien na 3 maanden GH, IGF-1 en/of symptomen niet voldoende onder controle zijn bij een dosis van 30 mg, kan de dosis worden verhoogd tot 40 mg per 4 weken.
Bij patiënten met GH-concentraties die constant onder 1 microgram/l blijven, bij wie IGF-1-serumconcentraties genormaliseerd zijn en bij wie de meeste reversibele verschijnselen/klachten van acromegalie zijn verdwenen na 3 maanden behandeling met 20 mg, kan 10 mg Sandostatine Long Acting Repeatable worden toegediend iedere 4 weken. Het is echter vooral in deze groep patiënten bij deze lage dosis van Sandostatine Long Acting Repeatable raadzaam om adequate controle van serum-GH- en serum-IGF-1-concentraties en klinische verschijnselen/klachten nauwlettend te controleren.
Bij patiënten op een stabiele dosis van Sandostatine Long Acting Repeatable dient elke 6 maanden het GH en de IGF-1 te worden bepaald.
Gastro-enteropancreatische endocriene tumoren
Behandeling van patiënten met symptomen die geassocieerd zijn met functionele gastro-enteropancreatische neuro-endocriene tumoren.
Het wordt aanbevolen om de behandeling te starten met de toediening van 20 mg Sandostatine Long Acting Repeatable met een interval van 4 weken. Patiënten die al worden behandeld met s.c. Sandostatine dienen behandeld te blijven met de voorgaande effectieve dosis gedurende 2 weken na de eerste injectie met Sandostatine Long Acting Repeatable.
Bij patiënten bij wie de symptomen en biologische markers goed onder controle zijn na 3 maanden behandeling, mag de dosis worden gereduceerd tot 10 mg Sandostatine Long Acting Repeatable iedere 4 weken.
Bij patiënten bij wie de klachten slechts gedeeltelijk onder controle zijn na 3 maanden behandeling, mag de dosis worden verhoogd tot 30 mg Sandostatine Long Acting Repeatable iedere 4 weken.
Op dagen waarop de symptomen die geassocieerd zijn met gastro-enteropancreatische tumoren kunnen toenemen tijdens de behandeling met Sandostatine Long Acting Repeatable, wordt additionele toediening van s.c. Sandostatine aanbevolen met de dosis die gebruikt werd voor de start van de behandeling met Sandostatine Long Acting Repeatable. Dit kan voornamelijk optreden in de eerste 2 maanden van de behandeling totdat therapeutische concentraties van octreotide worden bereikt.
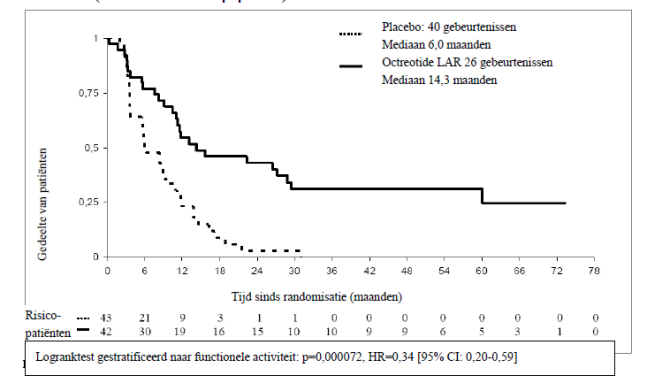
Behandeling van patiënten met gevorderde neuro-endocriene tumoren van de middendarm of van onbekende primaire tumorlocatie waarbij herkomst van niet-middendarm locaties is uitgesloten
De aanbevolen dosis Sandostatine Long Acting Repeatable is 30 mg toegediend iedere 4 weken (zie rubriek 5.1). Behandeling met Sandostatine Long Acting Repeatable voor tumorcontrole dient te worden voortgezet in afwezigheid van tumorprogressie.
Behandeling van TSH-producerende adenomen
Behandeling met Sandostatine Long Acting Repeatable dient te worden gestart met een dosis van 20 mg met een interval van 4 weken gedurende 3 maanden voordat men dosisaanpassing overweegt. De dosis wordt dan aangepast op basis van de TSH- en schildklierhormoonrespons.
Gebruik bij patiënten met een nierfunctiestoornis
Nierfunctiestoornis had geen invloed op de totale blootstelling (AUC) van octreotide bij s.c. toediening van Sandostatine. Daarom is er geen dosisaanpassing van Sandostatine Long Acting Repeatable nodig.
Gebruik bij patiënten met een leverfunctiestoornis
In een onderzoek met s.c. en i.v. toediening van Sandostatine werd aangetoond dat de eliminatiecapaciteit bij patiënten met levercirrose verminderd kan zijn, dit bleek niet bij patiënten met leververvetting. In bepaalde gevallen kan dosisaanpassing nodig zijn bij patiënten met een leverfunctiestoornis.
Gebruik bij ouderen
In een onderzoek met s.c. toediening van Sandostatine was er geen dosisaanpassing noodzakelijk bij proefpersonen met een leeftijd van ≥65 jaar. Daarom is er geen dosisaanpassing van Sandostatine Long Acting Repeatable nodig bij deze groep patiënten.
Gebruik bij kinderen
Er is beperkte ervaring met het gebruik van Sandostatine Long Acting Repeatable bij kinderen.
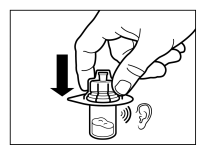
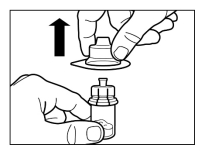
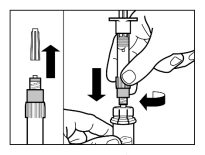
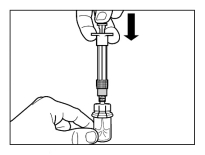
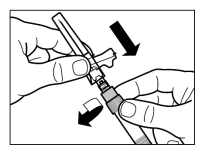
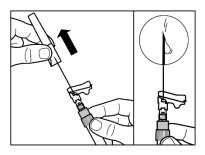
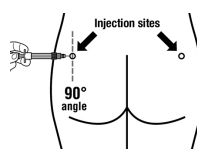
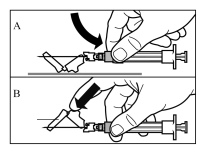
Wijze van toediening
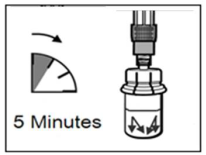
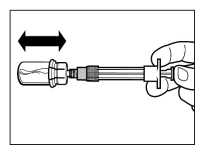
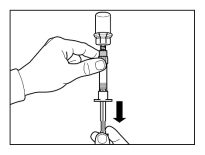
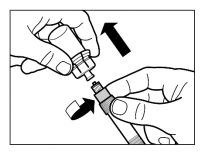
Sandostatine Long Acting Repeatable dient alleen via diepe intramusculaire injectie te worden toegediend. De locatie van herhaalde diepe intramusculaire injecties dient te worden afgewisseld tussen de linker en rechter gluteale spier (zie rubriek 6.6).
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor (een van) de in rubriek 6.1 vermelde hulpstof(fen).
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
De meest voorkomende gemelde bijwerkingen tijdens de behandeling met octreotide omvatten gastro-intestinale aandoeningen, aandoeningen van het zenuwstelsel, lever- en galaandoeningen en voedings- en stofwisselingsstoornissen.
De meest gemelde bijwerkingen in klinische onderzoeken met toediening van octreotide waren diarree, buikpijn, misselijkheid, flatulentie, hoofdpijn, cholelithiase, hyperglykemie en constipatie. Andere vaak gemelde bijwerkingen waren duizeligheid, gelokaliseerde pijn, galgruis, schildklierafwijkingen (bijv. verlaagd schildklierstimulerend hormoon [TSH], verlaagd totaal T4, en verlaagd vrij T4), dunne ontlasting, verminderde glucosetolerantie, braken, asthenie en hypoglykemie.
Tabel met een overzicht van de bijwerkingen
De volgende bijwerkingen, weergegeven in Tabel 1, zijn verzameld uit klinische onderzoeken met octreotide:
Bijwerkingen (Tabel 1) zijn gerangschikt naar frequentie, de meest frequente eerst, met gebruikmaking van de volgende afspraak: zeer vaak (≥1/10); vaak (≥1/100, <1/10); soms (≥1/1.000, <1/100); zelden (≥1/10.000, <1/1.000) zeer zelden (<1/10.000), inclusief geïsoleerde meldingen. Binnen iedere frequentiegroep worden bijwerkingen gerangschikt naar afnemende ernst.
Tabel 1 Bijwerkingen gemeld in klinisch onderzoek
Maagdarmstelselaandoeningen | |
Zeer vaak: | Diarree, buikpijn, misselijkheid, constipatie, flatulentie |
Zenuwstelselaandoeningen | |
Zeer vaak: | Hoofdpijn |
Endocriene aandoeningen | |
Vaak: | Hypothyreoïdie, schildklieraandoening (bijv. verlaagd TSH, verlaagd totaal T4 en verlaagd vrij T4) |
Lever- en galaandoeningen | |
Zeer vaak: | Cholelithiase |
Metabole en nutritionele aandoeningen | |
Zeer vaak: | Hyperglykemie |
Algemene aandoeningen en toedieningsplaatsstoornissen | |
Zeer vaak: | Injectieplaatsreacties |
Vaak: | Asthenie |
Onderzoeken | |
Vaak | Transaminasespiegels verhoogd |
Huid- en onderhuidaandoeningen | |
Vaak: | Pruritus, rash, alopecia |
Ademhalingsstelsel-, borstkas en mediastinumaandoeningen | |
Vaak: | Dyspneu |
Hartaandoeningen | |
Vaak: | Bradycardie |
Postmarketing
Spontaan gemelde bijwerkingen, weergegeven in Tabel 2, zijn gemeld op vrijwillige basis en het is niet altijd mogelijk om betrouwbaar een frequentie of een causaal verband met de blootstelling aan het geneesmiddel vast te stellen.
Tabel 2 Bijwerkingen afgeleid van spontane meldingen
Bloed- en lymfestelselaandoeningen |
Immuunsysteemaandoeningen |
Huid- en onderhuidaandoeningen |
Lever- en galaandoeningen |
Hartaandoeningen |
Onderzoeken |
Beschrijving van geselecteerde bijwerkingen
Galblaas en gerelateerde reacties
Het is bewezen dat somatostatine-analogen de contractiliteit van de galblaas doen afnemen en de hoeveelheid gal die wordt afgescheiden verminderen, wat kan leiden tot afwijkingen aan de galblaas en tot bezinksel. Ontwikkeling van galstenen is gemeld bij 15 tot 30% van langdurige gebruikers van s.c. Sandostatine. De incidentie in de gehele populatie (40 tot 60 jaar oud) is ongeveer 5 tot 20%. Langdurige blootstelling aan Sandostatine Long Acting Repeatable van patiënten met acromegalie of gastro-enteropancreatische tumoren suggereert dat behandeling met Sandostatine Long Acting Repeatable de incidentie van galstenen niet verhoogt, in vergelijking met s.c. behandeling. Als galstenen zich toch voordoen, zijn ze meestal asymptomatisch. Symptomatische galstenen moeten worden behandeld, hetzij door een oplossende therapie met galzuren of door een chirurgische ingreep.
Maagdarmstelselaandoeningen
In zeldzame gevallen kunnen gastro-intestinale bijwerkingen lijken op acute intestinale obstructie, met progressieve opgezette buik, ernstige epigastrische pijn, abdominale gevoeligheid en buikspasmen.
Het is bekend dat de frequentie van gastro-intestinale bijwerkingen met de tijd afneemt bij voortzetting van de behandeling.
Overgevoeligheid en anafylactische reacties
Overgevoeligheid en allergische reacties zijn gemeld tijdens de post-marketingfase. Als deze zich voordoen, hebben ze met name impact op de huid; zelden op de mond of de luchtwegen. Er zijn ook geïsoleerde gevallen van anafylactische shock gemeld.
Injectieplaatsreacties
Reacties gerelateerd aan de injectieplaats zoals pijn, roodheid, bloeding, jeuk, zwelling of verharding werden vaak gemeld bij patiënten die Sandostatine Long Acting Repeatable kregen, maar deze gebeurtenissen vereisten in het merendeel van de gevallen geen klinische interventie.
Voedings- en stofwisselingsstoornissen
Hoewel de gemeten fecale excretie van vet kan toenemen, is er tot nu toe geen bewijs dat langdurige behandeling met octreotide heeft geleid tot voedingstekorten als gevolg van malabsorptie.
Pancreasenzymen
In zeer zeldzame gevallen is acute pancreatitis gemeld binnen de eerste uren of dagen na behandeling met Sandostatine s.c., die verdween na stopzetting van het geneesmiddel. Daarnaast is cholelithiasegeïnduceerde pancreatitis gemeld bij patiënten die langdurig met Sandostatine s.c. werden behandeld.
Hartaandoeningen
Bradycardie is een vaak voorkomende bijwerking van somatostatine-analogen. In zowel acromegalie- als carcinoïdsyndroompatiënten werden veranderingen in het ecg waargenomen, zoals verlenging van het QT-interval, asverschuivingen, vroegtijdige repolarisatie, lage spanning, R/S-transitie, voortijdige progressie van de R-golf en niet-specifieke ST-T-golfveranderingen. De relatie van deze gebeurtenissen met octreotideacetaat is niet vastgesteld, omdat veel van deze patiënten onderliggende hartaandoeningen hebben (zie rubriek 4.4).
Trombocytopenie
Trombocytopenie is gemeld tijdens de post-marketingfase, met name tijdens de behandeling met Sandostatine (i.v.) bij patiënten met levercirrose en tijdens de behandeling met Sandostatine Long Acting Repeatable. Dit is omkeerbaar na stopzetting van de behandeling.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
E-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Novartis Pharma NV
Medialaan 40
B-1800 Vilvoorde
8. NUMMERS VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Sandostatine Long Acting Repeatable 10 mg: BE191746 / LU: 1998020008
- 0755136: 1*1 flacon poudre + 1*1 seringue prer. solvant
Sandostatine Long Acting Repeatable 20 mg: BE191737 / LU: 1998020007
- 0755153: 1*1 flacon poudre + 1*1 seringue prer. solvant
Sandostatine Long Acting Repeatable 30 mg: BE191685 / LU: 1998020011
- 0755167: 1*1 flacon poudre + 1*1 seringue prer. solvant
10. DATUM VAN HERZIENING VAN DE TEKST
10/2023
Goedkeuringsdatum: 11/2025
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 1395052 | SANDOSTATINE LAR 1FL 30MG | H01CB02 | € 754,27 | - | Ja | € 12,8 | € 8,5 |
| 1395060 | SANDOSTATINE LAR 1FL 20MG | H01CB02 | € 561,56 | - | Ja | € 12,8 | € 8,5 |