SAMENVATTING VAN DE PRODUCT KENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Humalog 100 eenheden/ml oplossing voor injectie in injectieflacon
Humalog 100 eenheden/ml oplossing voor injectie in patroon
Humalog 100 eenheden/ml KwikPen oplossing voor injectie in een voorgevulde pen
Humalog 100 eenheden/ml Junior KwikPen oplossing voor injectie in een voorgevulde pen
Humalog 100 eenheden/ml Tempo Pen oplossing voor injectie in een voorgevulde pen
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Iedere ml bevat 100 eenheden insuline lispro* (overeenkomend met 3,5 mg)
Injectieflacon
Iedere injectieflacon bevat 1000 eenheden insuline lispro in 10 ml oplossing.
Patroon
Iedere patroon bevat 300 eenheden insuline lispro in 3 ml oplossing.
KwikPen en Tempo Pen
Iedere voorgevulde pen bevat 300 eenheden insuline lispro in 3 ml oplossing.
Iedere voorgevulde pen geeft 1-60 eenheden af in stappen van 1 eenheid.
Junior KwikPen
Iedere voorgevulde pen bevat 300 eenheden insuline lispro in 3 ml oplossing.
Iedere Junior KwikPen geeft 0,5 – 30 eenheden af in stappen van 0,5 eenheid.
*geproduceerd in E. coli met behulp van recombinant-DNA-technologie.
Voor de volledige lijst van hulpstoffen zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Oplossing voor injectie.
Heldere, kleurloze, waterige oplossing.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Voor de behandeling van volwassenen en kinderen met diabetes mellitus die insuline nodig hebben voor handhaving van normale glucosehomeostase. Humalog is ook geïndiceerd voor de initiële stabilisatie van diabetes mellitus.
4.2 Dosering en wijze van toediening
Dosering
De dosering dient door de arts te worden bepaald, volgens de behoefte van de patiënt.
Junior KwikPen
Humalog 100 eenheden/ml Junior KwikPen is geschikt voor patiënten die profijt kunnen hebben van fijnere aanpassingen van de dosis insuline.
Humalog kan kort voor de maaltijd toegediend worden en indien nodig kort na de maaltijd.
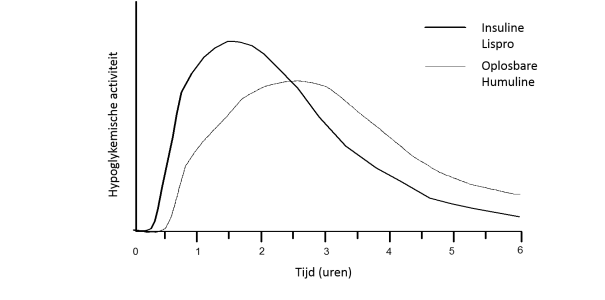
Subcutaan toegediende Humalog heeft een snel effect en heeft een kortere werkingsduur (2 tot 5 uur) in vergelijking met oplosbare insuline. Deze vlotte intrede van werking maakt het mogelijk om een Humalog injectie (of in het geval van toediening via continue subcutane infusie, een Humalog bolus) zeer kort voor een maaltijd te geven. Het tijdsverloop van de werkzaamheid van iedere insuline kan zeer variëren tussen verschillende personen of op verschillende tijdstippen in dezelfde persoon. Onafhankelijk van de injectieplaats blijft de snellere aanvang van werking behouden vergeleken met oplosbare insuline. Zoals met alle insulinepreparaten is de werkingsduur van Humalog afhankelijk van de dosis, injectieplaats, bloeddoorstroming, temperatuur en fysieke inspanning.
Humalog mag op advies van de arts worden gebruikt in combinatie met een langerwerkend insuline of orale sulfonylureumderivaten.
Speciale patiëntengroepen
Nierfunctiestoornis
De insulinebehoefte kan verminderd zijn in aanwezigheid van nierfunctiestoornissen.
Leverfunctiestoornis
De insulinebehoefte kan verminderd zijn bij patiënten met een leverfunctiestoornis vanwege een verminderde capaciteit voor de gluconeogenese en een verminderde insulineafbraak. Bij patiënten met een chronische leverfunctiestoornis kan een verhoging van de insulineresistentie echter leiden tot een verhoogde insulinebehoefte.
Pediatrische patiënten
Humalog kan gebruikt worden bij adolescenten en kinderen (zie rubriek 5.1)
Wijze van toediening
Subcutaan gebruik
De Humalog preparaten dienen te worden toegediend via subcutane injectie.
De KwikPen, Junior KwikPen en Tempo Pen zijn alleen geschikt voor subcutane injectie. Humalog in patronen is alleen geschikt voor subcutane injectie via een voor hergebruik geschikte pen van Lilly of via compatibele pompsystemen voor continue subcutane insuline infusie (CSII).
Subcutane toediening dient plaats te vinden in de bovenarm, de dijen, de billen of de buik. De injectieplaats dient te worden afgewisseld, zodat dezelfde injectieplaats niet vaker wordt gebruikt dan ongeveer eens per maand. De injectieplaatsen dienen altijd te worden afgewisseld binnen eenzelfde gebied om het risico op lipodystrofie en cutane amyloïdose te beperken (zie rubriek 4.4. en 4.8).
Er dient zorgvuldigheid te worden betracht wanneer Humalog subcutaan wordt toegediend, om er zeker van te zijn dat er niet in een bloedvat wordt geïnjecteerd. Na de injectie dient de injectieplaats niet gemasseerd te worden. Patiënten moeten worden geïnstrueerd om de juiste injectietechniek toe te passen.
Humalog KwikPennen
Humalog KwikPen is beschikbaar in twee sterktes. De Humalog 100 eenheden/ml KwikPen (en Humalog 200 eenheden/ml KwikPen, zie de afzonderlijke SmPC) geeft 1-60 eenheden af in stappen van 1 eenheid per enkelvoudige injectie. De Humalog 100 eenheden/ml Junior KwikPen geeft 0,5-30 eenheden af per enkelvoudige injectie in stappen van 0,5 eenheid. Het aantal eenheden insuline wordt getoond in het doseervenster van de pen, onafhankelijk van de sterkte en er dient geen dosisomzetting plaats te vinden bij het overzetten van een patiënt op een nieuwe sterkte of op een pen met een andere dosisstap.
Humalog Tempo Pen
De Humalog 100 eenheden/ml Tempo Pen geeft 1-60 eenheden af in stappen van 1 eenheid per enkelvoudige injectie. Het aantal eenheden insuline wordt getoond in het doseervenster van de pen ongeacht de sterkte en er dient geen dosisomzetting plaats te vinden bij het overzetten van een patiënt op een nieuwe sterkte of op een pen met een andere dosisstap. De Tempo Pen kan worden gebruikt met de Tempo Smart Button, een optionele module voor gegevensoverdracht (zie rubriek 6.6).
Patiënten moeten, als zij de Tempo Pen, de Tempo Smart Button en de mobiele applicatie gebruiken worden geïnstrueerd om, als zij onzeker zijn hoeveel zij hebben geïnjecteerd, hun bloedsuikerspiegels te controleren als zij nog een injectie overwegen of hiertoe een besluit nemen, net zoals bij elke insuline-injectie.
Het gebruik van Humalog in een insuline-infusiepomp
Voor subcutane injectie van Humalog waarbij gebruik wordt gemaakt van een infusiepomp voor continue toediening, kunt u het reservoir van de pomp vullen met behulp van een injectieflacon van 100 eenheden/ml. Sommige pompen zijn compatibel met patronen die in hun geheel in de pomp kunnen worden geplaatst.
Slechts bepaalde CE gewaarmerkte insuline-infusiepompen kunnen gebruikt worden voor de infusie van insuline lispro. Voordat de infusie van insuline lispro wordt gestart, moeten de aanwijzingen van de fabrikant van de pomp worden bestudeerd om zich te verzekeren van de geschiktheid van de betreffende pomp. Gebruik het juiste reservoir en katheter voor de pomp. Bij het vullen van het pompreservoir dient beschadiging hiervan te worden voorkomen door gebruik van de juiste naaldlengte op het vulsysteem. De infusieset (slang en canule) moet worden vervangen conform de instructies die zijn vermeld in de productinformatie die bij de infusieset wordt geleverd. In geval van een hypoglykemie, dient de infusie te worden stopgezet totdat deze voorbij is. Indien herhaaldelijk of ernstige lage bloedglucose waarden optreden, overweeg dan de noodzaak een insuline infusie te verminderen of te stoppen. Een pompdefect of verstopping van de infusieset kan leiden tot een snelle toename van glucosespiegels. Wanneer een onderbreking van de insulinedoorstroming wordt vermoed, volg de aanwijzingen in de productinformatie van de pomp. Humalog mag niet met andere insuline gemengd worden indien het gebruikt wordt in een insuline-infusiepomp.
Intraveneuze toediening van insuline
Indien noodzakelijk kan Humalog ook intraveneus worden toegediend, bijvoorbeeld voor de controle van bloedglucosespiegels tijdens een ketoacidose, acute ziektes of tijdens intra- en post-operatieve periodes.
Humalog 100 eenheden/ml is beschikbaar in injectieflacons als toediening via een intraveneuze injectie noodzakelijk is.
Intraveneuze injectie van insuline lispro moet worden uitgevoerd volgens de normale klinische praktijk voor intraveneuze injecties, bijvoorbeeld door middel van een intraveneuze bolusinjectie of met een infusiesysteem. Het frequent controleren van de bloedglucosespiegels is noodzakelijk.
Infusiesystemen met concentraties van insuline lispro tussen 0,1 eenheid/ml en 1,0 eenheid/ml in 0,9 % natriumchloride of 5 % dextrose zijn gedurende 48 uur stabiel bij kamertemperatuur. Het wordt aanbevolen het systeem helemaal klaar te maken voor gebruik voordat met de infusie naar de patiënt begonnen wordt.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstof(fen).
Hypoglykemie.
4.8 Bijwerkingen
Samenvatting van het veiligheidsprofiel
Hypoglykemie is de meest frequent optredende bijwerking van insulinetherapie waar een diabeet last van kan hebben. Ernstige hypoglykemie kan leiden tot bewusteloosheid, en in extreme gevallen tot overlijden. Geen specifieke frequentie voor hypoglykemie is gerapporteerd aangezien hypoglykemie een resultaat is van zowel insulinedosering als andere factoren zoals bijvoorbeeld mate van dieet en lichaamsbeweging van de patiënt.
Tabel met bijwerkingen
De volgende verwante bijwerkingen uit klinische studies zijn hieronder ingedeeld naar de MedDRA-voorkeursterminologie voor systeem/orgaanklassen en in volgorde van afnemende incidentie (zeer vaak: ≥ 1/10; vaak: ≥ 1/100, < 1/10; soms: ≥ 1/1.000, < 1/100; zelden: ≥ 1/10.000, < 1/1000; zeer zelden: < 1/10.000); niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Binnen iedere frequentiegroep worden bijwerkingen gerangschikt naar afnemende ernst.
MedDRA systeem orgaanklasse | Zeer vaak | Vaak | Soms | Zelden | Zeer zelden | Niet bekend |
Immuunsysteemaandoeningen |
| |||||
Locale allergie |
| X |
|
|
|
|
Systemische allergie |
|
|
| X |
|
|
Huid- en onderhuidaandoeningen |
| |||||
Lipodystrofie |
|
| X |
|
|
|
Cutane amyloïdose |
|
|
|
|
| X |
Beschrijving van geselecteerde bijwerkingen
Lokale allergie
Vaak treden lokale overgevoeligheidsreacties op. Roodheid, zwelling en jeuk kunnen voorkomen op de injectieplaats. Deze reactie gaat meestal in een paar dagen tot paar weken over. In sommige gevallen kan deze reactie gerelateerd worden aan andere factoren dan de insuline, zoals irriterende stoffen in het huidreinigingsmiddel, of een slechte injectietechniek.
Systemische allergie
Systemische allergie, dat zelden optreedt maar potentieel meer ernstig, is een gegeneraliseerde allergie voor insuline. Het kan rash over het gehele lichaam, kortademigheid, piepende ademhaling, bloeddrukdaling, snelle pols, of transpiratie veroorzaken. Ernstige gevallen van gegeneraliseerde allergie kunnen levensbedreigend zijn.
Huid- en onderhuidaandoeningen
Lipodystrofie en cutane amyloïdose kunnen optreden op de injectieplaats en kunnen de plaatselijke insuline-absorptie vertragen. Het continue afwisselen van de injectieplaats binnen eenzelfde gebied kan helpen deze reacties te verminderen of te voorkomen (zie rubriek 4.4).
Oedeem
Er zijn met insulinetherapie gevallen van oedeem gemeld, in het bijzonder als voorafgaande slechte metabole controle verbeterd is door intensieve insulinetherapie.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via: het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten, www.fagg.be, Afdeling Vigilantie: Website: www.eenbijwerkingmelden.be, e-mail: adr@fagg-afmps.be.
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Eli Lilly Nederland B.V., Papendorpseweg 83, 3528 BJ Utrecht, Nederland
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
EU/1/96/007/002
EU/1/96/007/004
EU/1/96/007/020
EU/1/96/007/021
EU/1/96/007/023
EU/1/96/007/031
EU/1/96/007/032
EU/1/96/007/043
EU/1/96/007/044
EU/1/96/007/045
EU/1/96/007/046
EU/1/96/007/047
10. DATUM VAN HERZIENING VAN DE TEKST
03 september 2020.
AFLEVERINGSWIJZE Aan medisch voorschrift onderworpen geneesmiddel.
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu.
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 1281534 | HUMALOG VIAL 100U/ML 10 ML | A10AB04 | € 24,41 | - | Ja | € 2 | € 1 |