SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET GENEESMIDDEL
Harmonet 0,075 mg/0,020 mg omhulde tabletten
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Elke tablet bevat 0,075 mg gestodeen en 0,020 mg ethinylestradiol.
Hulpstoffen met bekend effect : lactose en sacharose (elke tablet bevat 37,505 mg lactosemonohydraat en 19,66 mg sacharose, zie rubriek 4.4).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Omhulde tabletten
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Orale hormonale contraceptie
Bij de beslissing om Harmonet voor te schrijven moet rekening worden gehouden met de huidige risicofactoren van de individuele vrouw, in het bijzonder met de risicofactoren voor veneuze trombo-embolie (VTE) en hoe het risico op VTE met Harmonet zich verhoudt tot het risico met andere gecombineerde hormonale anticonceptiva (zie rubrieken 4.3 en 4.4).
4.2 Dosering en wijze van toediening
Start niet met Harmonet of blijf Harmonet niet gebruiken bij zwangerschap of bij een vermoeden van zwangerschap.
Dosering
Hoe Harmonet innemen
De tabletten moeten worden ingenomen in de op de blister aangegeven volgorde, dagelijks om ongeveer hetzelfde uur, gedurende 21 opeenvolgende dagen, met een pilvrije periode van 7 dagen tussen elke blister. Doorgaans begint een dervingsbloeding 2 tot 3 dagen na de inname van de laatste tablet. Deze kan aanhouden na aan de volgende blister te zijn begonnen.
Hoe starten met Harmonet
Geen hormonale contraceptie gedurende de vorige maand
De gebruikster moet Harmonet beginnen in te nemen op de eerste dag van de menstruatiecyclus (d.w.z. de eerste dag van de regels).
Beginnen met Harmonet tussen de 2de en de 7de dag van de menstruatiecyclus is toegestaan; het gebruik van een bijkomende, niet-hormonale, mechanische contraceptiemethode (condoom, spermadodend middel…) is aanbevolen gedurende de eerste 7 dagen van de inname van Harmonet.
In opvolging van een ander oraal hormonaal combinatiecontraceptivum (HCC)
Het gebruik van Harmonet moet beginnen op de dag die volgt op de inname van de laatste actieve tablet van het vorige oraal HCC maar, ten laatste, de dag na de gebruikelijke pilvrije periode of de laatste inactieve tablet van het vorige oraal HCC.
In opvolging van een progestatief contraceptivum (pil, prikpil, spiraaltje, implantaat)
De gebruikster kan op eender welke dag met de inname van een progestatieve pil (minipil) stoppen; het gebruik van Harmonet moet de volgende dag aanvatten. Het gebruik van Harmonet moet aanvatten op de dag van de verwijdering van het implantaat of het spiraaltje. Het gebruik van Harmonet gebeurt op de voorziene dag voor de volgende prikpil.
In ieder geval wordt de gebruikster aanbevolen een bijkomende, niet-hormonale, mechanische contraceptiemethode te gebruiken (condoom, spermadodend middel…) gedurende de eerste 7 dagen van de inname van Harmonet.
Na een zwangerschapsonderbreking tijdens het eerste trimester
De gebruikster mag onmiddellijk starten met Harmonet. In dat geval is geen bijkomende contraceptiemethode nodig.
Postpartum
Er dient rekening te worden gehouden met het verhoogde risico op trombo-embolie tijdens de zwangerschap en vooral tijdens de 6 weken durende periode van het puerperium (zie rubriek 4.4 - Risicofactoren voor VTE).
Harmonet mag slechts opgestart worden vanaf de 28ste dag na een bevalling (voor de gebruiksters die er voor kiezen om geen borstvoeding te geven) of na een zwangerschapsonderbreking tijdens het tweede trimester. Het is aanbevolen een bijkomende, niet-hormonale, mechanische contraceptiemethode te gebruiken (condoom, spermadodend middel…) gedurende de eerste 7 dagen van de inname van Harmonet. Zwangerschap moet worden uitgesloten indien seksuele betrekkingen hebben plaatsgevonden vóór het instellen van Harmonet; anders moet de vrouw wachten tot haar volgende menstruatiecyclus om met Harmonet te starten.
Voor vrouwen die borstvoeding geven, zie rubriek 4.6.
Wat doen in geval tabletten vergeten werden
De contraceptieve bescherming kan verminderd zijn indien tabletten Harmonet vergeten werden. Dit is in het bijzonder het geval indien deze vergetelheid de tussentijd tussen de laatste tablet van de lopende blister en de eerste tablet van de volgende blister verlengt.
- Indien het vergeten van een tablet wordt vastgesteld binnen de 12 uren volgend op het gebruikelijke uur van inname, onmiddellijk de vergeten tablet innemen en de behandeling voortzetten met inname van de volgende tablet op het gebruikelijke uur.
- Indien het vergeten van een tablet wordt vastgesteld meer dan 12 uren na het gebruikelijke uur van inname of indien meer dan één tablet vergeten werd, is de contraceptieve bescherming niet langer verzekerd.
- Onmiddellijk de vergeten tablet innemen; dit kan resulteren in de inname van twee tabletten op dezelfde dag. De behandeling voortzetten met inname van de volgende tablet op het gebruikelijke uur en tegelijk een bijkomende, niet-hormonale, mechanische contraceptiemethode gebruiken (condoom, spermadodend middel…) gedurende de volgende 7 dagen.
- Indien deze 7 dagen durende veiligheidsperiode met voorbehoedsmiddel zich uitstrekt tot voorbij de laatste tablet van de lopende blister, moet de pilvrije periode overgeslagen worden en moet onmiddellijk met de volgende blister begonnen worden na inname van de laatste tablet van de aangebroken blister. Een pilvrije periode tussen 2 blisters is niet toegestaan. Dit voorkomt een te lange periode zonder pilinname en vermindert het risico van een ongewilde ovulatie. Vermoedelijk zal geen dervingbloeding optreden vóór het einde van de nieuwe blister. De gebruikster kan echter wel spotting of tussenbloedingen vertonen.
- Indien zich geen dervingbloeding voordoet op het einde van de nieuwe blister, moet een eventuele zwangerschap uitgesloten worden alvorens een nieuwe blister aan te vatten.
Wat doen in geval van braken en/of diarree
Indien zich braken of diarree voordoet binnen de 4 uur na inname van een tablet, kan de absorptie van de tabletten verminderd zijn. In dergelijke gevallen moeten de instructies over het vergeten van tabletten opgevolgd worden (cfr vergeten vastgesteld binnen de 12 uren) en moet de gebruikster een tablet van een reserveblister innemen. Indien de gebruikster geen reserveblister meer heeft, moet een bijkomende, niet-hormonale, mechanische contraceptiemethode gebruikt worden gedurende de rest van de cyclus. De tabletten van de begonnen blister moeten verder ingenomen worden om een voortijdige dervingbloeding te voorkomen. Andere mechanische contraceptiemethoden (zoals condoom, spermadodend middel…) moeten overwogen worden indien verwacht wordt dat de gastro-intestinale stoornissen zullen aanhouden.
Pediatrische patiënten
De doeltreffendheid en de veiligheid van orale HCC’s zijn aangetoond bij vrouwen die zwanger kunnen worden.
Deze producten mogen niet worden gebruikt vóór de eerste regels.
Geriatrische patiënten
Orale HCC’s zijn niet geïndiceerd bij postmenopauzale vrouwen.
Wijze van toediening
Oraal gebruik.
4.3 Contra-indicaties
Gecombineerde hormonale anticonceptiva mogen in de volgende situaties niet worden gebruikt. Als één van deze aandoeningen zich voor het eerst voordoet tijdens het gebruik van Harmonet, moet Harmonet onmiddellijk worden stopgezet.
- Aanwezigheid van of risico op arteriële trombo-embolie (ATE)
- Arteriële trombo-embolie – bestaande arteriële trombo-embolie, eerder doorgemaakte arteriële trombo-embolie (bijv. myocardinfarct) of prodromale aandoening (bijv. angina pectoris)
- Cerebrovasculaire ziekte – bestaande beroerte, eerder doorgemaakte beroerte of prodromale aandoening (bijv. transient ischaemic attack (TIA))
- Bekende erfelijke of verworven predispositie voor arteriële trombo-embolie, bijvoorbeeld hyperhomocysteïnemie en antifosfolipiden-antistoffen (anticardiolipine-antistoffen, lupusanticoagulans)
- Voorgeschiedenis van migraine met focale neurologische symptomen
- Een hoog risico op arteriële trombo-embolie als gevolg van meerdere risicofactoren (zie rubriek 4.4) of door de aanwezigheid van een ernstige risicofactor, zoals:
- diabetes mellitus met vasculaire symptomen (micro- of macro-angiopathie)
- ernstige hypertensie
- ernstige dislipoproteïnemie
- Coronaire ziekte;
- Aanwezigheid van of risico op veneuze trombo-embolie (VTE)
- Veneuze trombo-embolie – bestaande VTE (bij antistollingsmiddelen) of eerder doorgemaakte VTE (bijv. diepe veneuze trombose [DVT] of longembolie [PE])
- Bekende erfelijke of verworven predispositie voor veneuze trombo-embolie, bijvoorbeeld APC-resistentie, (waaronder factor V-Leiden), antitrombine‑III-deficiëntie, proteïne C-deficiëntie, proteïne S-deficiëntie
- Zware operatie met langdurige immobilisatie (zie rubriek 4.4)
- Een hoog risico van veneuze trombo-embolie door de aanwezigheid van meerdere risicofactoren (zie rubriek 4.4);
- Trombogene valvulopathie;
- Trombogene hartritmestoornissen;
- Vermoeden of aanwezigheid van borstcarcinoom;
- Vermoeden of aanwezigheid van oestrogeenafhankelijke tumoren (endometrium,...);
- Leveradenoom of -carcinoom;
- Ernstig leverlijden tot normalisatie van de leverfunctie;
- Niet-gediagnosticeerde vaginale bloedingen;
- Vermoeden of aanwezigheid van zwangerschap;
- Overgevoeligheid voor de werkzame stoffen of voor één van de in rubriek 6.1 vermelde hulpstoffen.
- Aanwezigheid of voorgeschiedenis van pancreatitis geassocieerd met ernstige hypertriglyceridemie.
Harmonet is gecontra-indiceerd voor gelijktijdig gebruik met geneesmiddelen die ombitasvir/paritaprevir/ritonavir en dasabuvir bevatten, of geneesmiddelen die glecaprevir/pibrentasvir of sofosbuvir/velpatasvir/voxilaprevir bevatten (zie rubriek 4.5).
4.8 Bijwerkingen
Beschrijving van geselecteerde bijwerkingen
Er is een verhoogd risico waargenomen op arteriële en veneuze trombotische en trombo-embolische voorvallen, waaronder myocardinfarct, beroerte, transiënte ischemische aanvallen, veneuze trombose en longembolie bij vrouwen die gecombineerde hormonale anticonceptiva gebruikten. Hier wordt in rubriek 4.4 dieper op ingegaan.
Gebruik van orale HCC’s gaat ook gepaard met een verhoogd risico van:
- intra-epitheliale cervixneoplasie en cervixkanker;
- diagnose van borstkanker.
- goedaardige levertumoren (bijv. focale nodulaire hyperplasie, hepatisch adenoom)
Zie ook rubriek 4.4.
De volgende bijwerkingen staan per frequentiegroep als volgt opgelijst:
Zeer vaak ≥1/10
Vaak ≥1/100, < 1/10
Soms 1/1 000, <1/100
Zelden 1/10 000, <1/1 000
Zeer zelden <1/10 000
Frequentie niet bekend (kan met de beschikbare gegevens niet worden bepaald)
Systeem/orgaanklassen | Bijwerking |
Infecties en parasitaire aandoeningen |
|
Vaak | Vaginitis, waaronder vaginale candidiase |
Neoplasmata, benigne, maligne en niet-gespecificeerd (inclusief cysten en poliepen) | |
Immuunsysteemaandoeningen | |
Voedings- en stofwisselingsstoornissen |
|
Soms | Toegenomen of afgenomen eetlust |
Zelden | Glucose-intolerantie |
Zeer zelden | Opstoot van porfyrie |
Psychische stoornissen |
|
Vaak | Wijzigingen van de stemming en de libido, depressie |
Zenuwstelselaandoeningen |
|
Zeer vaak | Hoofdpijn, migraine |
Vaak | Nervositas, vertigo |
Zeer zelden | Opstoot van chorea |
Oogaandoeningen | |
Bloedvataandoeningen | |
Maagdarmstelselaandoeningen | |
Lever- en galaandoeningen | |
Huid- en onderhuidaandoeningen | |
Nier- en urinewegaandoeningen | |
Voortplantingsstelsel- en borstaandoeningen | |
Algemene aandoeningen en toedieningsplaatsstoornissen | |
Onderzoeken | |
* Neuritis optica kan partiële of volledige blindheid veroorzaken.
** Orale HCC’s kunnen een bestaande aandoening van de galblaas verergeren of het ontstaan van dergelijke aandoening activeren bij asymptomatische gebruiksters.
*** Het serumgehalte aan folaten kan dalen onder orale HCC’s. Dit kan van klinisch belang zijn indien de gebruikster snel na het stoppen van de pil zwanger raakt.
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be - Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be,
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Pfizer NV/SA
Pleinlaan 17
1050 Brussel
8. NUMMER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
BE174115
10. DATUM VAN HERZIENING VAN DE TEKST
03/2025
25B17
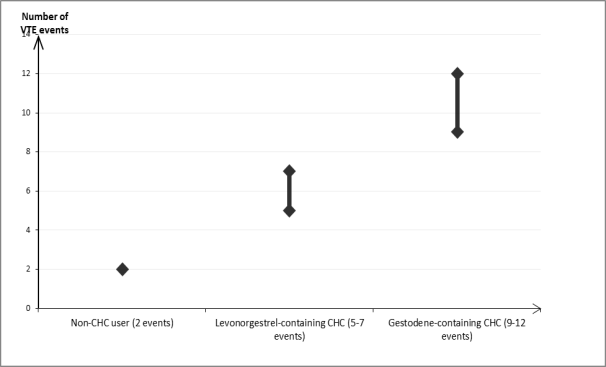
[1] Deze incidenties werden geschat op basis van alle epidemiologische onderzoeksgegevens samen, met gebruik van relatieve risico's voor de verschillende producten, vergeleken met levonorgestrelbevattende gecombineerde hormonale anticonceptiva.
[2] Middelste punt van het bereik ('mid-point of range') van 5‑7 per 10.000 vrouwjaren, op basis van een relatief risico voor levonorgestrelbevattende gecombineerde hormonale anticonceptiva versus niet-gebruik van ongeveer 2,3 tot 3,6
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 1224401 | HARMONET DRAG 3X21 | G03AA10 | € 15,42 | - | Ja | € 6,42 | € 6,42 |