1. NAAM VAN HET GENEESMIDDEL
Glivec 100 mg filmomhulde tabletten
Glivec 400 mg filmomhulde tabletten
2. KWALITATIEVE EN KWANTITATIEVE SAMENSTELLING
Glivec 100 mg filmomhulde tabletten
Elke filmomhulde tablet bevat 100 mg imatinib (als mesilaat).
Glivec 400 mg filmomhulde tabletten
Elke filmomhulde tablet bevat 400 mg imatinib (als mesilaat).
Voor de volledige lijst van hulpstoffen, zie rubriek 6.1.
3. FARMACEUTISCHE VORM
Filmomhulde tablet
Glivec 100 mg filmomhulde tabletten
Zeer donkergeel tot bruin-oranje filmomhulde tabletten, rond met “NVR” aan de ene zijde en “SA” en een breukstreep aan de andere zijde.
Glivec 400 mg filmomhulde tabletten
Zeer donkergeel tot bruin-oranje, ovale, biconvexe, filmomhulde tablet met schuine randen.
Tablet met de inscriptie “400” aan een zijde en een breukstreep aan de andere zijde met ‘SL’ aan elke kant van de breukstreep.
De filmomhulde tablet kan worden verdeeld in gelijke doses.
4. KLINISCHE GEGEVENS
4.1 Therapeutische indicaties
Glivec is geïndiceerd voor de behandeling van
- volwassen patiënten en kinderen met nieuw gediagnosticeerde Philadelphia chromosoom (bcr-abl) positieve (Ph+) chronische myeloïde leukemie (CML), voor wie beenmergtransplantatie niet als eerstelijnsbehandeling wordt beschouwd.
- volwassen patiënten en kinderen met Ph+ CML in de chronische fase na falen van interferon-alfa therapie, of in de acceleratiefase of in de blastaire crisis.
- volwassen patiënten en kinderen met nieuw gediagnosticeerde Philadelphia chromosoom positieve acute lymfoblastaire leukemie (Ph+ ALL) geïntegreerd met chemotherapie.
- volwassen patiënten met recidiverende of refractaire Ph+ ALL als monotherapie.
- volwassen patiënten met myelodysplastische/myeloproliferatieve ziekten (MDS/MPD) geassocieerd met herschikkingen van het platelet-derived growth factor receptor (PDGFR) gen.
- volwassen patiënten met hypereosinofiel syndroom (HES) in een gevorderd stadium en/of chronische eosinofiele leukemie (CEL) met FIP1L1-PDGFR herschikking.
Het effect van Glivec op het resultaat van beenmergtransplantatie werd niet bepaald.
Glivec is geïndiceerd voor
- de behandeling van volwassen patiënten met Kit (CD 117) positieve niet-reseceerbare en/of gemetastaseerde maligne gastrointestinale stromale tumoren (GIST).
- de adjuvante behandeling van volwassen patiënten die een significant risico hebben op recidief na resectie van Kit (CD117)-positieve GIST. Patiënten met een laag of zeer laag risico op recidief dienen geen adjuvante behandeling te krijgen.
- de behandeling van volwassen patiënten met niet-reseceerbare dermatofibrosarcoma protuberans (DFSP) en volwassen patiënten met terugkerende en/of gemetastaseerde DFSP die niet in aanmerking komen voor chirurgie.
Bij volwassen patiënten en kinderen is de doeltreffendheid van Glivec gebaseerd op algemene hematologische en cytogenetische responscijfers en progressievrije overleving in CML, op hematologische en cytogenetische responscijfers in Ph+ ALL, MDS/MPD, op hematologische responscijfers in HES/CEL en op objectieve responscijfers bij volwassen patiënten met niet-reseceerbare en/of gemetastaseerde GIST en DFSP en op recidief-vrije overleving bij adjuvante GIST. De ervaring met Glivec bij patiënten met MDS/MPD geassocieerd met PDGFR-gen herschikkingen is zeer beperkt (zie rubriek 5.1). Er zijn geen gecontroleerde onderzoeken die een klinisch voordeel of een verlengde overleving aantonen voor deze ziekten, behalve bij nieuw gediagnosticeerde CML in de chronische fase.
4.2 Dosering en wijze van toediening
De therapie dient zoals gebruikelijk te worden geïnitieerd door een arts die ervaring heeft in de behandeling van patiënten met hematologische maligniteiten en maligne sarcomen.
Voor andere doseringen dan 400 mg en 800 mg (zie doseringsaanbevelingen hieronder) zijn 100 mg en 400 mg deelbare tabletten beschikbaar.
De voorgeschreven dosis moet oraal worden ingenomen bij de maaltijd met een groot glas water om het risico op gastrointestinale irritaties te minimaliseren. Doses van 400 mg of 600 mg moeten eenmaal daags worden toegediend, terwijl een dagelijkse dosis van 800 mg moet worden toegediend als 400 mg tweemaal daags, ’s morgens en ’s avonds.
Voor patiënten die geen filmomhulde tabletten kunnen slikken, mogen de tabletten gedispergeerd worden in een glas niet bruisend water of appelsap. Het benodigde aantal tabletten moet in het geschikte volume drank (ongeveer 50 ml voor een 100 mg tablet, en 200 ml voor een 400 mg tablet) gedaan worden en omgeroerd worden met een lepel. De suspensie moet onmiddellijk worden toegediend na volledig uiteenvallen van de tablet(ten).
Dosering voor CML bij volwassen patiënten
De aanbevolen dosis van Glivec is 400 mg/dag voor volwassen patiënten in de chronische fase van CML. De chronische fase van CML wordt gedefinieerd als voldaan is aan alle volgende criteria: blasten <15% in bloed en beenmerg, perifere bloedbasofielen <20%, bloedplaatjes >100 x 109/l.
De aanbevolen dosis van Glivec is 600 mg/dag voor volwassen patiënten in de acceleratiefase. De acceleratiefase wordt gedefinieerd door de aanwezigheid van één van de volgende criteria: blasten 15% maar <30% in bloed of beenmerg, blasten en promyelocyten samen 30% in bloed of beenmerg (mits <30% blasten), perifere bloedbasofielen 20%, bloedplaatjes <100 x 109/l, onafhankelijk van de behandeling.
De aanbevolen dosis van Glivec is 600 mg/dag voor volwassen patiënten in de blastaire crisis. De blastaire crisis wordt gedefinieerd als blasten 30% in bloed of beenmerg of een extramedullaire ziekte verschillend van hepatosplenomegalie.
Behandelingsduur: In klinische onderzoeken werd de behandeling met Glivec voortgezet tot progressie van de ziekte. Het effect van het stopzetten van de behandeling na bereiken van een complete cytogenetische respons werd niet bestudeerd.
Er mag overwogen worden om de doses te verhogen van 400 mg tot 600 mg of 800 mg bij patiënten met de ziekte in chronische fase of van 600 mg tot een maximum van 800 mg (tweemaal daags een dosis van 400 mg) bij patiënten in de acceleratiefase of in de blastaire crisis. Deze dosisverhoging mag enkel gebeuren indien er geen ernstige bijwerkingen, niet-leukemie-gerelateerde neutropenie of trombocytopenie zijn opgetreden, onder de volgende omstandigheden: bij progressie van de ziekte (op elk tijdstip); in geval men er niet in slaagt een voldoende hematologische respons te bereiken na een behandeling van tenminste 3 maanden; in geval men er niet in slaagt een cytogenetische respons te bereiken na een behandeling van 12 maanden; of bij verlies van een eerder bereikte hematologische en/of cytogenetische respons. Patiënten moeten nauwkeurig gevolgd worden na een dosisverhoging, gezien de mogelijkheid tot een toegenomen incidentie van bijwerkingen bij hogere doses.
Dosering voor CML bij kinderen
De dosering voor kinderen dient gebaseerd te zijn op de lichaamsoppervlakte (mg/m2). De dosis van 340 mg/m2 per dag wordt aanbevolen voor kinderen in de chronische fase van CML en de gevorderde CML fasen (de totale dosis van 800 mg mag niet worden overschreden). De behandeling kan gegeven worden als een eenmaal daagse dosis, als alternatief mag de dagelijkse dosis verdeeld worden over twee toedieningen – één 's morgens en één 's avonds. De dosisaanbeveling is momenteel gebaseerd op een klein aantal pediatrische patiënten (zie rubrieken 5.1 en 5.2). Er is geen ervaring in de behandeling van kinderen jonger dan 2 jaar.
Dosisverhoging van 340 mg/m2 per dag tot 570 mg/m2 per dag (de totale dosis van 800 mg mag niet worden overschreden) kan worden overwogen bij kinderen indien er geen ernstige bijwerkingen of ernstige niet-leukemie-gerelateerde neutropenie of trombocytopenie zijn opgetreden, onder de volgende omstandigheden: bij progressie van de ziekte (op elk tijdstip); indien men er niet in slaagt een voldoende hematologische respons te bereiken na een behandeling van tenminste 3 maanden; indien men er niet in slaagt een cytogenetische respons te bereiken na een behandeling van 12 maanden; of bij verlies van een eerder bereikte hematologische en/of cytogenetische respons. Patiënten moeten nauwkeurig gevolgd worden na een dosisverhoging, gezien de mogelijkheid tot een toegenomen incidentie van bijwerkingen bij hogere doses.
Dosering voor Ph+ ALL bij volwassen patiënten
De aanbevolen dosis van Glivec is 600 mg/dag voor volwassen patiënten met Ph+ ALL. Hematologen die gespecialiseerd zijn in de behandeling van deze ziekte dienen toezicht te houden op alle behandelingsfasen van de therapie.
Behandelingsschema: bestaande gegevens hebben de doeltreffendheid en veiligheid van Glivec aangetoond, wanneer een dosis van 600 mg/dag werd toegediend in combinatie met chemotherapie in de inductie-, consolidatie- en onderhoudsfase (zie rubriek 5.1) voor volwassen patiënten met nieuw gediagnosticeerd Ph+ ALL. De duur van de Glivecbehandeling kan variëren met het gekozen behandelingsprogramma, maar in het algemeen geven langere blootstellingen aan Glivec betere resultaten.
Voor volwassen patiënten met recidiverende of refractaire Ph+ ALL is Glivec monotherapie in een dosering van 600 mg/dag veilig en doeltreffend en kan het worden gegeven totdat progressie van de ziekte optreedt.
Dosering voor Ph+ ALL bij kinderen
De dosering voor kinderen dient gebaseerd te zijn op de lichaamsoppervlakte (mg/m2). De dosis van 340 mg/m2 per dag wordt aanbevolen voor kinderen met Ph+ ALL (totale dosis niet hoger dan 600 mg).
Dosering voor MDS/MPD
De aanbevolen dosis van Glivec is 400 mg/dag voor volwassen patiënten met MDS/MPD.
Behandelingsduur: In het enige klinische onderzoek dat tot nu toe is uitgevoerd, werd de behandeling met Glivec voortgezet tot ziekteprogressie (zie rubriek 5.1). Ten tijde van de analyse bedroeg de behandelingsduur mediaan 47 maanden (24 dagen - 60 maanden).
Dosering voor HES/CEL
De aanbevolen dosis van Glivec is 100 mg/dag voor volwassen patiënten met HES/CEL.
Een dosisverhoging van 100 mg naar 400 mg mag voor deze patiënten worden overwogen in afwezigheid van bijwerkingen als evaluaties een onvoldoende respons op de behandeling aantonen.
De behandeling dient te worden voortgezet zolang de patiënt er baat bij heeft.
Dosering voor GIST
De aanbevolen dosis van Glivec is 400 mg/dag voor volwassen patiënten met niet-reseceerbare en/of gemetastaseerde maligne GIST.
Er bestaan beperkte gegevens over het effect van dosisverhogingen van 400 mg tot 600 mg of 800 mg bij patiënten die progressie van de ziekte vertonen bij de lagere dosis (zie rubriek 5.1).
Behandelingsduur: In klinische onderzoeken bij GIST-patiënten, werd de behandeling met Glivec voortgezet tot progressie van de ziekte. Op het moment van de analyse, was de mediane behandelingsduur 7 maanden (7 dagen tot 13 maanden). Het effect van stopzetten van de behandeling na het bereiken van een respons is niet onderzocht.
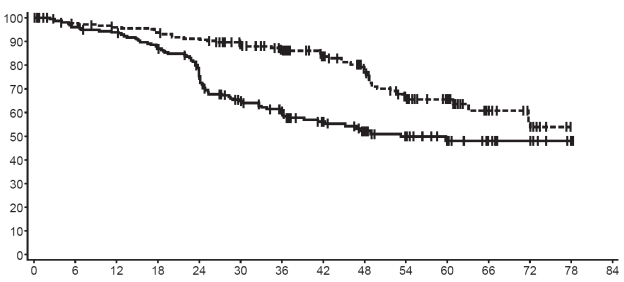
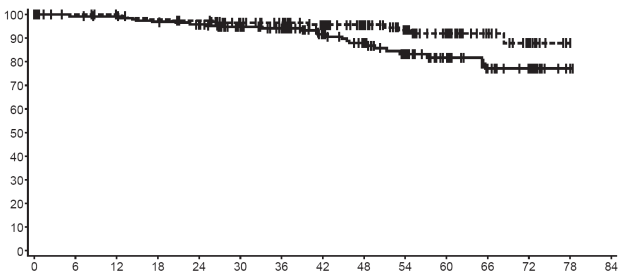
De aanbevolen Glivec-dosis is 400 mg/dag voor de adjuvante behandeling van volwassen patiënten volgend op resectie van GIST. De optimale behandelingsduur is nog niet bepaald. De duur van de behandeling in het klinisch onderzoek voor de onderbouwing van deze indicatie was 36 maanden (zie rubriek 5.1).
Dosering voor DFSP
De aanbevolen dosis van Glivec is 800 mg/dag voor volwassen patiënten met DFSP.
Dosisaanpassing in geval van bijwerkingen
Niet-hematologische bijwerkingen
Indien een ernstige niet-hematologische bijwerking ontstaat door het gebruik van Glivec, moet de behandeling onderbroken worden totdat de bijwerking verdwenen is. Hierna kan de behandeling hervat worden, zoals voorgeschreven afhankelijk van de oorspronkelijke ernst van de bijwerking.
Indien verhogingen van bilirubine >3 x de “institutional upper limit of normal (IULN)” of van levertransaminasen >5 x IULN optreden, moet Glivec gestopt worden tot de bilirubinewaarden tot een niveau <1,5 x IULN zijn teruggekeerd en de transaminasewaarden tot <2,5 x IULN. De behandeling met Glivec mag dan voortgezet worden met een gereduceerde dagelijkse dosis. Bij volwassenen dient de dosis gereduceerd te worden van 400 tot 300 mg of van 600 tot 400 mg, of van 800 tot 600 mg, en bij kinderen van 340 tot 260 mg/m2/dag.
Hematologische bijwerkingen
Dosisvermindering of stopzetting van de behandeling vanwege ernstige neutropenie en trombocytopenie worden aanbevolen, zoals aangeduid in onderstaande tabel.
Dosisaanpassingen in geval van neutropenie en trombocytopenie:
HES/CEL (startdosis 100 mg) | ANC <1,0 x 109/l | 1. Stop Glivec tot ANC 1,5 x 109/l en bloedplaatjes 75 x 109/l. |
Chronische fase CML, MDS/MPD en GIST (startdosis 400 mg) | ANC <1,0 x 109/l | 1. Stop Glivec tot ANC 1,5 x 109/l en bloedplaatjes 75 x 109/l. |
Chronische fase CML bij kinderen | ANC <1,0 x 109/l | 1. Stop Glivec tot ANC 1,5 x 109/l en bloedplaatjes 75 x 109/l. |
Acceleratiefase CML en blastaire crisis en Ph+ ALL (startdosis 600 mg) | aANC <0,5 x 109/l | 1. Onderzoek of de cytopenie verwant is met de leukemie (via mergaspiratie of biopsie). |
Acceleratiefase CML en blastaire crisis bij kinderen (startdosis 340 mg/m2) | aANC <0,5 x 109/l | 1. Onderzoek of de cytopenie verwant is met de leukemie (via merg-aspiratie of biopsie). |
DFSP | ANC <1,0 x 109/l | 1. Stop Glivec totdat ANC 1,5 x 109/l en bloedplaatjes 75 x 109/l. |
ANC = absolute neutrophil count | ||
a optredend na tenminste 1 maand behandeling | ||
Speciale patiëntgroepen
Pediatrische patiënten
Er is geen ervaring bij kinderen jonger dan 2 jaar met CML en bij kinderen jonger dan 1 jaar met Ph+ ALL (zie rubriek 5.1). De ervaring bij kinderen met MDS/MPD, DFSP, GIST en HES/CEL is zeer beperkt.
De veiligheid en werkzaamheid van imatinib bij kinderen jonger dan 18 jaar met MDS/MPD, DFSP, GIST en HES/CEL zijn niet vastgesteld in klinische studies. De momenteel beschikbare, gepubliceerde gegevens worden samengevat in rubriek 5.1, maar er kan geen doseringsadvies worden gegeven.
Leverinsufficiëntie
Imatinib wordt voornamelijk via de lever gemetaboliseerd. De minimum aanbevolen dosis van 400 mg per dag moet worden gegeven aan patiënten met milde, matige of ernstige leverfunctiestoornissen. De dosis kan worden verlaagd indien deze niet wordt verdragen (zie rubrieken 4.4, 4.8 en 5.2).
Classificatie van leverfunctiestoornissen:
Leverfunctiestoornis | Leverfunctie testen |
Mild | Totaal bilirubine: = 1,5 ULN |
Matig | Totaal bilirubine: >1,5–3,0 ULN |
Ernstig | Totaal bilirubine: >3–10 ULN |
ULN = gebruikelijke “upper limit of normal” | |
Nierinsufficiëntie
De minimale aanbevolen dosis van 400 mg per dag dient als startdosis te worden gegeven aan patiënten met nierfunctiestoornissen of aan patiënten die gedialyseerd worden. Nochtans is bij deze patiënten voorzichtigheid geboden. De dosis kan worden verlaagd indien de behandeling niet wordt verdragen. Indien de behandeling wordt verdragen, kan de dosis bij gebrek aan werkzaamheid worden verhoogd (zie rubrieken 4.4 en 5.2).
Ouderen
De farmacokinetiek van imatinib werd niet in het bijzonder bestudeerd bij ouderen. Er werden geen significante leeftijdsgebonden farmacokinetische verschillen waargenomen bij volwassen patiënten in klinische onderzoeken, welke meer dan 20% patiënten omvatten van 65 jaar en ouder. Er is geen specifieke dosisaanbeveling noodzakelijk voor ouderen.
4.3 Contra-indicaties
Overgevoeligheid voor de werkzame stof of voor een van de in rubriek 6.1 vermelde hulpstoffen.
4.8 Bijwerkingen
Patiënten in gevorderde stadia van kanker kunnen talrijke complicerende medische aandoeningen hebben die het moeilijk maken de oorzaak van de bijwerking te bepalen. Dit komt door de variëteit van symptomen die gerelateerd zijn aan de onderliggende ziekte, de progressie van de ziekte en de gelijktijdige toediening van talrijke geneesmiddelen.
In klinische onderzoeken bij CML werd het stopzetten van het geneesmiddel door bijwerkingen die gerelateerd waren aan het geneesmiddel gezien bij 2,4% van de nieuw gediagnosticeerde patiënten, 4% van de patiënten in de late chronische fase na falen van interferon therapie, 4% van de patiënten in de acceleratiefase na falen van interferon therapie en 5% van de patiënten in de blastaire crisis na falen van interferon therapie. Bij GIST werd bij 4% van de patiënten het studiegeneesmiddel stopgezet ten gevolge van bijwerkingen die gerelateerd waren aan het geneesmiddel.
De bijwerkingen waren vergelijkbaar bij alle indicaties, met twee uitzonderingen. Er werd meer myelosuppressie gezien bij CML patiënten dan bij GIST, wat waarschijnlijk te wijten is aan de onderliggende ziekte. In de studie bij patiënten met niet-reseceerbare en/of gemetastaseerde GIST vertoonden 7 (5%) patiënten CTC graad 3/4 gastro-intestinale bloedingen (3 patiënten), intra-tumorale bloedingen (3 patiënten) of beide (1 patiënt). Gastro-intestinale situering van de tumor kan de bron zijn geweest van de gastro-intestinale bloedingen (zie rubriek 4.4). Gastro-intestinale en tumorale bloedingen kunnen ernstig zijn en soms fataal. De meest vaak gerapporteerde (≥10%) geneesmiddel-gerelateerde bijwerkingen in beide gevallen waren lichte misselijkheid, braken, diarree, buikpijn, vermoeidheid, spierpijn, spierkrampen en rash. Oppervlakkige oedemen werden in alle studies vaak waargenomen en werden hoofdzakelijk beschreven als periorbitale oedemen of oedeem van de onderste ledematen. Deze oedemen waren echter zelden ernstig en kunnen behandeld worden met diuretica of andere ondersteunende maatregelen of door de dosis van Glivec te verlagen.
Wanneer imatinib werd gecombineerd met hoge dosis chemotherapie bij Ph+ ALL patiënten, werd voorbijgaande levertoxiciteit in de vorm van transaminaseverhoging en hyperbilirubinemie waargenomen. Rekening houdend met de beperkte veiligheidsdatabank, zijn de bijwerkingen tot nu toe gemeld bij kinderen in overeenstemming met het bekende veiligheidsprofiel bij volwassen patiënten met Ph+ ALL. De veiligheidsdatabank voor kinderen met Ph+ ALL is erg beperkt. Toch zijn er geen nieuwe veiligheidsproblemen geïdentificeerd.
Verschillende bijwerkingen zoals pleurale effusie, ascites, pulmonair oedeem en een snelle gewichtstoename, met of zonder oppervlakkig oedeem, kunnen gezamenlijk worden beschreven als “vochtretentie”. Deze bijwerkingen kunnen gewoonlijk verholpen worden door een tijdelijke onderbreking van Glivec en door diuretica en andere gepaste ondersteunende verzorgingsmaatregelen. Echter, sommige van deze bijwerkingen kunnen ernstig of levensbedreigend zijn. Enkele patiënten, met een complexe klinische voorgeschiedenis van pleurale effusie, congestief hart- en nierfalen, stierven tijdens een blastaire crisis. Er waren geen speciale veiligheidsbevindingen in de klinische onderzoeken bij kinderen.
Bijwerkingen
Bijwerkingen die vaker gemeld zijn dan een enkel geïsoleerd geval worden hieronder opgesomd volgens de systeem orgaan klasse en volgens frequentie. Frequentiegroepen zijn gedefinieerd volgens de volgende afspraak: zeer vaak (1/10), vaak (1/100, <1/10), soms (1/1.000, <1/100), zelden (1/10.000, <1/1.000), zeer zelden (<1/10.000), niet bekend (kan met de beschikbare gegevens niet worden bepaald).
Binnen iedere frequentiegroep worden bijwerkingen gerangschikt naar frequentie, beginnend bij de meest voorkomende.
Bijwerkingen en hun frequenties zijn gemeld in Tabel 1.
Tabel 1 Samenvatting van bijwerkingen in tabelvorm
Infecties en parasitaire aandoeningen | |
Soms: | Herpes zoster, herpes simplex, nasofaryngitis, pneumonie1, sinusitis, cellulitis, infectie van de bovenste luchtwegen, influenza, urineweginfectie, gastro-enteritis, sepsis |
Zelden: | Schimmelinfectie |
Niet bekend: | Hepatitis B-reactivering* |
Neoplasmata, benigne, maligne en niet-gespecificeerd (inclusief cysten en poliepen) | |
Zelden: | Tumorlysissyndroom |
Niet bekend: | Tumorbloeding/tumornecrose* |
Immuunsysteemaandoeningen | |
Niet bekend: | Anafylactische shock* |
Bloed- en lymfestelselaandoeningen | |
Zeer vaak: | Neutropenie, trombocytopenie, anemie |
Vaak: | Pancytopenie, febriele neutropenie |
Soms: | Trombocytemie, lymfopenie, beenmergdepressie, eosinofilie, lymfadenopathie |
Zelden: | Hemolytische anemie, trombothische microangiopathie |
Voedings- en stofwisselingsstoornissen | |
Vaak: | Anorexie |
Soms: | Hypokaliëmie, toegenomen eetlust, hypofosfatemie, verminderde eetlust, dehydratie, jicht, hyperurikemie, hypercalciëmie, hyperglykemie, hyponatriëmie |
Zelden: | Hyperkaliëmie, hypomagnesiëmie |
Psychische stoornissen | |
Vaak: | Slapeloosheid |
Soms: | Depressie, verminderd libido, angstgevoel |
Zelden: | Toestand van verwarring |
Zenuwstelselaandoeningen | |
Zeer vaak: | Hoofdpijn2 |
Vaak: | Duizeligheid, paresthesie, smaakstoornissen, hypo-esthesie |
Soms: | Migraine, slaperigheid, flauwvallen, perifere neuropathie, geheugenstoornissen, ischias, restless legs-syndroom, tremor, hersenbloeding |
Zelden: | Verhoogde intracraniële druk, convulsies, optische neuritis |
Niet bekend: | Cerebraal oedeem* |
Oogaandoeningen | |
Vaak: | Ooglidoedeem, verhoogde tranenvloed, conjunctivale bloeding, conjunctivitis, droge ogen, troebel zicht |
Soms: | Oogirritatie, oogpijn, orbitaal oedeem, sclerale bloeding, retinale bloeding, blefaritis, maculair oedeem |
Zelden: | Cataract, glaucoom, papiloedeem |
Niet bekend: | Vitreale bloeding* |
Evenwichtsorgaan- en ooraandoeningen | |
Soms: | Vertigo, tinnitus, gehoorverlies |
Hartaandoeningen | |
Soms: | Hartkloppingen, tachycardie, congestief hartfalen3, longoedeem |
Zelden: | Aritmieën, atriumfibrilleren, hartstilstand, myocardinfarct, angina pectoris, pericardiale effusie |
Niet bekend: | Pericarditis*, harttamponade* |
Bloedvataandoeningen4 | |
Vaak: | Blozen, bloedingen |
Soms: | Hypertensie, bloeduitstorting, subduraal hematoom, perifeer koudegevoel, hypotensie, Raynaud-fenomeen |
Niet bekend: | Trombose/embolie* |
Ademhalingsstelsel-, borstkas- en mediastinumaandoeningen | |
Vaak: | Dyspnoe, neusbloeding, hoest |
Soms: | Pleurale effusie5, faryngolaryngeale pijn, keelontsteking |
Zelden: | Pleuritische pijn, longfibrose, pulmonaire hypertensie, longbloeding |
Niet bekend: | Acuut respiratoir falen11*, interstitiële longaandoening* |
Maagdarmstelselaandoeningen | |
Zeer vaak: | Misselijkheid, diarree, braken, dyspepsie, buikpijn6 |
Vaak: | Flatulentie, opgezwollen buik, gastro-oesofageale reflux, constipatie, droge mond, gastritis |
Soms: | Stomatitis, zweren in de mond, gastro-intestinale bloeding7, oprisping, melaena, oesofagitis, ascites, maagzweer, haematemesis, cheilitis, dysfagie, pancreatitis |
Zelden: | Colitis, ileus, chronische darmontstekingen |
Niet bekend: | Ileus/darmobstructie*, gastro-intestinale perforatie*, diverticulitis*, “gastric antral vascular ectasia” (GAVE)* |
Lever- en galaandoeningen | |
Vaak: | Verhoogde leverenzymen |
Soms: | Hyperbilirubinemie, hepatitis, geelzucht |
Zelden: | Leverfalen8, levernecrose |
Huid- en onderhuidaandoeningen | |
Zeer vaak: | Periorbitaal oedeem, dermatitis/eczeem/rash |
Vaak: | Pruritus, gelaatsoedeem, droge huid, erytheem, alopecia, nachtelijk zweten, lichtovergevoeligheidsreactie |
Soms: | Pustulaire rash, kneuzing, toegenomen zweten, urticaria, blauwe plekken, verhoogde neiging tot kneuzingen, hypotrichosis, hypopigmentatie van de huid, exfoliatieve dermatitis, onychoclasis, folliculitis, petechieën, psoriasis, purpura, hyperpigmentatie van de huid, bulleuze erupties, panniculitis12 |
Zelden: | Acute febriele neutrofiele dermatosis (Sweet’s syndroom), verkleuring van de nagels, angioneurotisch oedeem, vesiculaire rash, erythema multiforme, leukocytoclastische vasculitis, Stevens-Johnson syndroom, acute gegeneraliseerde exanthemateuze pustulose (AGEP), pemphigus* |
Niet bekend: | Palmoplantair erytrodysesthesiesyndroom*, lichenoïde keratose*, lichen planus*, toxische epidermale necrolyse*, medicamenteuze rash met eosinofilie en systemische symptomen (DRESS)*, pseudoporfyrie* |
Skeletspierstelsel- en bindweefselaandoeningen | |
Zeer vaak: | Spierspasme en krampen, pijn van de skeletspieren met inbegrip van myalgie9, artralgie, botpijn10 |
Vaak: | Zwelling van de gewrichten |
Soms: | Stijfheid van gewrichten en spieren, osteonecrose* |
Zelden: | Spierzwakte, artritis, rabdomyolyse/myopathie |
Niet bekend: | Groeivertraging bij kinderen* |
Nier- en urinewegaandoeningen | |
Soms: | Nierpijn, hematurie, acuut nierfalen, verhoogde urinaire frequentie |
Niet bekend: | Chronisch nierfalen |
Voortplantingsstelsel- en borstaandoeningen | |
Soms: | Gynaecomastie, erectiele disfunctie, menorragie, onregelmatige menstruatie, seksuele disfunctie, tepelpijn, vergroting van de borst, scrotumoedeem |
Zelden: | Hemorragische corpus luteum/hemorragische ovariumcyste |
Algemene aandoeningen en toedieningsplaatsstoornissen | |
Zeer vaak: | Vochtretentie en oedeem, moeheid |
Vaak: | Zwakte, koorts, anasarca, koude rillingen, koortsrillingen |
Soms: | Pijn op de borst, malaise |
Onderzoeken | |
Zeer vaak: | Gewichtstoename |
Vaak: | Gewichtsafname |
Soms: | Verhoogd bloedcreatinine, verhoogd bloedcreatinefosfokinase, verhoogd bloedlactaatdehydrogenase, verhoogde alkalische fosfatase in bloed |
Zelden: | Verhoogd bloedamylase |
* Deze reactietypes zijn met name meldingen uit postmarketingervaring met Glivec. Deze omvatten zowel spontane meldingen als ernstige bijwerkingen uit lopende studies, de “expanded access” programma’s, klinische farmacologiestudies en explorerende studies voor niet‑geregistreerde indicaties. Omdat deze bijwerkingen zijn gemeld in een populatie met onduidelijke grootte, is het niet altijd mogelijk om een betrouwbare schatting te maken van hun frequentie of om een causaal verband met imatinibblootstelling vast te stellen. | |
Abnormale laboratoriumtesten
Hematologie
Bij CML werd cytopenie, met name neutropenie en trombocytopenie, consequent gezien in alle studies met de suggestie van een hogere frequentie bij hoge doses ≥750 mg (fase I-studie). Echter, het vóórkomen van cytopenie was ook duidelijk afhankelijk van het stadium van de ziekte, de frequentie van graad 3 of 4 neutropenie (ANC <1,0 x 109/l) en trombocytopenie (bloedplaatjes aantal <50 x 109/l) was tussen 4 en 6 keer hoger in de blastaire crisis en acceleratiefase (59–64% en 44–63% voor respectievelijk neutropenie en trombocytopenie) in vergelijking met nieuw gediagnosticeerde chronische fase van CML (16,7% neutropenie en 8,9% trombocytopenie). In nieuw gediagnosticeerde chronische fase van CML werden graad 4 neutropenie (ANC <0,5 x 109/l) en trombocytopenie (bloedplaatjes aantal <10 x 109/l) gezien bij respectievelijk 3,6% en <1% van de patiënten. De mediane duur van de neutropenische en trombocytopenische episodes varieerde meestal respectievelijk van 2 tot 3 weken en van 3 tot 4 weken. Deze verschijnselen kunnen meestal verholpen worden door of een reductie van de dosis of een onderbreking van de behandeling met Glivec. Ze kunnen echter in zeldzame gevallen leiden tot een permanent stoppen van de behandeling. De meest frequent gerapporteerde toxiciteiten bij kinderen met CML waren graad 3 of 4 cytopenieën waaronder neutropenie, trombocytopenie en anemie. Deze treden in het algemeen op binnen de eerste paar maanden van de therapie.
In de studie bij patiënten met niet-reseceerbare en/of gemetastaseerde GIST werd graad 3 en 4 anemie gerapporteerd in respectievelijk 5,4% en 0,7% van de patiënten, en bij tenminste enkele van deze patiënten zou dit gerelateerd kunnen zijn aan gastro-intestinale of intra-tumorale hemorragieën. Graad 3 en 4 neutropenie werd waargenomen in respectievelijk 7,5% en 2,7% van de patiënten en graad 3 trombocytopenie in 0,7% van de patiënten. Geen enkele patiënt ontwikkelde graad 4 trombocytopenie. De afnames in witte bloedcel (WBC)- en neutrofieltellingen traden voornamelijk op tijdens de eerste zes weken van de behandeling, met nadien waarden die betrekkelijk stabiel bleven.
Biochemie
Ernstige stijging van transaminasen (<5%) of bilirubine (<1%) was waargenomen bij CML patiënten en werd meestal verholpen door dosis-reductie of -onderbreking (de mediane duur voor deze episodes was ongeveer een week). Bij minder dan 1% van de CML patiënten werd de behandeling permanent gestopt vanwege abnormale leverfunctiewaarden. Bij GIST-patiënten (studie B2222) werden 6,8% graad 3 of 4 ALT (alanine aminotransferase) stijgingen en 4,8% graad 3 of 4 AST (aspartaat aminotranserase) stijgingen waargenomen. De bilirubine stijging was lager dan 3%.
Er zijn gevallen van cytolytische en cholestatische hepatitis en leverfalen; in sommige van deze gevallen was dit fataal, waaronder één patiënt op hoge dosis paracetamol.
Beschrijving van geselecteerde bijwerkingen
Hepatitis B-reactivering
Hepatitis B-reactivering is gemeld in verband met zogenaamde BCR-ABL-TKI's (Bcr-abl-tyrosinekinaseremmers). In een aantal gevallen resulteerde dit in acuut leverfalen of fulminante hepatitis die leidde tot levertransplantatie of een fatale afloop (zie rubriek 4.4).
Melding van vermoedelijke bijwerkingen
Het is belangrijk om na toelating van het geneesmiddel vermoedelijke bijwerkingen te melden. Op deze wijze kan de verhouding tussen voordelen en risico’s van het geneesmiddel voortdurend worden gevolgd. Beroepsbeoefenaren in de gezondheidszorg wordt verzocht alle vermoedelijke bijwerkingen te melden via:
België
Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten
www.fagg.be
Afdeling Vigilantie:
Website: www.eenbijwerkingmelden.be
e-mail: adr@fagg-afmps.be
7. HOUDER VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Ierland
8. NUMMER(S) VAN DE VERGUNNING VOOR HET IN DE HANDEL BRENGEN
Glivec 100 mg filmomhulde tabletten
EU/1/01/198/007
EU/1/01/198/008
EU/1/01/198/011
EU/1/01/198/012
EU/1/01/198/014
EU/1/01/198/015
EU/1/01/198/016
Glivec 400 mg filmomhulde tabletten
EU/1/01/198/009
EU/1/01/198/010
EU/1/01/198/013
10. DATUM VAN HERZIENING VAN DE TEKST
16.10.2025
Gedetailleerde informatie over dit geneesmiddel is beschikbaar op de website van het Europees Geneesmiddelenbureau https://www.ema.europa.eu
PRIJZEN
| CNK code | Verpakking | ATC5 code | Prijs | Af-fabriek prijs | Voorschriftplichtig | Remgeld reguliere tegemoetkoming | Remgeld verhoogde tegemoetkoming |
|---|---|---|---|---|---|---|---|
| 2083392 | GLIVEC 400MG FILMOMH TABL 30 X 400MG | L01EA01 | € 828,46 | - | Ja | € 2 | € 1 |
| 4422911 | GLIVEC 100MG FILMOMH TABL 120 | L01EA01 | € 846,04 | - | Ja | € 2 | € 1 |