1. NAAM VAN HET DIERGENEESMIDDEL
Bravecto 112,5 mg spot-on oplossing voor kleine katten (1,2 - 2,8 kg)
Bravecto 250 mg spot-on oplossing voor middelgrote katten (>2,8 - 6,25 kg)
Bravecto 500 mg spot-on oplossing voor grote katten (>6,25 - 12,5 kg)
4. FARMACOLOGISCHE GEGEVENS
4.1 ATCvet-code: QP53BE02
4.2 Farmacodynamische eigenschappen
Fluralaner is een acaricide en een insecticide. Het is werkzaam tegen teken (Ixodes spp.), vlooien (Ctenocephalides spp.) en oormijten (Otodectes cynotis) bij de kat.
Binnen 12 uur na aanhechting van vlooien (C. felis) en binnen 48 uur na aanhechting van teken (I. ricinus) treedt het effect op.
Fluralaner is zeer potent tegen teken en vlooien door blootstelling tijdens het voeden, m.a.w. het is systemisch werkzaam tegen de doelparasieten.
Fluralaner is een sterke remmer van delen van het zenuwstelsel van geleedpotigen door de antagonistische werking op ligandafhankelijke chloridekanalen (GABA-receptor en glutamaat-receptor).
Bij moleculaire on target studies op insect GABA receptoren van de vlo en de vlieg wordt fluralaner niet beïnvloed door dieldrinresistentie.
Bij in vitro bio-assays wordt fluralaner niet beïnvloed door bewezen veldresistentie tegen amidines (teken), organofosfaten (teken, mijten), cyclodiënes (teken, vlooien, vliegen), macrocyclische lactonen (zeeluizen), fenylpyrazolen (teken, vlooien), benzofenyl urea (teken), pyrethroïden (teken, mijten) en carbamaten (mijten).
Het diergeneesmiddel draagt bij aan de beheersing van de vlooienpopulatie in de omgeving waar de behandelde katten toegang tot hebben.
Nieuwe vlooien op een kat worden gedood voordat ze levensvatbare eitjes kunnen produceren. Een in vitro studie liet tevens zien dat een zeer lage concentratie van fluralaner de productie van levensvatbare eitjes bij vlooien stopt.
De levenscyclus van de vlo wordt doorbroken door het snelle en langdurige effect tegen volwassen vlooien op het dier en de afwezigheid van de productie van levensvatbare eieren.
4.3 Farmacokinetische eigenschappen
Fluralaner wordt gemakkelijk transdermaal opgenomen van de topicale toedieningsplek waarbij maximale plasmaconcentraties tussen 3 en 21 dagen na toediening worden bereikt. De langdurige aanwezigheid en langzame eliminatie uit het plasma (t1/2 = 12 dagen) en het gebrek aan een uitgebreid metabolisme resulteren in werkzame concentraties fluralaner voor de duur van het doseringsinterval. Onveranderd fluralaner wordt uitgescheiden via de faeces en in zeer kleine mate via de urine.
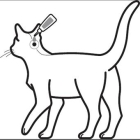
 Stap 1: Onmiddellijk voor gebruik het sachet openen en de pipet eruit halen. Doe handschoenen aan. De pipet dient bij de basis of bij het harde bovenste deel onder de dop rechtop vastgehouden te worden (punt naar boven) om deze te openen. De draai-en-gebruik dop dient met de klok mee of tegen de klok in één keer rondgedraaid te worden. De dop zal op de pipet blijven; het is niet mogelijk deze te verwijderen. De pipet is open
Stap 1: Onmiddellijk voor gebruik het sachet openen en de pipet eruit halen. Doe handschoenen aan. De pipet dient bij de basis of bij het harde bovenste deel onder de dop rechtop vastgehouden te worden (punt naar boven) om deze te openen. De draai-en-gebruik dop dient met de klok mee of tegen de klok in één keer rondgedraaid te worden. De dop zal op de pipet blijven; het is niet mogelijk deze te verwijderen. De pipet is open