SAMENVATTING VAN DE PRODUCTKENMERKEN
1. NAAM VAN HET DIERGENEESMIDDEL
Clindabactin 55 mg kauwtabletten voor honden en katten
4. KLINISCHE GEGEVENS
4.2 Indicaties voor gebruik met specificatie van de doeldiersoort(en)
Honden
Voor de behandeling van geïnfecteerde wonden, abcessen en infecties van de mondholte, met inbegrip van parodontale aandoeningen, veroorzaakt door of geassocieerd met Staphylococcus spp., Streptococcus spp. (met uitzondering van Streptococcus faecalis), Bacteroides spp., Fusobacterium necrophorum en Clostridium perfringens gevoelig voor clindamycine.
Voor de behandeling van oppervlakkige pyodermie geassocieerd met Staphylococcus pseudintermedius gevoelig voor clindamycine.
Voor de behandeling van osteomyelitis, veroorzaakt door Staphylococcus aureus gevoelig voor clindamycine.
Katten
Voor de behandeling van geïnfecteerde wonden, abcessen en infecties van de mondholte, met inbegrip van parodontale aandoeningen, veroorzaakt door bacteriën die gevoelig zijn voor clindamycine.
4.3 Contra-indicaties
Niet gebruiken bij overgevoeligheid voor het werkzame bestanddeel of één van de hulpstoffen of voor lincomycine. Niet toedienen aan konijnen, hamsters, cavia’s, chinchilla’s, paarden en herkauwers, want ingestie van clindamycine kan bij deze diersoorten ernstige gastro-intestinale stoornissen veroorzaken waaraan het dier kan sterven.
4.8 Interactie met andere geneesmiddelen en andere vormen van interactie
Het is aangetoond dat clindamycinehydrochloride neuromusculaire blokkerende eigenschappen vertoont die het werkingsmechanisme van andere neuromusculaire blokkerende stoffen kan versterken. Voorzichtigheid is geboden wanneer het diergeneesmiddel wordt gebruikt bij dieren die dergelijke stoffen krijgen.
Aluminiumzouten en -hydroxiden, kaolien en aluminium-magnesium-silicaatcomplex kunnen de absorptie van lincosamiden verminderen. Deze spijsverteringsstoffen moeten ten minste 2 uur vóór clindamycine worden toegediend.
Clindamycine mag niet gelijktijdig met of onmiddellijk na erythromycine of andere macroliden worden gebruikt om macrolide-geïnduceerde resistentie voor clindamycine te voorkomen.
Clindamycine kan de plasmawaarden van cyclosporine verminderen met een risico op een gebrek aan activiteit.
Tijdens het gelijktijdige gebruik van clindamycine en aminoglycosiden (bv. gentamicine) kan het risico op ongewenste interacties (acuut nierfalen) niet worden uitgesloten.
Clindamycine mag niet gelijktijdig met chlooramfenicol of macroliden worden gebruikt, aangezien ze elkaar antagoneren op hun aangrijpingspunt aan ribosoomonderdeel 50S.
4.9 Dosering en toedieningsweg
Oraal gebruik.
1. Voor de behandeling van geïnfecteerde wonden, abcessen en infecties van de mondholte, met inbegrip van parodontale aandoeningen bij honden en katten,:
• 5,5 mg/kg lichaamsgewicht om de 12 uur gedurende 7 tot 10 dagen, OF
• 11 mg/kg lichaamsgewicht om de 24 uur gedurende 7 tot 10 dagen
Als er binnen 4 dagen geen klinische respons wordt waargenomen, moet de diagnose worden herzien.
2. Voor de behandeling van oppervlakkige pyodermie bij honden:
• 5,5 mg/kg lichaamsgewicht om de 12 uur, OF
• 11 mg/kg lichaamsgewicht om de 24 uur
Behandeling van oppervlakkige pyodermie bij honden wordt gewoonlijk aanbevolen voor een periode van 21 dagen. Het is mogelijk de behandeling te verkorten of te verlengen op basis van een klinisch oordeel.
3. Voor de behandeling van osteomyelitis bij honden:
• 11 mg/kg lichaamsgewicht om de 12 uur gedurende minimaal 28 dagen
Als er binnen 14 dagen geen klinische respons wordt waargenomen, moet de behandeling worden stopgezet en de diagnose worden herzien.
Teneinde een juiste dosering te berekenen, dient het lichaamsgewicht zo nauwkeurig mogelijk te worden bepaald. Dit om onderdosering te vermijden. Tabletten kunnen in twee of vier gelijke delen worden verdeeld om een accurate dosering te verzekeren. Leg de tablet op een vlak oppervlak met de breuklijn naar boven en de bolle (ronde) kant naar beneden.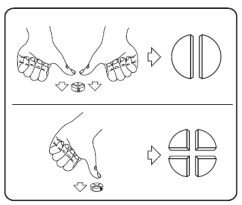
Twee gelijke delen: duw met uw duimen op beide zijden van de tablet.
Vier gelijke delen: duw met uw duim in het midden van de tablet.
4.11 Wachttijd(en)
Niet van toepassing.