- Aperçu notices
- Notice
Notice : information de l’utilisateur
Menopur Ferring 75 IU, poudre et solvant pour solution injectable
Menopur Ferring 150 IU, poudre et solvant pour solution injectable
Ménotrophine HP
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
- Gardez cette notice. Vous pourriez avoir besoin de la relire.
- Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
- Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
- Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
Que contient cette notice ?
- 1. QU’EST-CE QUE MENOPUR FERRING ET DANS QUEL CAS EST-IL UTILISÉ ?
- 2. QUELLES SONT LES INFORMATIONS À CONNAÎTRE AVANT D’UTILISER MENOPUR FERRING ?
- 3. COMMENT UTILISER MENOPUR FERRING ?
- 4. QUELS SONT LES EFFETS INDÉSIRABLES ÉVENTUELS ?
- 5. COMMENT CONSERVER MENOPUR FERRING
- 6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
1. QU’EST-CE QUE MENOPUR FERRING ET DANS QUEL CAS EST-IL UTILISÉ ?
Menopur Ferring se présente sous forme d’une poudre qui doit être mélangée avec un liquide (solvant) avant d’être utilisée. Il est administré par injection sous la peau ou dans le muscle.
Menopur Ferring contient deux hormones appelées hormone folliculostimulante (FSH) et hormone lutéinisante (LH). La FSH et la LH sont des hormones naturelles produites dans le corps des hommes et des femmes. Elles aident les organes reproducteurs à fonctionner normalement. La FSH et la LH contenues dans Menopur Ferring sont obtenues à partir de l’urine de femmes post-ménopausales. La substance active est hautement purifiée et est connue sous le nom de ménotrophine.
Menopur Ferring est utilisé pour traiter l’infertilité féminine dans les deux situations suivantes :
i. Les femmes qui ne parviennent pas à être enceintes parce que leurs ovaires ne produisent pas d’ovules (y compris le syndrome des ovaires polykystiques). Menopur Ferring est utilisé chez les femmes ayant précédemment reçu un médicament appelé citrate de clomiphène pour traiter leur infertilité, et qui n’ont pas réagi à ce traitement.
ii. Les femmes incluses dans des programmes d’assistance médicale à la procréation (AMP) (ceci inclut fécondation in vitro/transfert d’embryon (FIV/TE), transfert intratubaire de gamètes (GIFT) et injection intracytoplasmique de spermatozoïdes (ICSI)). Menopur Ferring aide les ovaires à développer de nombreux sacs d’ovules (follicules) au sein desquels un ovule peut grandir (développement folliculaire multiple).
2. QUELLES SONT LES INFORMATIONS À CONNAÎTRE AVANT D’UTILISER MENOPUR FERRING ?
Avant de commencer le traitement par Menopur Ferring, vous et votre partenaire devez être évalués par un médecin pour déterminer les causes de vos problèmes de fertilité. En particulier, vous devez être examinée pour déterminer si vous ne présentez pas une des affections suivantes, ce qui permettrait de vous donner un traitement approprié :
- une sous-activité de la thyroïde ou des glandes adrénales;
- des concentrations élevées d’une hormone appelée prolactine (hyperprolactinémie);
- des tumeurs de l’hypophyse (une glande située à la base du cerveau);
- des tumeurs de l’hypothalamus (une zone située sous la partie du cerveau appelée le thalamus).
Si vous savez que vous présentez une des affections ci-dessus, parlez-en à votre médecin avant de commencer le traitement par Menopur Ferring.
N’utilisez jamais Menopur Ferring
- si vous êtes allergique à la substance active ou à l’un des autres composants contenus dans ce médicament mentionnés dans la rubrique 6.
- si vous avez des tumeurs au niveau de l’utérus, des ovaires, du sein ou des régions du cerveau comme l’hypophyse ou l’hypothalamus.
- si vous avez des poches de liquide dans les ovaires (kystes ovariens) ou des ovaires élargis (sauf dus au syndrome des ovaires polykystiques).
- si vous présentez une malformation physique de votre utérus ou d’autres organes génitaux.
- si vous souffrez de saignements vaginaux dont la cause est inconnue.
- si vous avez des fibromes (tumeurs bénignes) au niveau de l’utérus.
- si vous êtes enceinte ou que vous allaitez.
- si vous avez eu une ménopause précoce.
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou infirmier/ère avant d’utiliser Menopur Ferring.
Parlez-en à votre médecin si vous souffrez de :
- maux de ventre;
- gonflement du ventre;
- nausées;
- vomissements;
- diarrhée;
- prise de poids;
- difficultés respiratoires;
- réduction de la production d’urine.
Parlez-en immédiatement à votre médecin, même si les symptômes se manifestent plusieurs jours après l’administration de la dernière injection. Ces symptômes peuvent indiquer un degré élevé d’activité des ovaires, susceptible de s’aggraver.
Si ces symptômes deviennent sévères, le traitement de l’infertilité doit être interrompu et vous recevrez un traitement en milieu hospitalier.
Le respect de la posologie recommandée et un contrôle rigoureux de votre traitement permettront de réduire votre risque de manifester ces symptômes.
Si vous arrêtez d’utiliser Menopur Ferring, vous pouvez encore ressentir ces symptômes.
Veuillez contacter immédiatement votre médecin si l’un de ces symptômes apparaît.
Durant le traitement avec ce médicament, normalement votre médecin programmera des échographies et parfois des examens sanguins afin de contrôler votre réponse au traitement.
Un traitement avec des hormones comme Menopur Ferring peut augmenter le risque de :
- grossesse ectopique (grossesse en dehors de l’utérus) si vous avez des antécédents de maladie des trompes de Fallope;
- fausse couche;
- grossesse multiple (des jumeaux, des triplés, etc.);
- malformations congénitales (déficiences physiques présentes chez le bébé à la naissance).
Certaines femmes traitées pour leur infertilité avec plusieurs médicaments ont développé des tumeurs dans les ovaires et d’autres organes de la reproduction. Il n’est pas établi si le traitement avec des hormones comme Menopur Ferring peut provoquer ce type de problème.
Les femmes enceintes sont plus susceptibles de développer des caillots sanguins dans les vaisseaux sanguins (veines ou artères). Le traitement de l’infertilité peut augmenter le risque que cela se produise, en particulier si vous avez une surcharge pondérale ou si vous savez que vous souffrez d’une maladie de la coagulation du sang (thrombophilie) ou si vous ou un membre de votre famille (parent de sang) avez/a déjà développé des caillots sanguins. Parlez-en à votre médecin si vous pensez être concernée par ce problème.
Enfants
Il n’y a pas d’utilisation pertinente de Menopur Ferring chez les enfants.
Autres médicaments et Menopur Ferring
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament.
Le citrate de clomiphène est un autre médicament utilisé dans le traitement de l’infertilité. Si Menopur Ferring est utilisé en association avec le citrate de clomiphène, l’effet sur les ovaires peut être accru.
Grossesse et allaitement
Menopur Ferring ne doit pas être utilisé pendant la grossesse ou l’allaitement.
Conduite de véhicules et utilisation de machines
Il est peu probable que Menopur Ferring ait d’effet sur votre aptitude à conduire des véhicules et à utiliser des machines.
Menopur Ferring contient le sodium
Menopur Ferring contient moins de 1 mmol (23 mg) de sodium par dose, c.-à-d. qu’il est essentiellement “sans sodium”.
3. COMMENT UTILISER MENOPUR FERRING ?
Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin ou pharmacien. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
i. Femmes qui n’ovulent pas (ne produisent pas d’ovules)
Le traitement doit commencer pendant les 7 premiers jours du cycle menstruel (le jour 1 correspond au premier jour de vos règles). Le traitement doit être administré chaque jour pendant au moins 7 jours.
La dose initiale recommandée est de 37 IU à 75 IU, à adapter selon votre âge, votre réserve ovarienne, votre poids corporel et votre réponse ovarienne antérieure aux gonadotrophines. Cette dose initiale est maintenue pendant au moins 7 jours.
Cette dose peut être augmentée en fonction de votre réponse au traitement (jusqu’à une dose maximale de 225 IU par jour). Chaque dose doit être administrée pendant au moins 7 jours avant d’être modifiée par votre médecin. Il est recommandé d’augmenter la dose par palier de 37,5 IU (et certainement pas plus de 75 IU par ajustement). Le cycle de traitement doit être interrompu en l’absence de réponse après 4 semaines.
Si l’on obtient une réponse adéquate, une injection unique d’une autre hormone appelée gonadotrophine chorionique humaine (hCG) doit être administrée. Une dose de 5000 IU à 10 000 IU doit être administrée un jour après la dernière injection de Menopur Ferring. Il est recommandé d’avoir des rapports sexuels le jour de l’injection de hCG, ainsi que le lendemain. À titre d’alternative, il est possible de pratiquer une insémination artificielle (injecter de sperme directement dans l’utérus). Votre médecin contrôlera scrupuleusement votre évolution pendant au moins deux semaines suivant l’injection de hCG.
Votre médecin surveillera l’effet du traitement par Menopur Ferring. En fonction de votre évolution, votre médecin peut décider d’arrêter le traitement par Menopur Ferring et de ne pas vous administrer l’injection de hCG. Dans ce cas, il/elle vous demandera d’utiliser une méthode barrière de contraception (par exemple un préservatif) ou de ne pas avoir des rapports sexuels jusqu’au début de votre prochain cycle.
ii. Femmes incluses dans des programmes d’assistance médicale à la procréation
Si vous recevez également un traitement par un agoniste de la GnRH (un médicament qui stimule le fonctionnement d’une hormone appelée Gonadotropin Releasing Hormone (GnRH)), le traitement par Menopur Ferring doit commencer environ deux semaines après le début du traitement par l’agoniste de la GnRH.
Si vous recevez également un traitement par un antagoniste de la GnRH, le traitement par Menopur Ferring doit commencer à jour 2 ou jour 3 de votre cycle menstruel (jour 1 étant le premier jour de vos règles).
Menopur Ferring doit être injecté tous les jours pendant au moins 5 jours. La dose initiale habituelle de Menopur Ferring est de 150 IU à 225 IU. Une dose initiale plus faible peut être nécessaire chez les femmes présentant un risque accru d’hyperstimulation ovarienne (par exemple les femmes atteintes du syndrome des ovaires polykystiques) ou chez les femmes de faible poids corporel.
Cette dose peut être adaptée en fonction de votre réponse au traitement jusqu’à un maximum de 450 IU par jour. La dose ne doit pas être augmentée de plus de 150 IU par ajustement. Normalement, le traitement ne doit pas se poursuivre au-delà de 20 jours.
Si vous présentez suffisamment de follicules, vous recevrez une injection unique d’un médicament appelé gonadotrophine chorionique humaine (hCG) à une dose pouvant aller jusqu’à 10 000 IU pour déclencher l’ovulation (libération d’un ovule).
Votre médecin contrôlera scrupuleusement votre évolution pendant au moins deux semaines suivant l’injection de hCG.
Votre médecin surveillera l’effet du traitement par Menopur Ferring. En fonction de votre évolution, votre médecin peut décider d’arrêter le traitement par Menopur Ferring et de ne pas vous administrer l’injection de hCG. Dans ce cas, il/elle vous demandera d’utiliser une méthode barrière de contraception (par exemple un préservatif) ou de ne pas avoir des rapports sexuels jusqu’au début de votre prochain cycle.
INSTRUCTIONS D’UTILISATION
Si à la clinique on vous a demandé de vous injecter vous-même Menopur Ferring, vous devez suivre les instructions qui vous ont été données.
La première injection de Menopur Ferring doit être administrée sous la supervision d’un médecin ou d’un/e infirmier/ère.
DISSOLUTION DE MENOPUR FERRING
Ce médicament se présente sous forme d’une poudre et doit être dissous avant utilisation. Le solvant (liquide) que vous devez utiliser pour la dissolution est fourni avec la poudre. Menopur Ferring doit être dissous juste avant son utilisation. Pour ce faire, suivez les étapes suivantes :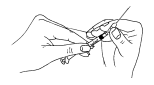
- Fixez fermement une aiguille longue et épaisse (aiguille d’aspiration/reconstitution) à la seringue.
- Cassez l’embout de l’ampoule contenant le liquide (solvant), le point étant tourné vers vous.
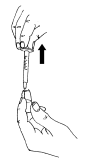 Insérez l’aiguille dans l’ampoule contenant le liquide.
Insérez l’aiguille dans l’ampoule contenant le liquide.
- Aspirez tout le liquide de l’ampoule dans la seringue.
- Insérez l’aiguille à travers le bouchon en caoutchouc du flacon contenant la poudre et injectez lentement tout le liquide dans le flacon. Visez la paroi du flacon pour éviter de former des bulles d’air.
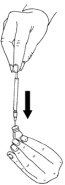
- La poudre doit se dissoudre rapidement (dans les 2 minutes) et une solution claire doit se former. Bien que cela se produise déjà normalement lorsque seulement quelques gouttes de solvant sont ajoutées, il est toujours nécessaire d’ajouter la quantité totale du solvant.
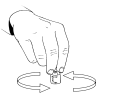 Faites tourner la solution pour faciliter la dissolution de la poudre.
Faites tourner la solution pour faciliter la dissolution de la poudre.
Ne secouez pas car cela entraînerait la formation de bulles d’air.
Si la solution n’est pas claire ou contient des particules, elle ne doit pas être utilisée.
- Aspirez à nouveau la solution dans la seringue.

Si on vous a prescrit plus d’un flacon de poudre Menopur Ferring par injection, vous pouvez aspirer à nouveau la solution (la première dilution de Menopur Ferring) dans la seringue et l’injecter dans un deuxième flacon de poudre. Vous pouvez faire cela avec jusqu’à un maximum de trois flacons de poudre au total – mais ne faites qui ce que votre médecin vous a dit.
INJECTION DE MENOPUR FERRING
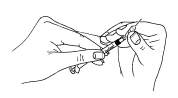 Une fois que vous avez aspiré la dose prescrite dans la seringue, remplacez l’aiguille par une aiguille courte et mince (aiguille d’injection).
Une fois que vous avez aspiré la dose prescrite dans la seringue, remplacez l’aiguille par une aiguille courte et mince (aiguille d’injection).- Tournez la seringue avec l’aiguille vers le haut et tapotez doucement afin que toutes les bulles d’air s’accumulent dans l’embout. Enfoncez le piston soigneusement jusqu’à ce que la première goutte de liquide sorte.
- Votre médecin ou votre infirmier/ère vous indiquera le site où faire l’injection (par exemple l’avant de la cuisse, dans l’abdomen, etc.).
- Désinfectez le site d’injection.
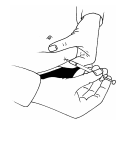
- Pour l’injection, pincez votre peau pour produire un pli et insérez l’aiguille dans le pli en un mouvement rapide à un angle de 90 degrés par rapport au corps. Enfoncez le piston pour injecter la solution, puis retirez l’aiguille.
- Après avoir retiré la seringue, exercez une pression sur le site d’injection pour arrêter tout saignement. Masser légèrement le site d’injection aidera à disperser la solution sous la peau.
- Ne jetez pas le matériel utilisé avec les ordures ménagères. Il convient de l’éliminer de manière appropriée.
Si vous avez utilisé plus de Menopur Ferring que vous n’auriez dû
Si vous avez utilisé trop de Menopur Ferring, prenez immédiatement contact avec votre médecin, votre pharmacien ou le centre Antipoison (070/245.245).
Si vous oubliez d’utiliser Menopur Ferring
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Parlez-en à un/e infirmier/ère ou un médecin.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, votre pharmacien ou votre infirmier/ère.
4. QUELS SONT LES EFFETS INDÉSIRABLES ÉVENTUELS ?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
L’utilisation d’hormones pour traiter l’infertilité, comme Menopur Ferring, peut provoquer un degré élevé d’activité au niveau des ovaires et une affection appelée syndrome d’hyperstimulation ovarienne (SHO), en particulier chez les femmes ayant des ovaires polykystiques. Les symptômes comprennent : maux de ventre, gonflement du ventre, nausées, vomissements, diarrhée et prise de poids. En cas de SHO sévère, une accumulation de liquide dans l’abdomen, le bassin et/ou la cage thoracique, une difficulté respiratoire, une réduction de la production d’urine, la formation de caillots sanguins dans les vaisseaux sanguins (thromboembolie) et une torsion des ovaires (torsion ovarienne) ont été rapportées comme des complications rares.
Si vous ressentez l’un de ces symptômes, contactez immédiatement votre médecin, même s’ils se manifestent quelques jours après la dernière injection.
Des réactions allergiques (hypersensibilité) peuvent survenir lors de l’utilisation de Menopur Ferring. Les symptômes de telles réactions peuvent comprendre : éruption cutanée, démangeaisons, gonflement de la gorge et des difficultés respiratoires. Si vous ressentez l’un de ces symptômes, contactez immédiatement votre médecin.
Les effets indésirables fréquents suivants apparaissent chez 1 à 10 patientes sur 100 traitées :
- maux de ventre;
- maux de tête;
- nausées;
- gonflement du ventre;
- douleurs pelviennes;
- hyperstimulation des ovaires entraînant un degré élevé d’activité (syndrome d’hyperstimulation ovarienne);
- réactions locales au site d’injection (telles que douleurs, rougeur, bleus, gonflement et/ou démangeaisons).
Les effets indésirables peu fréquents suivants apparaissent chez 1 à 10 patientes sur 1000 traitées :
- vomissements;
- gêne abdominale;
- diarrhée;
- fatigue;
- étourdissements;
- poches de liquide dans les ovaires (kystes ovariens);
- troubles au niveau des seins (y compris douleurs, sensibilité et gêne des seins, douleurs du mamelon et gonflement des seins);
- bouffées de chaleur.
Les effets indésirables rares suivants apparaissent chez 1 à 10 patientes sur 10 000 traitées :
- acné;
- éruption cutanée.
En plus des effets indésirables mentionnés ci-dessus, les effets indésirables suivants ont été observés après la commercialisation de Menopur Ferring et leur fréquence est inconnue :
- troubles de la vue;
- fièvre;
- se sentir malade;
- réactions allergiques;
- prise de poids;
- douleurs au niveau des muscles et des articulations (par exemple, douleurs du dos, douleurs dans la nuque et douleurs dans les bras et les jambes);
- torsion des ovaires (torsion ovarienne) en tant que complication d’un degré élevé d’activité des ovaires en raison d’une hyperstimulation;
- démangeaisons;
- urticaire;
- caillots sanguins en tant que complication d’un degré élevé d’activité des ovaires en raison d’une hyperstimulation.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via :
Belgique
Agence fédérale des médicaments et des produits de santé (www.afmps.be)
Division Vigilance :
Site internet : www.notifieruneffetindesirable.be
E-mail : adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy ou Division de la Pharmacie et des Médicaments de la Direction de la Santé
Site internet : www.guichet.lu/pharmacovigilance
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER MENOPUR FERRING
Tenir hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage après EXP. La date de péremption fait référence au dernier jour de ce mois.
À conserver à une température ne dépassant pas 25°C. Ne pas congeler. À conserver dans l’emballage d’origine, à l’abri de la lumière.
Pour une utilisation immédiate et unique après reconstitution.
Ne jetez aucun médicament au tout-à-l’égout ni avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient Menopur Ferring
Menopur Ferring 75 IU
La substance active est la ménotrophine hautement purifiée (gonadotrophine ménopausique humaine, hMG), correspondant à 75 IU d’activité d’hormone folliculostimulante (FSH) et 75 IU d’activité d’hormone lutéinisante (LH).
Les autres composants de la poudre sont :
- lactose monohydraté
- polysorbate 20
- hydroxyde de sodium
- acide chlorhydrique dilué
Les autres composants du solvant sont :
- eau pour préparations injectables
- chlorure de sodium
- acide chlorhydrique dilué
Menopur Ferring 150 IU
La substance active est la ménotrophine hautement purifiée (gonadotrophine ménopausique humaine, hMG), correspondant à 150 IU d’activité d’hormone folliculostimulante (FSH) et 150 IU d’activité d’hormone lutéinisante (LH).
Les autres composants de la poudre sont :
- lactose monohydraté
- polysorbate 20
- hydroxyde de sodium
- acide chlorhydrique dilué
Les autres composants du solvant sont :
- eau pour préparations injectables
- chlorure de sodium
- acide chlorhydrique dilué
Aspect de Menopur Ferring et contenu de l’emballage extérieur
Menopur Ferring se compose d’une poudre et d’un solvant pour solution injectable.
L’emballage contient cinq ou dix flacons en verre transparent contenant une poudre blanche à blanc cassé. L’emballage contient aussi un nombre égal d’ampoules en verre transparent contenant un solvant incolore.
Titulaire de l’autorisation de mise sur le marché et fabricant
Titulaire de l’autorisation de mise sur le marché
Ferring N.V., The Crescent Business Center
Lenniksebaan 451, B-1070 Anderlecht
Tél. : +32 (0)53 / 72 92 00
ferringnvsa@ferring.be
Fabricant
Ferring GmbH, Wittland 11, D-24109 Kiel, Allemagne
Numéro de l’autorisation de mise sur le marché
Belgique
Menopur Ferring 75 IU : BE197504
Menopur Ferring 150 IU : BE430762
Luxembourg
Menopur Ferring 75 IU: 2002090043
Menopur Ferring 150 IU: 2013060193
Mode de délivrance
Médicament soumis à prescription médicale.
La dernière date à laquelle cette notice a été approuvée est 12/2024.
PRIX
| Code CNK | Emballage | Prix | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|
| 1585769 | MENOPUR FERRING PULV+SOLV IM/SC 10 | € 194,66 | Oui | - | - |