Notice : Information de l’utilisateur
STELARA 90 mg solution injectable en stylo prérempli
ustekinumab
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
Cette notice a été écrite pour la personne prenant le médicament.
- Gardez cette notice. Vous pourriez avoir besoin de la relire.
- Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
- Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
- Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
Que contient cette notice ?
1. QU’EST-CE QUE STELARA ET DANS QUEL CAS EST-IL UTILISÉ ?
Qu’est-ce que Stelara
Stelara contient une substance active qui s’appelle ustekinumab, un anticorps monoclonal. Les anticorps monoclonaux sont des protéines qui reconnaissent et se lient spécifiquement à certaines protéines dans le corps.
Stelara appartient à un groupe de médicaments appelés « immunosuppresseurs ». Ces médicaments agissent en affaiblissant partiellement le système immunitaire.
Dans quel cas Stelara est-il utilisé
Stelara administré à l’aide du stylo prérempli est utilisé pour le traitement des maladies inflammatoires suivantes :
- Psoriasis en plaques (chez les adultes)
- Rhumatisme psoriasique (chez les adultes)
- Maladie de Crohn modérée à sévère (chez les adultes)
- Rectocolite hémorragique modérée à sévère (chez les adultes)
Psoriasis en plaques
Le psoriasis en plaques est une maladie de la peau qui provoque une inflammation affectant la peau et les ongles. Stelara réduira l’inflammation ainsi que d’autres signes de la maladie.
Stelara administré à l’aide du stylo prérempli est utilisé chez les patients adultes souffrant de psoriasis en plaques modéré à sévère, qui ne peuvent pas utiliser la ciclosporine, le méthotrexate ou la photothérapie, ou lorsque ces traitements n’ont pas été efficaces.
Rhumatisme psoriasique
Le rhumatisme psoriasique est une maladie inflammatoire des articulations, habituellement associée à du psoriasis. Si vous avez un rhumatisme psoriasique actif, vous recevrez d’abord d’autres médicaments. Si vous ne répondez pas suffisamment bien à ces médicaments, vous pourrez recevoir Stelara afin de :
- Réduire les signes et symptômes de votre maladie.
- Améliorer votre état physique.
- Ralentir les atteintes de vos articulations.
Maladie de Crohn
La maladie de Crohn est une maladie inflammatoire des intestins. Si vous êtes atteint de la maladie de Crohn, vous recevrez d’abord d’autres médicaments. Si vous ne répondez pas suffisamment bien à ces médicaments ou que vous y êtes intolérants, Stelara pourra vous être administré afin de réduire les signes et les symptômes de votre maladie.
Rectocolite hémorragique
La rectocolite hémorragique est une maladie inflammatoire des intestins. Si vous êtes atteint de rectocolite hémorragique, vous recevrez d’abord d’autres médicaments. Si vous ne répondez pas suffisamment bien à ces médicaments ou que vous y êtes intolérant, Stelara pourra vous être administré afin de réduire les signes et les symptômes de votre maladie.
2. QUELLES SONT LES INFORMATIONS À CONNAÎTRE AVANT D’UTILISER STELARA ?
N’utilisez jamais Stelara
- Si vous êtes allergique à l’ustekinumab ou à l’un des autres composants contenus dans ce médicament (mentionnés dans la rubrique 6)
- Si vous avez une infection évolutive que votre médecin considère importante.
Si vous n’êtes pas sûr que l’une des situations ci-dessus s’applique à vous, parlez-en avec votre médecin ou pharmacien avant d’utiliser Stelara.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant d’utiliser Stelara. Votre médecin va vérifier votre état de santé avant chaque traitement. Assurez-vous d’informer votre médecin de toutes les maladies dont vous souffrez avant chaque traitement. Informez également votre médecin si vous avez été récemment à proximité de quelqu’un qui pourrait avoir la tuberculose. Votre médecin vous examinera et fera un test pour la tuberculose avant que vous preniez Stelara. Si votre médecin pense que vous êtes à risque pour la tuberculose, vous pourrez recevoir des médicaments pour la traiter.
Faites attention aux effets indésirables graves :
Stelara peut provoquer des effets indésirables graves, incluant des réactions allergiques et des infections. Vous devez faire attention à certains signes de maladie pendant que vous prenez Stelara. Consultez le paragraphe « Effets indésirables graves » dans la rubrique 4 pour une liste complète de ces effets indésirables.
Avant d’utiliser Stelara, informez votre médecin :
- Si vous avez déjà eu une réaction allergique à Stelara. Si vous n’êtes pas sûr, demandez à votre médecin.
- Si vous avez déjà eu un cancer quel qu’en soit le type – car les immunosuppresseurs comme Stelara affaiblissent partiellement le système immunitaire. Ceci peut augmenter le risque de cancer.
- Si vous avez été traité pour un psoriasis avec d’autres médicaments biologiques (un médicament produit à partir d’une source biologique et habituellement administré par injection) – le risque de cancer peut être plus élevé.
- Si vous avez ou avez récemment eu une infection.
- Si vous avez de nouvelles lésions ou des lésions qui évoluent sur les zones de psoriasis ou sur la peau saine.
- Si vous avez déjà eu une réaction allergique au latex ou à une injection de Stelara – le conditionnement de ce médicament contient du latex ce qui peut provoquer des réactions allergiques sévères chez les personnes qui sont sensibles au latex. Consultez le paragraphe « Effets indésirables graves » dans la rubrique 4 pour les signes d’une réaction allergique.
- Si vous prenez d’autres traitements pour le psoriasis et/ou le rhumatisme psoriasique – tels qu’un autre immunosuppresseur ou une photothérapie (quand votre corps est traité avec un type de lumière ultra-violet (UV)). Ces traitements peuvent également affaiblir partiellement le système immunitaire. L’utilisation simultanée de ces traitements avec Stelara n’a pas été étudiée. Cependant, il est possible que cela augmente le risque de maladies liées à un système immunitaire plus faible.
- Si vous recevez ou avez déjà reçu des injections pour traiter les allergies – on ne sait pas si Stelara peut les affecter.
- Si vous avez 65 ans ou plus – vous pouvez être plus sujet aux infections.
Si vous n’êtes pas sûr que l’une des situations ci-dessus s’applique à vous, parlez-en avec votre médecin ou pharmacien avant d’utiliser Stelara.
Certains patients ont présenté des réactions de type lupus, notamment un lupus cutané ou un syndrome de type lupus, au cours du traitement par ustekinumab. Consultez immédiatement un médecin si vous développez une éruption cutanée rouge, en relief, squameuse, comportant parfois une bordure plus foncée, sur les zones de peau exposées au soleil ou associée à des douleurs articulaires.
Crise cardiaque et accident vasculaire cérébral (AVC)
Des crises cardiaques et des AVC ont été observés dans une étude chez des patients atteints de psoriasis traités par Stelara. Votre médecin vérifiera régulièrement vos facteurs de risque de maladie cardiaque et d’AVC afin de s’assurer qu’ils sont traités de manière adéquate. Consultez immédiatement un médecin si vous développez des douleurs thoraciques, une faiblesse ou des sensations anormales d’un côté de votre corps, un affaissement du visage ou des anomalies de la parole ou de la vue.
Enfants et adolescents
L’utilisation du stylo prérempli de Stelara n’est pas recommandée chez les enfants et les adolescents âgés de moins de 18 ans atteints de psoriasis ou de la maladie de Crohn car il n’a pas été étudié dans cette tranche d’âge. Il convient d’utiliser plutôt la seringue préremplie ou le flacon chez les enfants âgés de 6 ans et plus et les adolescents atteints de psoriasis. Il convient plutôt d’utiliser la solution pour perfusion, le flacon ou la seringue préremplis pour les enfants âgés de 2 ans et plus atteints de la maladie de Crohn.
Stelara n’est pas recommandé chez les enfants et les adolescents âgés de moins de 18 ans atteints de rhumatisme psoriasique ou de rectocolite hémorragique ou chez les enfants atteints de la maladie de Crohn âgés de moins de 2 ans car il n’a pas été étudié dans ces tranches d’âge.
Autres médicaments, vaccins et Stelara
Informez votre médecin ou pharmacien :
- Si vous prenez, avez pris récemment ou pourriez prendre tout autre médicament.
- Si vous vous êtes récemment fait ou allez vous faire vacciner. Certains types de vaccins (vaccins vivants) ne doivent pas être administrés pendant l’utilisation de Stelara.
- Si vous avez reçu Stelara pendant votre grossesse, informez le médecin s’occupant de votre bébé de votre traitement par Stelara avant que votre bébé ne reçoive un vaccin quel qu’il soit, notamment les vaccins vivants, tels que le vaccin BCG (utilisé pour prévenir la tuberculose). Les vaccins vivants ne sont pas recommandés pour votre bébé au cours des douze premiers mois après la naissance si vous avez reçu Stelara pendant la grossesse, à moins que le médecin de votre bébé ne recommande le contraire.
Grossesse et allaitement
- Si vous êtes enceinte, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin avant de prendre ce médicament.
- Il n’a pas été observé de risque accru de malformations congénitales chez les bébés exposés à Stelara in utero. Cependant, l’expérience clinique avec Stelara chez les femmes enceintes est limitée. Il est ainsi préférable d’éviter l’utilisation de Stelara en cas de grossesse.
- Si vous êtes une femme en âge de procréer, vous devez éviter de tomber enceinte et vous devez prendre une contraception adaptée pendant toute l’utilisation de Stelara et jusqu’à 15 semaines au moins après le dernier traitement par Stelara.
- Stelara peut traverser la barrière placentaire et passer chez le bébé à naître. Si vous avez reçu Stelara au cours de votre grossesse, votre bébé peut présenter un risque plus élevé de contracter une infection.
- Si vous avez reçu Stelara pendant votre grossesse, il est important que vous informiez les médecins et les autres professionnels de santé s’occupant de votre bébé avant qu’il ne recoive un vaccin quel qu’il soit. Les vaccins vivants, tels que le vaccin BCG (utilisé pour prévenir la tuberculose), ne sont pas recommandés pour votre bébé au cours des douze premiers mois après la naissance si vous avez reçu Stelara pendant la grossesse, à moins que le médecin de votre bébé ne recommande le contraire.
- L’ustekinumab peut passer en très faible quantité dans le lait maternel. Si vous allaitez ou pensez allaiter, demandez conseil à votre médecin. Vous devez décider avec lui si vous devez plutôt allaiter ou utiliser Stelara. Ne faites pas les deux.
Conduite de véhicules et utilisation de machines
Stelara n’a aucun effet ou qu’un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines.
Stelara contient du polysorbate 80
Stelara contient 0,04 mg de polysorbate 80 (E433) par dose équivalent à 0,04 mg/mL. Les polysorbates peuvent provoquer des réactions allergiques. Informez votre médecin si vous avez déjà présenté une allergie.
3. COMMENT UTILISER STELARA ?
Stelara doit être utilisé sous la responsabilité et la surveillance d’un médecin expérimenté dans le diagnostic et le traitement des maladies pour lesquelles Stelara est destiné.
Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin. Vérifiez auprès de votre médecin en cas de doute. Parlez avec votre médecin afin de savoir quand vous recevrez vos injections et quand vous aurez vos rendez-vous de suivi.
Quelle quantité de Stelara est administrée ?
Votre médecin déterminera la quantité de Stelara dont vous avez besoin et la durée du traitement.
Adultes âgés de 18 ans et plus
Psoriasis ou Rhumatisme psoriasique
- La dose initiale recommandée est 45 mg de Stelara. Pour les patients pesant plus de 100 kilogrammes (kg), la dose initiale est de 90 mg au lieu de 45 mg.
- Après la dose initiale, vous recevrez la dose suivante 4 semaines après, puis ensuite toutes les 12 semaines. Les doses suivantes sont en général les mêmes que la dose initiale.
Maladie de Crohn ou rectocolite hémorragique
- Pendant le traitement, la première dose d'environ 6 mg/kg de Stelara sera administrée par votre médecin à l’aide d’une perfusion dans une veine de votre bras (perfusion intraveineuse). Après la dose initiale, vous recevrez la dose suivante de 90 mg de Stelara par une injection sous la peau (« sous-cutanée ») après 8 semaines, puis toutes les 12 semaines par la suite.
- Chez certains patients, après la première injection sous la peau, Stelara 90 mg peut être administré toutes les 8 semaines. Votre médecin décidera quand vous devez recevoir votre prochaine dose.
Comment Stelara est administré
- Stelara est administré par injection sous la peau (« sous-cutanée »). Au début de votre traitement, le personnel médical ou une infirmière pourra réaliser l’injection de Stelara.
- Cependant, vous et votre médecin pouvez décider que vous réaliserez vous-même vos injections de Stelara. Dans ce cas vous recevrez une formation qui vous apprendra comment vous injecter Stelara vous-même.
- Pour les instructions sur comment injecter Stelara, consultez la rubrique « Instructions d’utilisation » à la fin de cette notice.
Parlez à votre médecin de toute question sur l’auto-injection de Stelara.
Si vous avez utilisé plus de Stelara que vous n’auriez dû
Si vous avez utilisé plus de Stelara ou si vous en avez trop reçu, parlez-en immédiatement à un médecin ou un pharmacien. Gardez toujours sur vous l’emballage extérieur, même s’il est vide.
Si vous oubliez d’utiliser Stelara
Si vous oubliez une dose, contactez votre médecin ou pharmacien. Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez d’utiliser Stelara
Il n’est pas dangereux d’arrêter d’utiliser Stelara. Cependant, si vous arrêtez, vos symptômes peuvent revenir.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDÉSIRABLES ÉVENTUELS ?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
Effets indésirables graves
Certains patients peuvent avoir des effets indésirables graves qui peuvent nécessiter un traitement urgent.
Réactions allergiques – elles peuvent nécessiter un traitement urgent. Informez votre médecin ou cherchez immédiatement une aide médicale d’urgence si vous constatez l’un des signes suivants.
- Les réactions allergiques graves (anaphylaxie) sont rares chez les personnes prenant Stelara (peuvent affecter jusqu’à 1 personne sur 1 000). Les signes incluent :
- difficultés à respirer ou à avaler
- pression sanguine basse, ce qui peut provoquer des vertiges et des légers étourdissements
- gonflement de la face, des lèvres, de la bouche ou de la gorge.
- Les signes fréquents d’une réaction allergique incluent éruptions cutanées et urticaire (ils peuvent affecter jusqu’à 1 personne sur 100).
Dans de rares cas, des réactions allergiques pulmonaires et une inflammation pulmonaire ont été signalées chez des patients traités par ustekinumab. Informez immédiatement votre médecin si vous présentez des symptômes comme la toux, l’essoufflement et la fièvre.
Si vous avez une réaction allergique grave, votre médecin peut décider que vous ne devez plus utiliser Stelara.
Infections - elles peuvent nécessiter un traitement urgent. Informez votre médecin immédiatement si vous constatez l’un des signes suivants.
- Les infections du nez ou de la gorge et les rhumes sont fréquents (peuvent affecter jusqu’à 1 personne sur 10)
- Les infections thoraciques sont peu fréquentes (peuvent affecter jusqu’à 1 personne sur 100)
- L’inflammation des tissus sous la peau (cellulite) est peu fréquente (peut affecter jusqu’à 1 personne sur 100)
- Les zona (un type d’éruption cutanée douloureuse avec des cloques) sont peu fréquents (peuvent affecter jusqu’à 1 personne sur 100)
Stelara peut altérer votre capacité à lutter contre les infections. Certaines infections peuvent devenir graves et peuvent comprendre des infections d’origine virale, fongique, bactérienne (notamment la tuberculose), ou parasitaire, y compris des infections survenant principalement chez les personnes présentant un système immunitaire plus faible (infections opportunistes). Des infections opportunistes du cerveau (encéphalite, méningite), des poumons et des yeux ont été rapportées chez des patients recevant un traitement par ustekinumab.
Vous devez faire attention aux signes d’infection pendant que vous utilisez Stelara. Ceux-ci incluent :
- Fièvre, symptômes pseudo-grippaux, sueurs nocturnes, perte de poids
- Sensation de fatigue ou d’essoufflement ; toux qui ne passe pas
- Peau chaude, rouge et douloureuse, ou une éruption cutanée douloureuse avec des cloques
- Sensation de brûlure lorsque vous urinez
- Diarrhées
- Troubles visuels ou perte de la vue
- Maux de tête, raideur de la nuque, sensibilité à la lumière, nausées ou confusion.
Informez votre médecin immédiatement si vous constatez l’un de ces signes d’infection. Ils peuvent être des signes d’infections telles que des infections thoraciques, des infections de la peau, un zona ou des infections opportunistes, qui pourraient conduire à des complications graves. Informez votre médecin si vous avez une infection qui ne passe pas ou qui revient. Votre médecin peut décider que vous ne devez plus utiliser Stelara jusqu’à ce que l’infection soit partie. Informez également votre médecin si vous avez des coupures ou des plaies ouvertes car elles pourraient s’infecter.
Desquamation de la peau – l’augmentation de la rougeur et de la desquamation de la peau sur une surface corporelle plus étendue peuvent être des symptômes de psoriasis érythrodermique ou d’érythrodermie, qui sont des atteintes graves de la peau. Vous devez informer immédiatement votre médecin si vous remarquez un de ces signes.
Autres effets indésirables
Effets indésirables fréquents (peuvent affecter jusqu’à 1 personne sur 10):
- Diarrhées
- Nausées
- Vomissements
- Sensations de fatigue
- Vertiges
- Mal de tête
- Démangeaisons (prurit)
- Douleurs du dos, des muscles ou des articulations
- Mal de gorge
- Rougeur et douleur au site d’injection
- Infection des sinus
Effets indésirables peu fréquents (peuvent affecter jusqu’à 1 personne sur 100):
- Infections dentaires
- Infection mycotique vaginale
- Dépression
- Nez bouché ou congestionné
- Saignement, ecchymose (bleu), induration, gonflement et démangeaisons au site d’injection
- Sensation de faiblesse
- Paupière tombante et muscles affaissés sur un côté du visage (« paralysie faciale » ou « paralysie dite de Bell »), ce qui est généralement temporaire
- Un changement de l’aspect du psoriasis avec rougeur et apparition de petites vésicules jaunes ou blanches, parfois accompagnées de fièvre (psoriasis pustuleux).
- Peau qui pèle (desquamation de la peau)
- Acné
Effets indésirables rares (peuvent affecter jusqu’à 1 personne sur 1 000):
- Rougeur et desquamation de la peau sur une surface corporelle plus étendue, qui peut démanger ou être douloureuse (érythrodermie). Des symptômes semblables se développent parfois dans le cadre de l’évolution naturelle de la maladie (psoriasis érythrodermique).
- Inflammation des petits vaisseaux sanguins, pouvant entraîner une éruption cutanée accompagnée de petits boutons rouges ou violets, de la fièvre ou des douleurs articulaires (vascularite)
Effets indésirables très rares (peuvent affecter jusqu’à 1 personne sur 10 000) :
- Formation de cloques sur la peau, potentiellement accompagnées d’une rougeur, de démangeaisons et de douleurs (pemphigoïde bulleuse).
- Lupus cutané ou syndrome de type lupus (éruption cutanée rouge, en relief, squameuse sur les zones de peau exposées au soleil, éventuellement associée à des douleurs articulaires).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via :
Belgique
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance
Site internet : www.notifieruneffetindesirable.be
E-mail : adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER STELARA
- Tenir ce médicament hors de la vue et de la portée des enfants.
- A conserver au réfrigérateur (entre 2°C et 8°C). Ne pas congeler.
- Conserver le stylo prérempli dans l’emballage extérieur à l’abri de la lumière.
- Si nécessaire, les stylos préremplis individuels peuvent aussi être conservés à température ambiante jusqu’à 30°C pendant une période unique de 30 jours maximum dans le carton d’origine à l’abri de la lumière. Inscrire la date à laquelle le stylo prérempli est retiré du réfrigérateur pour la première fois et la date à laquelle il ne doit plus être utilisé dans l’espace prévu à cet effet sur le carton. La date à laquelle le stylo prérempli ne doit plus être utilisé ne doit pas dépasser la date de péremption initiale imprimée sur le carton. Une fois qu’un stylo prérempli a été conservé à température ambiante (jusqu’à 30 °C), il ne doit pas être remis au réfrigérateur. Jeter le stylo prérempli s’il n’est pas utilisé dans les 30 jours suivant sa conservation à température ambiante ou à la date de péremption initiale, si celle-ci est antérieure.
- Ne pas agiter les stylos préremplis. Une agitation prolongée et vigoureuse peut endommager le médicament.
N’utilisez pas ce médicament
- Après la date de péremption indiquée sur l’emballage après “EXP”. La date de péremption fait référence au dernier jour de ce mois.
- Si vous remarquez que le liquide est décoloré, laiteux ou si vous voyez des particules étrangères qui flottent (voir rubrique 6 « Comment se présente Stelara et contenu de l’emballage extérieur »).
- Si vous savez ou pensez que le produit a pu être exposé à des températures extrêmes (telles qu’une congélation ou un réchauffement accidentel).
- Si le produit a été vigoureusement agité.
Stelara est à usage unique. Tout produit inutilisé restant dans le stylo prérempli doit être jeté. Ne jetez aucun médicament au tout à l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient Stelara
- La substance active est l’ustekinumab. Chaque stylo prérempli contient 90 mg d’ustekinumab dans 1 mL.
- Les autres composants sont : L-histidine, monochlorhydrate monohydraté de L-histidine, polysorbate 80 (E433), saccharose et eau pour préparations injectables.
Comment se présente Stelara et contenu de l’emballage extérieur
Stelara est une solution injectable limpide à légèrement opalescente (ayant un aspect nacré), incolore à jaune clair. La solution peut contenir quelques petites particules protéiques translucides ou blanches. Elle est fournie dans un emballage cartonné contenant un stylo prérempli unidose en verre de 1 mL. Chaque stylo prérempli contient 90 mg d’ustekinumab dans 1 mL de solution injectable.
Titulaire de l’Autorisation de mise sur le marché
Janssen-Cilag International NV
Turnhoutseweg 30
B‑2340 Beerse
Belgique
Fabricant
Janssen Biologics B.V.
Einsteinweg 101
2333 CB Leiden
Pays Bas
Pour toute information complémentaire concernant ce médicament, veuillez prendre contact avec le représentant local du titulaire de l’autorisation de mise sur le marché :
België/Belgique/Belgien
Janssen-Cilag NV
Tel/Tél: 0800 93 377
info_belux@its.jnj.com
Luxembourg/Luxemburg
Janssen-Cilag NV
Tél/Tel: 800 29 504
info_belux@its.jnj.com
Nederland
Janssen-Cilag B.V.
Tel: 0800 242 42 42
info_nl@its.jnj.com
La dernière date à laquelle cette notice a été révisée est avril 2026.
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’Agence européenne des médicaments https://www.ema.europa.eu.
Instructions d’utilisation
Stelara
(ustekinumab)
injection par voie sous-cutanée
Stylo prérempli
Ces « Instructions d’utilisation » contiennent des informations sur la manière d’injecter Stelara.
Important
Stelara est fourni en stylo prérempli unidose contenant une dose de 45 mg ou une dose de 90 mg.
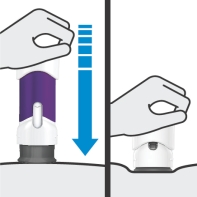
Pendant l’injection, poussez la poignée à fond vers le bas jusqu’à ce que le corps violet ne soit plus visible afin d’injecter la dose complète. NE SOULEVEZ PAS LE STYLO PRÉREMPLI pendant l’injection ! Si vous le soulevez, le stylo prérempli se verrouillera et vous ne recevrez pas la dose complète.
Si votre médecin décide que vous ou un aidant pouvez être en mesure d’administrer vos injections de Stelara à domicile, vous devez suivre une formation sur la manière appropriée de préparer et d’injecter Stelara avec le stylo prérempli. N’essayez pas de vous injecter le médicament avant d’avoir été formé par votre médecin.
Chaque stylo prérempli ne peut être utilisé qu’une seule fois. Jetez-le (voir Étape 3) après utilisation même s’il reste du médicament à l’intérieur.
Ne réutilisez pas le stylo prérempli.
Lisez ces Instructions d’utilisation avant d’utiliser le stylo prérempli de Stelara et chaque fois que vous recevez un nouveau stylo prérempli. De nouvelles informations peuvent avoir été ajoutées. Cette notice ne remplace pas une discussion avec votre médecin sur votre état de santé ou votre traitement.
Si vous ne pouvez pas vous administrer vous-même l’injection :
- demandez à votre médecin ou infirmier/ère de vous aider, ou
- demandez à une personne formée par un médecin ou un/une infirmier/ère de vous administrer vos injections.
Pour réduire le risque de piqûres d’aiguille accidentelles, chaque stylo prérempli comporte un protège aiguille qui recouvre automatiquement l’aiguille et se verrouille après l’administration de votre injection, lorsque l’injecteur est soulevé. Ne soulevez pas le stylo prérempli pendant l’injection tant que l’injection n’est pas terminée.
Le capuchon de l’aiguille à l’intérieur du capuchon inférieur du stylo prérempli contient du latex. Ne manipulez pas le capuchon de l’aiguille si vous êtes allergique au latex.
Veuillez également lire attentivement la notice avant de commencer votre injection et posez toutes vos questions à votre médecin ou infirmier/ère.
![]() Informations sur la conservation
Informations sur la conservation
À conserver au réfrigérateur entre 2 °C et 8 °C. Si nécessaire, conserver à une température ambiante ne dépassant pas 30 °C pendant une durée maximale de 30 jours dans l’emballage d’origine. Ne remettez pas au réfrigérateur après avoir conservé le médicament à température ambiante.
Ne pas congeler le stylo prérempli.
Conservez le stylo prérempli et tous les médicaments hors de portée des enfants.
N’agitez pas le stylo prérempli. L’agitation peut altérer le médicament Stelara. N’utilisez pas le stylo prérempli s’il a été agité. Prenez un nouveau stylo prérempli.
Conservez le stylo prérempli dans l’emballage d’origine à l’abri de la lumière et des dégradations.
![]() Besoin d’aide ?
Besoin d’aide ?
Si vous avez la moindre question, contactez votre médecin pour en parler. Pour obtenir une assistance supplémentaire ou faire part de vos commentaires, reportez-vous à la notice pour connaître les coordonnées de votre représentant local. 

![]()
![]()
![]()

![]()


![]()



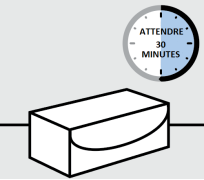
Réunissez le ou les emballages
S’ils sont réfrigérés, sortez le ou les emballages de stylo prérempli du réfrigérateur et placez-les sur une surface plane.
Laissez à température ambiante pendant au moins 30 minutes avant utilisation.
Ne réchauffez pas d’une autre manière.
Si votre dose est de 45 mg, vous recevrez un stylo prérempli de 45 mg.
Si votre dose est de 90 mg, vous recevrez un stylo prérempli de 90 mg ou deux stylos préremplis de 45 mg. Si vous recevez deux stylos préremplis de 45 mg, suivez les Étapes 1 à 3 pour les deux injections.
Choisissez un site d’injection différent pour la deuxième injection.
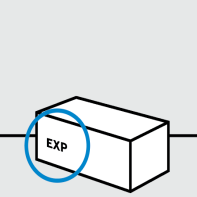
Vérifiez la date de péremption (« EXP ») et les dispositifs d’inviolabilité sur l’emballage
N’utilisez pas le stylo prérempli si les dispositifs d’inviolabilité sur l’emballage ont été rompus ou si la date de péremption est dépassée.
N’utilisez pas le stylo prérempli s’il a été conservé à température ambiante pendant plus de 30 jours ou s’il a été conservé à une température dépassant 30 °C. Contactez votre médecin ou pharmacien pour obtenir un nouveau stylo prérempli.
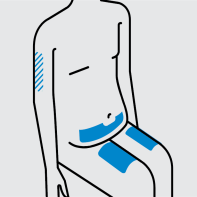
Choisissez le site d’injection
Choisissez l’une des zones suivantes pour votre injection:
- Dessus des cuisses
- Bas du ventre (de l’abdomen), sauf une zone de 5 centimètres autour du nombril
Si une autre personne réalise l’injection, elle peut également utiliser :
- Arrière du haut du bras
N’injectez pas au niveau d’une peau sensible, présentant un bleu, une peau rouge ou dure.
Utilisez un site d’injection différent à chaque injection.
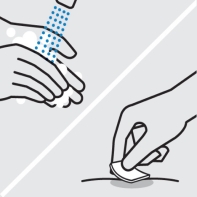
Lavez-vous les mains
Lavez-vous bien les mains au savon et à l’eau chaude.
Nettoyez le site d’injection
Essuyez le site d’injection choisi avec un tampon imbibé d’alcool et laissez-le sécher.
Ne touchez pas, ne ventilez pas et ne soufflez pas sur le site d’injection après l’avoir nettoyé.
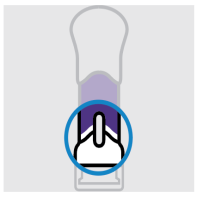
Inspectez le liquide dans la fenêtre
Choisissez une surface de travail bien éclairée, propre et plane.
Sortez le stylo prérempli de l’emballage et vérifiez l’absence de dégradations.
Vérifiez le liquide dans la fenêtre de visualisation. Il doit être limpide à légèrement opalescent et incolore à jaune clair et peut contenir des minuscules particules blanches ou translucides et une ou plusieurs bulles d’air. Ceci est normal.
N’injectez pas si le liquide est congelé, trouble, s’il a changé de couleur ou contient des particules de grande taille. Contactez votre médecin ou pharmacien pour obtenir un nouveau stylo prérempli.
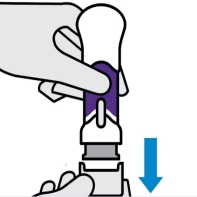
Retirez le capuchon inférieur
Maintenez les mains à l’écart du protège aiguille une fois le capuchon retiré. Il est normal d’observer quelques gouttes de liquide.
Injectez Stelara dans les 5 minutes qui suivent le retrait du capuchon.
Ne remettez pas le capuchon. Cela pourrait endommager l’aiguille.
N’utilisez pas le stylo prérempli s’il est tombé après avoir retiré le capuchon. Contactez votre médecin ou pharmacien pour obtenir un nouveau stylo prérempli.
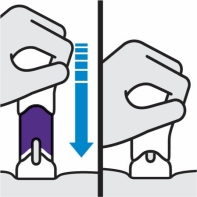
Placez le stylo droit contre la peau. Poussez la poignée à fond vers le bas jusqu’à ce que le corps violet ne soit plus visible.
NE SOULEVEZ PAS LE STYLO PRÉREMPLI pendant l’injection !
Si vous le soulevez, le protège aiguille se verrouillera en affichant une bande jaune et vous n’aurez pas reçu la dose complète.
Vous pouvez entendre un clic au début de l’injection. Continuez à pousser.
Si vous sentez une résistance, continuez à pousser. Ceci est normal.
Le médicament s’injecte lorsque vous poussez. Poussez à la vitesse qui vous convient.
![]()
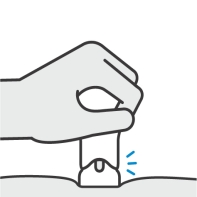
Vérifiez que votre injection est terminée
Votre injection est terminée lorsque :
- Le corps violet n’est plus visible.
- Vous ne pouvez plus pousser la poignée vers le bas.
- Vous pouvez entendre un clic.
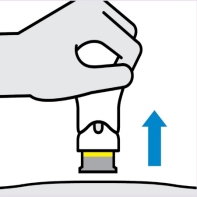
Soulevez droit vers le haut
La bande jaune indique que le protège aiguille est en place et verrouillé.

Jetez le stylo prérempli
Placez le stylo prérempli usagé dans un collecteur pour éliminer les objets tranchants, immédiatement après utilisation.
Ne jetez pas (n’éliminez pas) les stylos préremplis avec les ordures ménagères.
Ne recyclez pas le collecteur usagé.
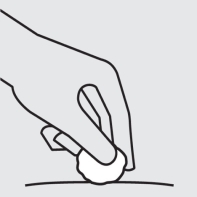
Vérifiez le site d’injection
Une petite quantité de sang ou de liquide peut être présente au site d’injection. Ceci est normal. Appuyez avec une boule de coton ou une compresse de gaze sur le site d’injection jusqu’à l’arrêt du saignement.
Ne frottez pas le site d’injection.
Si nécessaire, recouvrez le site d’injection d’un pansement.
Si vous recevez deux stylos préremplis de 45 mg pour une dose de 90 mg, répétez les étapes 1 à 3 avec le deuxième stylo prérempli. Choisissez un site d’injection différent pour la deuxième injection.
PRIX
| Code CNK | Emballage | Prix | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|
| 4721791 | STELARA 90 mg solution injectable en stylo prérempli | € 1405,91 | Oui | € 12,8 | € 8,5 |