Notice : Information du patient
Entyvio 108 mg, solution injectable en stylo prérempli
vedolizumab
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
- Gardez cette notice. Vous pourriez avoir besoin de la relire.
- Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
- Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
- Si vous ressentez un quelconque effet indésirable, parlez‑en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
Que contient cette notice ?
1. QU’EST‑CE QUE ENTYVIO ET DANS QUEL CAS EST‑IL UTILISÉ
Qu’est‑ce que Entyvio ?
Entyvio contient le principe actif nommé « vedolizumab ». Le vedolizumab fait partie d’un groupe de médicaments biologiques appelés les anticorps monoclonaux (AcM).
Comment Entyvio agit‑il ?
Le vedolizumab agit en bloquant une protéine à la surface de globules blancs responsables de l’inflammation dans la rectocolite hémorragique et la maladie de Crohn. Cela réduit le degré d’inflammation.
Dans quel cas Entyvio est‑il utilisé ?
Entyvio est utilisé chez l’adulte pour traiter les signes et symptômes de la :
- rectocolite hémorragique active modérée à sévère
- maladie de Crohn active modérée à sévère.
Rectocolite hémorragique
La rectocolite hémorragique est une maladie qui provoque une inflammation du gros intestin. Si vous souffrez de rectocolite hémorragique, vous recevrez d’abord d’autres médicaments. Si vous ne répondez pas suffisamment bien à ces médicaments ou que vous ne les tolérez pas, votre médecin pourra vous donner Entyvio afin de réduire les signes et symptômes de votre maladie.
Maladie de Crohn
La maladie de Crohn est une maladie qui provoque une inflammation du système digestif. Si vous souffrez de la maladie de Crohn, vous recevrez d’abord d’autres médicaments. Si vous ne répondez pas suffisamment bien à ces médicaments ou que vous ne les tolérez pas, votre médecin pourra vous donner Entyvio afin de réduire les signes et symptômes de votre maladie.
2. QUELLES SONT LES INFORMATIONS À CONNAÎTRE AVANT D’UTILISER ENTYVIO
N’utilisez jamais Entyvio :
- si vous êtes allergique au vedolizumab ou à l’un des autres composants contenus dans ce médicament (mentionnés dans la rubrique 6).
- si vous présentez une infection active sévère, telle qu’une TB (tuberculose), une septicémie, une diarrhée et des vomissements sévères (gastro‑entérite), une infection du système nerveux.
Avertissements et précautions
Adressez‑vous à votre médecin, votre pharmacien ou votre infirmier/ère avant d’utiliser Entyvio.
Informez votre médecin, votre pharmacien ou votre infirmier/ère immédiatement lorsque vous utilisez ce médicament pour la première fois, en cours du traitement, ainsi qu’entre les doses :
- si vous faites l’expérience d’une vision floue ou double, ou d’une perte de vision, d’une difficulté à parler, de faiblesse dans un bras ou une jambe, d’un changement dans la façon dont vous marchez ou de problèmes d’équilibre, d’un engourdissement persistant, d’une diminution ou d’une perte de sensation, d’une perte de mémoire ou de confusion. Tous ces symptômes peuvent être révélateurs d’une maladie du cerveau grave et potentiellement fatale connue sous le nom de leuco‑encéphalopathie multifocale progressive (LEMP).
- si vous avez une infection, ou pensez avoir une infection ; les signes incluent une sensation de froid, des frissons, une toux persistante ou une forte fièvre. Certaines infections peuvent devenir graves, voire menacer la vie du malade si elles ne sont pas traitées.
- si vous présentez les signes d’une réaction allergique tels que respiration sifflante, difficulté respiratoire, urticaire, démangeaisons, gonflement ou état vertigineux. Pour des informations plus détaillées, voir les réactions allergiques à la rubrique 4.
- si vous devez être vacciné ou avez récemment été vacciné. Entyvio peut modifier la façon dont vous répondez à une vaccination.
- si vous avez un cancer, informez‑en votre médecin. Votre médecin devra décider si vous pouvez toujours être traité par Entyvio.
- si vous ne sentez pas d’amélioration, le vedolizumab peut mettre jusqu’à 14 semaines pour agir chez certains patients présentant une maladie de Crohn très active.
Enfants et adolescents
Entyvio n’est pas recommandé chez les enfants ou les adolescents (âgés de moins de 18 ans) en raison du manque d’informations relatives à l’utilisation de ce médicament dans ce groupe d’âge.
Autres médicaments et Entyvio
Informez votre médecin, pharmacien ou infirmier/ère si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
- Entyvio ne doit pas être donné avec d’autres médicaments biologiques qui inhibent votre système immunitaire, l’effet de cette association n’étant pas connu.
Informez votre médecin si vous avez précédemment pris :
- du natalizumab (médicament utilisé pour la sclérose en plaques) ou
- du rituximab (médicament utilisé pour certains types de cancer et la polyarthrite rhumatoïde).
Votre médecin décidera si vous pouvez recevoir Entyvio.
Grossesse et allaitement
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin avant d’utiliser ce médicament.
Grossesse
Les effets d’Entyvio chez la femme enceinte ne sont pas connus. Par conséquent, ce médicament n’est pas recommandé pendant la grossesse. Votre médecin et vous devez déterminer si le bénéfice pour vous surpasse clairement le risque potentiel pour vous‑même ou votre bébé.
Si vous êtes une femme en âge de procréer, il vous est déconseillé d’être enceinte pendant votre traitement par Entyvio. Vous devez utiliser une contraception efficace pendant le traitement et pendant au moins 4,5 mois après la dernière prise du traitement.
Allaitement
Si vous allaitez ou prévoyez d'allaiter, informez‑en votre médecin. Entyvio passe dans le lait maternel. Il n’existe pas suffisamment de données sur l’effet que cela pourrait avoir sur votre bébé ou sur la production de lait. Une décision doit être prise soit d’arrêter l’allaitement soit d’arrêter le traitement par Entyvio en prenant en compte le bénéfice de l’allaitement pour votre enfant au regard du bénéfice du traitement pour vous.
Conduite de véhicules et utilisation de machines
Ce médicament a un effet mineur sur votre aptitude à conduire des véhicules ou à utiliser des outils ou des machines. Un faible nombre de patients a eu des étourdissements après avoir reçu Entyvio. Si vous ressentez des étourdissements, ne conduisez pas et n’utilisez pas d’outils ni de machines.
Entyvio 108 mg, solution injectable contient du sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c.‑à‑d. qu’il est essentiellement « sans sodium ».
Entyvio contient du polysorbate 80
Ce médicament contient 1,48 mg de polysorbate 80 par stylo prérempli d’Entyvio 108 mg. Les polysorbates peuvent provoquer des réactions allergiques. Informez votre médecin si vous avez des allergies connues.
3. COMMENT UTILISER ENTYVIO
Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin ou pharmacien. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Vous ou votre aidant recevrez une formation sur l’utilisation des injections d’Entyvio sous la peau (injections sous‑cutanées).
Quelle dose d’Entyvio allez‑vous recevoir ?
Le traitement par Entyvio est identique pour la rectocolite hémorragique et la maladie de Crohn.
La dose recommandée est de 108 mg d’Entyvio administrée par injection sous‑cutanée une fois toutes les 2 semaines.
- Au début du traitement, le médecin administrera les premières doses d’Entyvio par le biais d’un goutte‑à‑goutte dans une veine de votre bras (perfusion intraveineuse) pendant environ 30 minutes.
- Après au moins 2 perfusions intraveineuses, vous pourrez commencer à recevoir Entyvio par injection sous‑cutanée. La première injection sous‑cutanée sera administrée au moment de la prochaine perfusion intraveineuse programmée, puis toutes les 2 semaines.
Injection d’Entyvio
Les injections sous‑cutanées peuvent être administrées par vous‑même ou votre aidant, après avoir reçu la formation correspondante. Des instructions sont fournies à la fin de cette notice.
Si vous oubliez ou manquez une injection d’Entyvio
Si vous oubliez ou manquez une dose, injectez‑vous la dose suivante dès que possible puis toutes les 2 semaines.
Si vous arrêtez d’utiliser Entyvio
N’arrêtez pas d’utiliser Entyvio sans en parler d’abord à votre médecin.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, votre pharmacien ou votre infirmier/ère.
4. QUELS SONT LES EFFETS INDÉSIRABLES ÉVENTUELS
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
Effets indésirables graves
Informez immédiatement votre médecin si vous remarquez l’un ou l’autre des symptômes suivants :
- réactions allergiques (pouvant affecter jusqu’à 1 personne sur 100) dont les signes peuvent inclure : respiration sifflante ou difficulté respiratoire, urticaire, démangeaisons, gonflement, état vertigineux, rougeur de la peau, et
- infections (pouvant affecter jusqu’à 1 personne sur 10) dont les signes peuvent inclure : sensation de froid ou frissons, forte fièvre ou éruption cutanée
Autres effets indésirables
Informez votre médecin dès que possible si vous remarquez l’un des effets indésirables suivants :
Effets indésirables très fréquents (pouvant affecter plus de 1 personne sur 10)
- rhume
- douleurs articulaires
- maux de tête
Effets indésirables fréquents (pouvant affecter jusqu’à 1 personne sur 10)
- pneumonie
- infection du gros intestin par la bactérie Clostridium difficile
- fièvre
- infection pulmonaire
- modifications du fonctionnement de votre foie, augmentation des enzymes hépatiques (mise en évidence par les analyses de sang)
- fatigue
- toux
- grippe
- mal de dos
- douleur à la gorge
- infection des sinus
- démangeaisons
- éruptions cutanées et rougeurs
- douleurs dans les membres
- crampes musculaires
- faiblesse musculaire
- infection de la gorge
- gastroentérite
- infection anale
- lésions anales
- constipation
- ballonnements
- flatulences
- hypertension artérielle
- picotements ou fourmillements
- brûlures d’estomac
- hémorroïdes
- nez bouché
- eczéma
- sueurs nocturnes
- acné
- réactions au site d’injection (y compris douleur, gonflement, rougeur ou démangeaisons)
- zona (herpès zoster)
Effets indésirables peu fréquents (pouvant affecter jusqu’à 1 personne sur 100)
- rougeur et sensibilité au toucher des follicules pileux
- mycose de la gorge et de la bouche
- infection vaginale
- vision floue (perte de netteté de la vue)
Effets indésirables très rares (pouvant affecter jusqu’à 1 personne sur 10 000)
- réaction allergique soudaine et grave pouvant entraîner une difficulté respiratoire, gonflement, rythme cardiaque rapide, sueurs, baisse de la tension artérielle, étourdissements, perte de conscience et collapsus (réaction anaphylactique et choc anaphylactique)
- inflammation du foie (hépatite). Les signes et symptômes de l’hépatite peuvent comprendre des anomalies des tests de la fonction hépatique, une coloration jaunâtre des yeux ou de la peau (ictère), une douleur à droite de l’abdomen, des ecchymoses
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles)
- affection pulmonaire pouvant entraîner un essoufflement (pneumopathie interstitielle)
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez‑en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration :
Belgique
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance:
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER ENTYVIO
- Tenir ce médicament hors de la vue et de la portée des enfants
- N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage et sur l’étiquette après EXP. La date de péremption fait référence au dernier jour de ce mois
- Entyvio est à usage unique.
- À conserver au réfrigérateur (entre 2 °C et 8 °C). Conserver le(s) stylo(s) prérempli(s) dans l’emballage d’origine à l’abri de la lumière. Si nécessaire, un stylo prérempli peut être conservé hors du réfrigérateur à l’abri de la lumière à température ambiante (jusqu’à 25 °C) pendant 7 jours maximum. Ne pas utiliser le stylo prérempli si celui‑ci a été conservé hors du réfrigérateur pendant plus de 7 jours.
- Ne pas congeler. Ne pas exposer à la lumière directe du soleil.
- N’utilisez pas ce médicament si vous remarquez des particules dans le liquide ou une décoloration (la solution doit être incolore à jaune) avant l’administration.
- Ne jetez aucun médicament au tout‑à‑l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient Entyvio
- La substance active est le vedolizumab. Chaque stylo prérempli contient 108 mg de vedolizumab.
- Les autres composants sont l’acide citrique monohydraté (E 330), le citrate de sodium dihydraté (E 331), la L‑histidine, le monochlorhydrate de L‑histidine, le chlorhydrate de L‑arginine, le polysorbate 80 (E 433) et l’eau pour préparations injectables. Voir la rubrique 2 « Entyvio 108 mg, solution injectable contient du sodium » et « Entyvio contient du polysorbate 80 ».
Comment se présente Entyvio et contenu de l’emballage extérieur
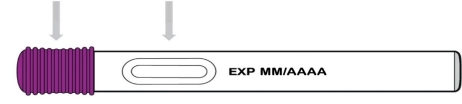
- Entyvio est une solution injectable incolore à jaune fournie dans un stylo prérempli en verre pourvu d’un dispositif de sécurité automatique de l’aiguille qui s’active et vient verrouiller une protection par‑dessus l’aiguille une fois le stylo retiré du site d’injection.
- Entyvio est disponible dans des emballages contenant 1, 2 ou 6 stylo(s) prérempli(s). Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’Autorisation de mise sur le marché
Takeda Pharma A/S
Delta Park 45
2665 Vallensbaek Strand
Danemark
Fabricant
Takeda Austria GmbH
St. Peter‑Straβe 25
A‑4020 Linz
Autriche
Pour toute information complémentaire concernant ce médicament, veuillez prendre contact avec le représentant local du titulaire de l’autorisation de mise sur le marché :
België/Belgique/Belgien | Lietuva |
България | Luxembourg/Luxemburg |
Česká republika | Magyarország |
Danmark | Malta |
Deutschland | Nederland |
Eesti | Norge |
Ελλάδα | Österreich |
España | Polska |
France | Portugal |
Hrvatska | România |
Ireland | Slovenija |
Ísland | Slovenská republika |
Italia | Suomi/Finland |
Κύπρος | Sverige |
Latvija |
|
La dernière date à laquelle cette notice a été révisée est 01/2026.
Autres sources d’informations
Cette notice est disponible dans des formats appropriés pour les aveugles ou les mal‑voyants ; demandez‑la auprès de votre représentant local du titulaire de l’autorisation de mise sur le marché.
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’Agence européenne des médicaments https://www.ema.europa.eu.
-----------------------------------------------------------------------------------------------------------------------
Les informations suivantes sont destinées exclusivement aux professionnels de la santé.
Traçabilité
Afin d’améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
Mode d’emploi :
Veuillez lire et respecter ces instructions avant l’injection du médicament. Votre médecin, infirmier/ère ou pharmacien doit vous montrer comment utiliser le stylo prérempli d’Entyvio avant que vous l’utilisiez pour la première fois.
Votre stylo prérempli unidose d’Entyvio
Avant utilisation | |||
Capuchon violet | Fenêtre de visualisation |
|
|
| |||
Après utilisation | |||
| Fenêtre de visualisation (injection terminée) |
|
|
| |||
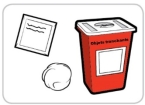
1) Posez le matériel dont vous avez besoin pour l’injection sur une surface propre et plane |
|
|
|
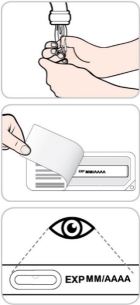
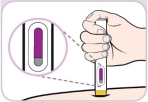
2) Ouvrez et inspectez le stylo prérempli |
|
|
|
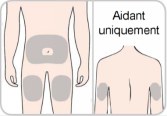
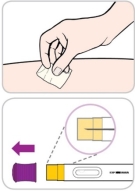
3) Préparez le site d’injection |
|
|
|
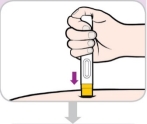
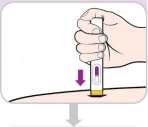
4) Injectez Entyvio | |
|
|
5) Jetez le matériel usagé |
|
|
|
PRIX
| Code CNK | Emballage | Prix | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|
| 4297081 | ENTYVIO 108MG SOL INJ STYLO PREREMPLIE 6 | € 2785,13 | Oui | € 12,8 | € 8,5 |
| 4301693 | ENTYVIO 108MG SOL INJ STYLO PREREMPLIE 2 | € 936,53 | Oui | € 12,8 | € 8,5 |