- Aperçu notices
- Notice
NOTICE : INFORMATION DE L’UTILISATEUR
Minirin Spray 10 microgrammes/dose solution pour pulvérisation nasale
Acétate de desmopressine
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
Gardez cette notice. Vous pourriez avoir besoin de la relire.
Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
Que contient cette notice ?
- 1. QU’EST-CE QUE MINIRIN SPRAY 10 MICROGRAMMES/DOSE SOLUTION POUR PULVÉRISATION NASALE ET DANS QUEL CAS EST-IL UTILISÉ ?
- 2. QUELLES SONT LES INFORMATIONS À CONNAÎTRE AVANT D’UTILISER MINIRIN SPRAY 10 MICROGRAMMES/DOSE SOLUTION POUR PULVÉRISATION NASALE ?
- 3. COMMENT UTILISER MINIRIN SPRAY 10 MICROGRAMMES/DOSE SOLUTION POUR PULVÉRISATION NASALE ?
- 3. TEST DE LA FONCTION RÉNALE
- 4. QUELS SONT LES EFFETS INDÉSIRABLES ÉVENTUELS ?
- 5. COMMENT CONSERVER MINIRIN SPRAY 10 MICROGRAMMES/DOSE SOLUTION POUR PULVÉRISATION NASALE
- 6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
1. QU’EST-CE QUE MINIRIN SPRAY 10 MICROGRAMMES/DOSE SOLUTION POUR PULVÉRISATION NASALE ET DANS QUEL CAS EST-IL UTILISÉ ?
Groupe de médicaments
Hormone de l’hypophyse; analogue de la vasopressine, l’hormone naturelle qui limite la quantité d’urine produite (qui la rend plus concentrée).
Indications thérapeutiques
- Traitement de la miction excessive et d’une sensation de soif anormalement élevée, causées par un déficit en l’hormone régulant l’élimination d’eau par les reins.
- Traitement de la miction excessive et d’une sensation de soif excessive survenant après une intervention chirurgicale dans la région de l’hypophyse.
- Diagnostic de diabète insipide d’origine centrale (maladie décrite ci-dessus) et contrôle de la fonction rénale (possibilité des reins d’extraire l’eau de l’urine).
Seul un diabète insipide confirmé peut être traité de manière chronique par Minirin Spray.
2. QUELLES SONT LES INFORMATIONS À CONNAÎTRE AVANT D’UTILISER MINIRIN SPRAY 10 MICROGRAMMES/DOSE SOLUTION POUR PULVÉRISATION NASALE ?
N’utilisez jamais Minirin Spray
- si vous êtes allergique à la desmopressine ou à l’un des autres composants contenus dans ce médicament mentionnés dans la rubrique 6.
- si vous éprouvez une sensation accrue de soif et si vous urinez beaucoup sans qu’un diabète insipide soit confirmé (risque d’accumulation excessive de liquide en cas de consommation de quantités excessives de liquide).
- si vous présentez une insuffisance de fonctionnement du cœur connue ou suspectée ou une autre affection qui font que vous devez prendre des médicaments diurétiques.
- si vous présentez une réduction modérée ou sévère de la fonction rénale.
- si vous savez que vous avez un trop faible taux de sodium dans le sang ou que vous y êtes prédisposé.
- si vous souffrez d’un SIADH (syndrome de sécrétion excessive d’hormone antidiurétique, l’hormone naturelle contrôlant l’équilibre hydrique).
Avertissements et précautions
- En cas d’utilisation de Minirin Spray, il est recommandé de démarrer par la dose la plus faible, de l’augmenter prudemment et de veiller à ce que les enfants soient surveillés lors de l’administration afin de garantir la prise d’une dose correcte.
- L’apport de liquide doit être limité au minimum à partir d’une heure avant et jusqu’à 8 heures après l’administration.
- Si vous recevez Minirin Spray pour un test de la fonction rénale, l’apport de liquide doit être limité et vous ne pouvez consommer au maximum que 0,5 l entre une heure avant et jusqu’à 8 heures après l’administration.
- Chez les enfants de moins de 1 an, le test de la fonction rénale peut uniquement être effectué à l’hôpital sous étroite surveillance.
- Si vous utilisez Minirin Spray sans restriction simultanée de l’apport de liquide, il peut se produire une accumulation de liquide et/ou un trop faible taux de sodium dans le sang, avec ou sans signes d’alarme (maux de tête, nausées/vomissements, prise de poids et, dans les cas graves, convulsions).
- En cas de prise de poids progressive ou d’un trop faible taux de sodium dans le sang, il faut limiter de manière drastique l’apport de liquide, et votre médecin arrêtera éventuellement l’administration de Minirin Spray.
- Habituellement, un traitement correct du diabète insipide supprime automatiquement la sensation de soif. Vous devez y être attentif chez les jeunes enfants, par exemple.
- Vous devez vous assurer avant de démarrer le traitement, vous êtes vérifié que vous n’avez pas de dysfonctionnement vésical grave et d’obstruction des voies urinaires.
- Si l’équilibre hydrique et/ou électrolytique est perturbé, comme en cas d’infections généralisées, de fièvre ou d’une inflammation gastro-intestinale, il faut interrompre ou soigneusement adapter le traitement.
- Si vous présentez un risque de pression accrue dans le crâne (risque accru d’un trop faible taux de sodium dans le sang/intoxication par l’eau).
- Si vous êtes un enfant, affaibli ou âgé, ou si vous avez déjà un faible taux de sodium dans le sang, vous pouvez présenter un risque accru d’un trop faible taux de sodium dans le sang.
- Si vous prenez simultanément des médicaments connus pour induire un SIADH (syndrome de sécrétion excessive d’hormone antidiurétique, l’hormone naturelle contrôlant l’équilibre hydrique) (voir “Autres médicaments et Minirin Spray”).
- Si vous prenez simultanément des AINS (médicaments anti-inflammatoires non stéroïdiens; ce sont des médicaments qui inhibent l’inflammation). Veuillez également lire la rubrique “Autres médicaments et Minirin Spray”.
- Si vous recevez du liquide dans une veine après une opération.
- Si vous avez eu auparavant une cirrhose du foie (affection hépatique induite par l’alcool), un syndrome néphrotique (trouble rénal), un fonctionnement insuffisant des surrénales et une fonction thyroïdienne trop faible.
- Les données de post-commercialisation ont montré qu’il existe un risque d’un beaucoup trop faible taux de sodium dans le sang lors de l’utilisation de la pulvérisation nasale pour traiter le diabète insipide d’origine centrale.
Dans les cas ci-dessus, votre médecin prendra des précautions à prévenir la survenue d’un trop faible taux de sodium dans le sang et surveillera attentivement la restriction de votre apport de liquide.
- Si vous êtes atteint d’une maladie des artères coronaires, si vous avez une tension artérielle élevée ou si vous êtes enceinte, vous devez être traité(e) avec vigilance et votre tension artérielle doit être contrôlée régulièrement, même si Minirin Spray n’exerce probablement aucun effet sur la tension artérielle à la dose prescrite.
- Si vous avez un diabète insipide après une lésion ou une opération. Dans ces cas, le diabète insipide peut être de nature transitoire. Pour cette raison, vous devez être régulièrement contrôlé(e).
- Si vous êtes un patient atteint de mucoviscidose (affection se caractérisant par la sécrétion d’un mucus anormalement épais au niveau des poumons et du pancréas), il faut surveiller attentivement l’utilisation de Minirin Spray.
- Si vous prenez encore d’autres médicaments. Veuillez également lire la rubrique “Autres médicaments et Minirin Spray”.
Des réactions anaphylactiques (réactions d’hypersensibilité très graves, mettant la vie en danger) n’ont pas été observées dans les études cliniques. Il y a eu néanmoins des rapports spontanés de réactions d’hypersensibilité générales graves.
Veuillez consulter votre médecin si l’une des mises en garde mentionnées ci-dessus est d’application pour vous, ou si elle l’a été dans le passé.
Adressez-vous à votre médecin ou pharmacien avant d’utiliser Minirin Spray.
Autres médicaments et Minirin Spray
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament.
Les médicaments connus pour induire un SIADH (syndrome de sécrétion excessive d’hormone antidiurétique, l’hormone naturelle contrôlant l’équilibre hydrique), tels que certains médicaments utilisés en cas de dépression, plus précisément des antidépresseurs tricycliques et des inhibiteurs sélectifs de la recapture de la sérotonine, le chlorpropamide (utilisé en cas de diabète), la chlorpromazine (utilisée en cas de maladie mentale), l’oxcarbazépine et la carbamazépine (utilisées en cas d’épilepsie), peuvent exercer un effet supplémentaire favorisant la rétention de liquide et augmenter ainsi le risque d’accumulation de liquide. Votre médecin doit tenir compte du fait qu’il/elle doit probablement adapter la posologie dans ces cas.
Des AINS peuvent causer une rétention de liquide/un trop faible taux de sodium dans le sang (voir la rubrique 2 “Avertissements et précautions”).
Il est improbable que Minirin Spray ait des interactions avec les médicaments agissant sur le métabolisme dans le foie.
Minirin Spray avec des aliments et boissons
Vous pouvez, si vous le souhaitez, utiliser Minirin Spray en même temps que des aliments et des boissons. Néanmoins, l’apport de liquide doit être limité au minimum à partir d’une heure avant et jusqu’à 8 heures après l’administration. Veuillez également lire la rubrique “Avertissements et précautions”.
Grossesse, allaitement et fertilité
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Par précaution, il est préférable d’éviter d’utiliser Minirin Spray pendant la grossesse.
Minirin Spray peut être utilisé pendant l’allaitement, avec prudence et selon la prescription du médecin. Néanmoins, l’administration doit se faire avec la prudence nécessaire et après avoir consulté le médecin.
Conduite de véhicules et utilisation de machines
Minirin Spray n’a aucun effet ou qu’un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines.
Minirin Spray contient du chlorure de benzalkonium
Ce médicament contient 0,1 mg de chlorure de benzalkonium dans chaque millilitre. Le chlorure de benzalkonium peut provoquer des irritations ou un gonflement à l’intérieur du nez, surtout s’il est utilisé sur une longue période.
3. COMMENT UTILISER MINIRIN SPRAY 10 MICROGRAMMES/DOSE SOLUTION POUR PULVÉRISATION NASALE ?
Veillez à toujours prendre ce médicament en suivant exactement les indications de votre médecin ou pharmacien. Vérifiez auprès de votre médecin ou votre pharmacien en cas de doute.
Généralités
Votre médecin doit respecter une restriction de liquide (voir “Avertissements et précautions”).
Si des signes ou des symptômes d’une rétention de liquide et/ou d’un trop faible taux de sodium dans le sang apparaissent (maux de tête, nausées/vomissements, prise de poids et, dans les cas graves, convulsions), il faut interrompre votre traitement jusqu’à ce que vous soyez complètement rétabli. Si votre médecin reprend le traitement, il/elle doit instaurer une restriction de liquide stricte (voir “Quelles sont les informations à connaître avant d’utiliser Minirin Spray 10 microgrammes/dose solution pour pulvérisation nasale ?”).
Il faut adapter la quantité de médicament selon la personne. Votre médecin débute par une quantité-test.
Adultes : Habituellement, votre médecin débute par une quantité-test de 10 microgrammes (1 pulvérisation). Vous obtenez habituellement une production d’urine normale avec 10 à 20 microgrammes (1 à 2 pulvérisations), deux fois par jour.
Un traitement requiert en général 2 doses nasales.
Lorsque vous ne pouvez pas concentrer l’urine après une rétention de liquide et que vous y arrivez après administration de Minirin Spray (20 microgrammes = 2 pulvérisations), c’est le signe d’un diabète insipide d’origine centrale.
3. TEST DE LA FONCTION RÉNALE
Votre médecin vérifie ainsi quelles concentrations de sel sont atteintes dans l’urine après administration de Minirin Spray. Votre médecin compare aux valeurs que vous obtenez lors d’une fonction rénale normale.
Les quantités de Minirin Spray administrées à ce but sont les suivantes :
pour les adultes et les enfants âgés de plus de 15 ans : 40 microgrammes (4 pulvérisations).
Pour éviter une intoxication par l’eau, l’apport de liquide doit être limité à un maximum de 0,5 l pendant 1 heure avant et jusqu’à 8 heures après l’administration de Minirin Spray. Vous devez vider la vessie avant l’administration de Minirin Spray.
Après l’administration de Minirin, toute l’urine collectée pendant la première heure doit être jetée. Pendant les 8 heures suivantes, 2 portions d’urine sont collectées pour contrôler la concentration de sel.
Votre médecin vous dira combien de temps vous devez utiliser Minirin Spray.
Utilisation chez les enfants et les adolescents
Minirin Spray ne convient pas si des doses inférieures à 10 microgrammes sont nécessaires. Dans ces cas, vous pouvez utiliser Minirin gouttes nasales administrées par Rhinyle.
Il est recommandé d’administrer la dose aux enfants sous la surveillance d’un adulte, qui veillera à ce que la dose correcte soit prise.
Diabète insipide
Il faut adapter la quantité de médicament selon la personne. Habituellement, votre médecin débute par une dose-test.
Pour les enfants, la dose-test est de 5 microgrammes.
Pour les nourrissons, la dose-test est de 2,5 microgrammes.
Un traitement requiert en général 2 doses nasales.
Minirin Spray ne convient pas si des doses inférieures à 10 microgrammes sont nécessaires. Dans ces cas, vous pouvez utiliser Minirin gouttes nasales administrées par Rhinyle.
Diagnostic du diabète insipide d’origine centrale
La posologie doit être adaptée d’une personne à l’autre selon l’âge de l’enfant et l’état pour maintenir l’équilibre hydrique et l’élimination normale de l’urine.
Test de la fonction rénale
- Enfants âgés de plus de 15 ans : 40 microgrammes (4 pulvérisations).
- Enfants âgés de moins de 15 ans : 20 microgrammes (2 pulvérisations).
- Nourrissons (< 1 an) : 10 microgrammes (1 pulvérisation).
Utilisation chez les populations spécifiques
Patients présentant des troubles rénaux : Minirin ne doit pas être utilisé chez les patients souffrant de troubles rénaux modérés à sévères (voir la rubrique 2).
Comment utiliser la pulvérisation nasale ?
Avant chaque administration, il faut se moucher le nez afin de favoriser l’absorption du produit par la muqueuse nasale.
- Otez le bouchon protecteur en plastique transparent et conservez-le afin de pouvoir refermer le flacon par la suite.
- Pour obtenir la quantité exacte du médicament, inclinez légèrement le flacon afin que le petit tube en plastique plonge dans la solution.
- Préparez le spray en pulvérisant 3 à 4 fois.
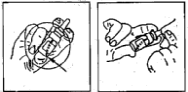
- Inclinez légèrement la tête en arrière. Introduisez l’embout nasal dans une narine et exercez une pression.
- Dès que le spray est prêt à l’emploi, il délivre 100 microlitres à chaque pulvérisation (soit une dose de 10 microgrammes).
- Lorsque plusieurs pulvérisations sont requises, pulvérisez alternativement dans les deux narines et patientez au moins 5 minutes entre 2 pulvérisations dans une même narine en évitant tout mouchage.
- Après chaque utilisation, refermez le flacon et conservez-le en position verticale.
Si le spray n’a pas été utilisé pendant une semaine, il est nécessaire d’amorcer à nouveau la pompe pour pulvérisation en appuyant une fois.
En cas de doute d’avoir pris la dose correcte, vous ne devez pas réutiliser le spray avant la prochaine dose prévue.
Si vous avez utilisé plus de Minirin Spray que vous n’auriez dû
Si vous avez utilisé une trop grande quantité de pulvérisation nasale, cela se traduit par une durée d’action prolongée, s’accompagnant d’un risque accru d’accumulation de liquide et d’un trop faible taux de sodium dans le sang.
Traitement
Le traitement est adapté selon la personne par le médecin. Habituellement, vous devez arrêter le traitement par Minirin Spray et limiter l’apport de liquide, et un traitement directement axé sur les symptômes qui se produisent chez vous est instauré, le cas échéant.
En cas de suspicion d’œdème cérébral, une prise en charge immédiate dans un service de soins intensifs est requise.
Si vous avez utilisé ou pris trop de Minirin Spray, prenez immédiatement contact avec votre médecin, votre pharmacien ou le Centre Antipoison (070/245.245).
Si vous oubliez d’utiliser Minirin Spray
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez d’utiliser Minirin Spray
Consultez toujours votre médecin si vous envisagez d’arrêter le traitement.
Consultez toujours votre médecin pour réduire lentement la dose, autrement les symptômes peuvent réapparaître.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDÉSIRABLES ÉVENTUELS ?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
L’effet indésirable le plus grave de Minirin est un trop faible taux de sodium dans le sang.
Si, lors de l’utilisation de Minirin Spray, vous ne réduisez pas simultanément votre apport de liquide, cela peut entraîner une accumulation de liquide/un trop faible taux de sodium dans le sang, avec ou sans signes d’alarme tels que des maux de tête, des nausées/vomissements, une prise de poids, un malaise, des douleurs abdominales, des crampes musculaires, des étourdissements, de la confusion, une conscience diminuée et, dans les cas graves, des convulsions et un coma.
Une accumulation de liquide peut survenir en cas d’utilisation de trop grandes quantités, de mauvais diagnostic ou d’apport excessif de liquide pendant le traitement.
Des réactions anaphylactiques (réactions d’hypersensibilité très graves, mettant la vie en danger) n’ont pas été observées dans les études cliniques. Il y a eu néanmoins des rapports spontanés de réactions d’hypersensibilité générales graves.
L’évaluation des effets indésirables est basée sur le degré de leur apparition :
Très fréquent : peut affecter plus de 1 personne sur 10
Fréquent : peut affecter jusqu’à 1 personne sur 10
Peu fréquent : peut affecter jusqu’à 1 personne sur 100
Rare : peut affecter jusqu’à 1 personne sur 1000
Très rare : peut affecter jusqu’à 1 personne sur 10 000
Fréquence indéterminée : ne peut être estimée sur la base des données disponibles
Très fréquent (peut affecter plus de 1 personne sur 10) :
- Affections respiratoires, thoraciques et médiastinales : congestion nasale/inflammation de la muqueuse nasale
- Investigations : température corporelle élevée**
Fréquent (peut affecter jusqu’à 1 personne sur 10) :
- Affections psychiatriques : insomnie, affection labile**, cauchemars**, nervosité**, agression**
- Affections du système nerveux : maux de tête*
- Affections respiratoires, thoraciques et médiastinales : saignement nasal, infection des voies respiratoires supérieures**
- Affections gastro-intestinales : gastroentérite, nausées*, douleurs abdominales*
- Troubles généraux et anomalies au site d’administration : fatigue*
Peu fréquent (peut affecter jusqu’à 1 personne sur 100) :
- Troubles du métabolisme et de la nutrition : trop faible taux de sodium dans le sang
- Affections gastro-intestinales : vomissements*
Rare (peut affecter jusqu’à 1 personne sur 1000) :
- Affections du système nerveux : étourdissements*
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) :
- Affections du système immunitaire : réactions d’hypersensibilité
- Troubles du métabolisme et de la nutrition : déshydratation***
- Affections psychiatriques : confusion*
- Affections du système nerveux : convulsions*, coma*, somnolence
- Affections vasculaires : tension artérielle élevée
- Affections respiratoires, thoraciques et médiastinales : essoufflement
- Affections gastro-intestinales : diarrhées
- Affections de la peau et du tissu sous-cutané : démangeaisons, éruption cutanée, urticaire
- Affections musculo-squelettiques et systémiques : spasmes musculaires*
- Troubles généraux et anomalies au site d’administration : accumulation de liquide dans les membres, douleurs thoraciques, frissonnements
- Investigations : prise de poids*
* Observé relatif à un trop faible taux de sodium dans le sang.
** Observé principalement chez les enfants et les adolescents.
*** Observé dans l’indication de diabète insipide d’origine centrale.
Quelques cas d’atteinte des fibres nerveuses (démyélinisation) dus à une adaptation trop rapide du taux de sodium dans le sang ont été rapportés. Afin d’éviter cela, il faut traiter soigneusement un trop faible taux de sodium dans le sang.
Population pédiatrique
L’hyponatrémie (trop faible taux de sodium dans le sang) est réversible. Chez les enfants, cela est souvent lié à des changements dans la routine quotidienne qui influencent l’apport de liquide et/ou la sécrétion par la transpiration. Pour les enfants, une attention spéciale doit être accordée aux précautions décrites dans la rubrique 2.
Autres populations spécifiques
Les jeunes enfants, les patients âgés et les patients présentant un taux de sodium sérique dans l’intervalle inférieur des valeurs normales peuvent présenter un risque accru d’un trop faible taux de sodium dans le sang (voir la rubrique 2).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via :
Belgique
Agence Fédérale des Médicaments et des Produits de Santé (www.afmps.be)
Division Vigilance :
Site internet : www.notifieruneffetindesirable.be
E-mail : adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy ou Division de la Pharmacie et des Médicaments de la Direction de la Santé
Site internet : www.guichet.lu/pharmacovigilance
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER MINIRIN SPRAY 10 MICROGRAMMES/DOSE SOLUTION POUR PULVÉRISATION NASALE
Tenir hors de la vue et de la portée des enfants.
Ce médicament ne nécessite pas de précautions particulières de conservation. Conserver toujours le flacon avec pompe pour pulvérisation en position verticale.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’étiquette et l’emballage extérieur après “EXP”. La date de péremption fait référence au dernier jour de ce mois.
Ne jetez aucun médicament au tout-à-l’égout ni avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient Minirin Spray
- La substance active est la desmopressine. 1 ml de solution contient 0,1 mg d’acétate de desmopressine, ce qui correspond à 0,089 mg de desmopressine.
- Les autres composants sont le chlorure de sodium, l’acide citrique monohydraté, le phosphate disodique dihydraté, le chlorure de benzalkonium (solution) et l’eau purifiée.
Aspect de Minirin Spray et contenu de l’emballage extérieur
Flacon avec pompe pour pulvérisation et embout nasal contenant 2,5 ml de solution (correspondant à 25 doses).
Titulaire de l’autorisation de mise sur le marché et fabricant
Titulaire de l’autorisation de mise sur le marché
nv Ferring sa, The Crescent Business Center
Lenniksebaan 451, B-1070 Anderlecht
Tél. : +32 (0)53/72 92 00 – ferringnvsa@ferring.com
Fabricant
Ferring GmbH, Wittland 11, 24109 Kiel, Allemagne
Numéro de l’autorisation de mise sur le marché
Belgique
BE164954
Luxembourg
2005118290
Mode de délivrance
Médicament soumis à prescription médicale.
La dernière date à laquelle cette notice a été révisée est 12/2024.
PRIX
| Code CNK | Emballage | Prix | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|
| 1087030 | MINIRIN SPRAY 10MCG/DOS 2,5ML0,1MG | € 17,01 | Oui | - | - |