RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
1. DÉNOMINATION DU MÉDICAMENT VÉTÉRINAIRE
CYLANIC 250 mg + 62,5 mg comprimés pour chiens et chats
4. INFORMATIONS CLINIQUES
4.2 Indications d’utilisation, en spécifiant les espèces cibles
Pour le traitement des infections causées par des bactéries sensibles à l’amoxicilline et à l’acide clavulanique, notamment : les maladies de la peau (y compris les pyodermies profondes et superficielles) ; les infections des tissus mous (abcès et sacculite anale) ; les infections dentaires
(par exemple, la gingivite) ; les infections des voies urinaires ; les maladies respiratoires (impliquant les voies respiratoires supérieures et inférieures) ; les entérites.
4.3 Contre-indications
Ne pas utiliser chez les lapins, les cobayes, les hamsters, les gerbilles ou les chinchillas.
Ne pas utiliser en cas d’hypersensibilité connue aux substances actives, à d’autres antimicrobiens du groupe des β-lactamines ou à l’un des excipients.
Ne pas utiliser chez les animaux présentant un dysfonctionnement grave des reins accompagné d’anurie et d’oligurie.
Ne pas utiliser chez les ruminants et les chevaux.
4.8 Interactions médicamenteuses et autres formes d’interactions
Le chloramphénicol, les macrolides, les sulfamides et les tétracyclines peuvent inhiber l’effet antibactérien des pénicillines en raison du début rapide de leur action bactériostatique. Tenir compte des allergies croisées potentielles avec d’autres pénicillines. Les pénicillines peuvent augmenter l’effet des aminoglycosides.
4.9 Posologie et voie d’administration
Pour administration orale.
La dose recommandée est de 12,5 mg/kg de poids vif (10 mg d’amoxicilline/2,5 mg d’acide clavulanique par kg de poids vif), deux fois par jour.
Le tableau suivant est destiné à servir de guide pour administrer les comprimés à la dose recommandée.
Pour assurer une posologie correcte le poids vif doit être déterminé aussi précisément que possible afin d’éviter tout risque de sous-dosage.
| Nombre de comprimés deux fois par jour | ||
Poids vif | Amoxicilline/Acide clavulanique | Amoxicilline/Acide clavulanique | Amoxicilline/Acide clavulanique |
1-1,25 | ¼ | - | - |
>1,25-2,5 | ½ | - | - |
>2,5-3,75 | ¾ | - | - |
>3,75-5 | 1 | - | - |
>5-6,25 | 1 ¼ | ¼ | - |
>6,25-12,5 | - | ½ | ¼ |
>12,5-18,75 | - | ¾ | - |
>18,75-25 | - | 1 | ½ |
>25-31,25 | - | 1 ¼ | - |
>31,25-37,5 | - | 1 ½ | - |
>37,5-50 | - | - | 1 |
>50-62,5 | - | - | 1 ¼ |
>62,5-75 | - | - | 1 ½ |
![]() = ¼ de comprimé
= ¼ de comprimé ![]() = ½ comprimé
= ½ comprimé ![]() = ¾ de comprimé
= ¾ de comprimé ![]() = 1 comprimé
= 1 comprimé
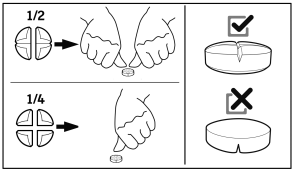
Les comprimés peuvent être divisés en 2 ou 4 parts égales afin d’assurer un dosage précis.
La durée minimale du traitement est de 5 jours, la majorité des cas de routine répondant après 5 à 7 jours de traitement.
Dans les cas chroniques ou réfractaires, un traitement plus long peut être nécessaire, par exemple pour les maladies cutanées chroniques : 10 à 20 jours, les cystites chroniques : 10 à 28 jours, les maladies respiratoires : 8 à 10 jours.
Dans de telles circonstances, la durée globale du traitement est laissée à la discrétion du clinicien, mais doit être suffisamment longue pour assurer la résolution complète de la maladie bactérienne.
4.11 Temps d’attente
Sans objet.