RESUME DES CARACTERISTIQUES DU PRODUIT
1. DENOMINATION
Duracef 500 mg gélules
Duracef 250 mg/5 ml poudre pour suspension buvable Duracef 500 mg/5 ml poudre pour suspension buvable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Duracef 500 mg gélules : Céfadroxil monohydraté (= 500 mg de céfadroxil anhydre) Duracef 250 mg/5 ml poudre pour suspension buvable : céfadroxil monohydraté (= 85,71 mg de céfadroxil anhydre par gramme de poudre)
Duracef 500 mg/5 ml poudre pour suspension buvable : céfadroxil monohydraté (= 171,42 mg de céfadroxil anhydre par gramme de poudre)
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Duracef 500 mg gélules
Duracef 250 mg/5 ml poudre pour suspension buvable Duracef 500 mg/5 ml poudre pour suspension buvable
4. DONNEES CLINIQUES
4.1 Indications thérapeutiques
Le céfadroxil est indiqué dans le traitement des infections suivantes, lorsqu'elles sont causées par des germes sensibles :
Infections des voies respiratoires : Amygdalite, pharyngite bactérienne, sinusite,
laryngite.
La pénicilline est le médicament de choix pour des infections dues aux streptocoques A bêta-hémolytiques et la prévention du rhumatisme articulaire. Des études substantielles au sujet de l'efficacité du céfadroxil dans cette prophylaxie ne sont pas jusqu'à présent disponibles.
Infections de la peau et des tissus mous : Lymphangite, abcès, cellulite, ulcères de
décubitus, mastite, furonculose, érysipèle.
4.2 Posologie et mode d’administration
Posologie:
Des études ont démontré que le Duracef peut s'administrer en deux prises par jour. Dans le traitement des pharyngites à streptocoque du groupe A, le céfadroxil peut être administré en une seule prise par jour.*(voir tableau ci-dessous)
Cette prise monoquotidienne est susceptible de provoquer des effets indésirables digestifs plus fréquents et/ou plus intenses qu'une posologie administrée en plusieurs prises journalières.
Adultes
Page 1 de 10![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
La posologie moyenne habituelle pour les adultes est de 2 g par jour dans les infections courantes. Elle peut être augmentée en fonction de la gravité de l'infection. Elle peut être réduite à 1 g par jour en une seule prise pendant 10 jours dans la pharyngite à streptocoques.
Population pédiatrique
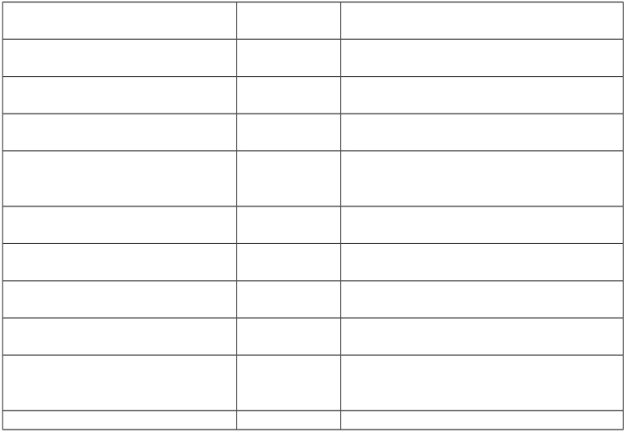
La dose journalière usuelle est de 30 mg/kg/jour. La dose peut être portée à 100 mg/kg/jour, si la gravité de l'infection l'exige.
| | |
| 2,5 ml 2,5 ml 5 ml 5 ml * 5 ml 1x/jour 10 ml 1x/jour |
Le traitement doit être poursuivi jusqu’à ce que l'éradication bactérienne ait été démontrée.
Un minimum de 10 jours de traitement est recommandé pour toute infection causée par des streptocoques bêta-hémolytiques du groupe A. La pénicilline est le médicament de choix pour les infections dues aux streptocoques A bêta-hémolytiques et la prévention du rhumatisme articulaire. Des études substantielles au sujet de l'efficacité du céfadroxil dans cette prophylaxie ne sont pas jusqu'à présent disponibles.
Dans les infections graves, présentant un danger vital ou exigeant des doses plus élevées ou plus rapprochées, un traitement par céphalosporines injectables ou par d’autres antibiotiques, devra être envisagé.
Les céphalosporines diffusent très faiblement dans le liquide céphalorachidien, elles ne sont pas indiquées dans le traitement des méningites même à germes sensibles.
Insuffisance rénale
Chez l'adulte, on recommande une dose initiale de 1000 mg de céfadroxil et une dose d'entretien de 500 mg à des intervalles de temps basés sur le niveau de la clairance de la créatinine.
Clairance de la créatinine Intervalles entre les prises de 1 g
25 à 50 ml/min. 12 heures
10 à 25 ml/min. 24 heures
0 à 10 ml/min. 36 heures
Les patients présentant un taux de clairance de la créatinine supérieur à
50 mL/min/1,73m² peuvent être traités comme s’ils avaient une fonction rénale normale.
Page 2 de 10
L'hémodialyse permet l'élimination d’environ 63 % d’une dose d’1 g de céfadroxil après 6 à 8 heures d’hémodialyse. La demi-vie d'élimination est d'environ 3 heures au cours de la dialyse.
Mode d’administration :
Le Duracef doit être administré par voie orale, sous forme de gélules ou de suspensions.
Le Duracef est stable en milieu acide et peut être administré sans tenir compte des repas.
En cas de troubles gastro-intestinaux, occasionnellement signalés, l'administration avec le repas peut aider à mieux les tolérer.
4.3 Contre-indications
Allergie connue aux antibiotiques du groupe des céphalosporines ou à tout autre composant de la formulation. Il existe une allergie croisée entre les antibiotiques du groupe des pénicillines et celui des céphalosporines chez certains patients.
4.8 Effets indésirables
Les effets indésirables observés avec le céfadroxil sont similaires à ceux observés avec d’autres céphalosporines.
Le tableau ci-après répertorie l’ensemble des effets indésirables actuellement mentionnés dans le RCP. La liste est présentée par classe de systèmes d’organes, par terme préféré dans la terminologie MedDRA et par fréquence, à l’aide des catégories de fréquence suivantes : très fréquent (≥ 1/10), fréquent (≥ 1/100, < 1/10), peu fréquent (≥ 1/1 000, < 1/100), rare
(≥ 1/10 000, < 1/1 000), très rare (< 1/10 000) et fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Effets indésirables médicamenteux observés dans l’expérience clinique ou post-AMM :
Classe de systèmes d’organes Fréquence Terme MedDRA
Infections et Infestations Rare Infection vaginale
Fréquence
indéterminée
Candidose génitale
Affections hématologiques et du système lymphatique
Fréquence
indéterminée
Agranulocytose, neutropénie et thrombocytopénie
Affections du système immunitaire
Fréquence
indéterminée
Réaction anaphylactique, œdème angioneurotique*, hypersensibilité*, maladie sérique
Affections gastro-intestinales
Fréquent
Diarrhées, dyspepsie, nausées, vomissements
Fréquence
indéterminée
Colite pseudomembraneuse
Affections hépatobiliaires
Fréquence
indéterminée
Insuffisance hépatique, cholestase, et anomalie de la fonction hépatique
Affections de la peau et du tissu sous-cutané
Rare
Urticaire*, rash*, prurit*
Fréquence
indéterminée
Syndrome de Stevens-Johnson, érythème multiforme ; nécrolyse epidermale toxique
Affections musculo-squelettiques Fréquence Arthralgie
Page 5 de 10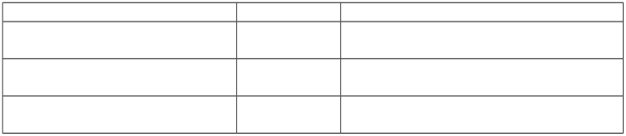
et systémiques indéterminée
Affections des organes de reproduction et du sein
Fréquence
indéterminée
Prurit génital
Troubles généraux et anomalies au site d'administration
Fréquent
Pyrexie
Investigations
Fréquence
indéterminée
Hausse des transaminases
*) Ces réactions se dissipent généralement dès l’arrêt du médicament.
Une éosinophilie, une leucopénie, une réaction de Coombs faussement positive directe et indirecte, une gêne abdominale, un étourdissement et une céphalée peuvent survenir.
Certains cas rares d’anémie hémolytique d’origine immunologique ont été rapportés pendant l’utilisation de céphalosporines. Un cas a été observé pendant le traitement par céfadroxil d’un patient ayant des antécédents confirmés d’allergie aux pénicillines, un test de Coombs positif et des anticorps anti-érythrocytaires étaient présents.
Troubles rénaux
L’antibiotique est éliminé tel quel par les reins. Ceci peut avoir un impact sur la fonction rénale si elle a été préalablement gravement touchée.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via l’Agence Fédérale des Médicaments et des Produits de Santé - Division Vigilance – EUROSTATION II - Place Victor Horta, 40/ 40 – B- 1060 Bruxelles – website : www.afmps.be - e-mail :
adversedrugreactions@fagg-afmps.be
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
PharmaSwiss Česká republika s.r.o
Jankovcova 1569/2c
170 00, Prague 7 Tchéquie
8. NUMEROS D'AUTORISATION DE MISE SUR LE MARCHE
Duracef 500 mg gélules : BE 108692
Duracef 250 mg/5 ml poudre pour suspension buvable : BE108577 Duracef 500 mg/5 ml poudre pour suspension buvable : BE108516
10. DATE DE MISE À JOUR DU TEXTE
Date de mise à jour du texte : 06/2018 Date d’approbation : 02/2019
Page 10 de 10
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 0838276 | DURACEF SUSP OR 1X80ML 250MG/5ML | J01DB05 | € 23,9 | - | Oui | € 12,37 | € 10,5 |
| 1204965 | DURACEF SUSP OR 1X80ML 500MG/5ML | J01DB05 | € 25,67 | - | Oui | € 13,39 | € 10,5 |