1. DENOMINATION DU MEDICAMENT
Combivent® 0,5 mg/2,5 ml + 2,5 mg/2,5 ml
Solution pour inhalation par nébuliseur
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
2,5 mL de solution pour inhalation contiennent 522 mcg de Bromure d'ipratropium monohydraté (= 500 mcg de bromure d'ipratropium anhydre) et 3013 mcg de Sulfate de salbutamol (= 2500 mcg salbutamol base).
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Solution pour inhalation par nébuliseur.
4. DONNEES CLINIQUES
4.1 Indications thérapeutiques
Combivent est indiquée dans le traitement du bronchospasme chez les adultes souffrant d'affections pulmonaires obstructives chroniques qui requièrent un traitement symptomatique par une combinaison anticholinergique/bêta-2-mimétique.
4.2 Posologie et mode d’administration
Posologie
Combivent solution pour inhalation par nébuliseur n'est destiné qu'aux adultes.
Adultes (y compris les personnes âgées)
La posologie recommandée est d'1 ampoule, 3 à 4 fois par jour.
Populations particulières
Insuffisance rénale ou hépatique
Aucune donnée n’est disponible. Combivent solution pour inhalation par nébuliseur sera administré avec prudence chez ces patients.
Population pédiatrique
Combivent n’est pas indiqué chez les enfants et les adolescents.
Asthme
Dans le cas de l’asthme, une thérapie anti-inflammatoire concomitante doit être envisagée.
Traitement des crises aiguës
Dans de nombreux cas, 1 ampoule est suffisante pour soulager les symptômes.
Dans les cas graves, si la crise n’a pas été soulagée avec 1 ampoule, l’administration d’une seconde ampoule peut s’avérer nécessaire. Il est alors conseillé aux patients de consulter immédiatement un médecin ou l’hôpital le plus proche.
Si des doses de Combivent plus élevées que celles recommandées sont nécessaires pour maîtriser les symptômes, le plan de traitement du patient doit être réévalué.
En cas de dyspnée aiguë s’aggravant rapidement, si le traitement par Combivent solution pour inhalation par nébuliseur n'apporte pas d'amélioration, il sera conseillé au patient de consulter immédiatement un médecin ou l’hôpital le plus proche.
Mode d’administration
Combivent solution pour inhalation par nébuliseur s'administre via un nébuliseur ou via un appareil à pression positive intermittente.
Chaque ampoule est prête à l'emploi et ne nécessite aucune dilution. Toutefois, certains types d'appareils requièrent un volume supérieur à 2,5 ml: dans ces cas, on ajoutera au Combivent du sérum physiologique pour atteindre le volume minimum nécessaire.
La solution est destinée à l'inhalation et non à l'ingestion par voie orale ou l’administation par voie parentérale.
Le traitement doit être initié et administré sous surveillance médicale, par exemple en milieu hospitalier. Un traitement à domicile n’est recommandé que dans des cas exceptionnels (symptômes graves ou patients nécessitant des doses plus élevées) quand une faible dose de bronchodilatateurs bêta-agonistes à action rapide a été insuffisante pour apporter un soulagement, après avoir consulté un médecin expérimenté.
Le traitement avec la solution pour inhalation par nébuliseur doit toujours être débuté par la dose la plus faible recommandée (1 ampoule). Dans les cas très graves, il est parfois nécessaire d’utiliser 2 ampoules pour soulager les symptômes. L’administration doit être arrêtée dès qu’un soulagement suffisant des symptômes est atteint.
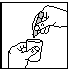
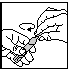
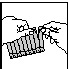
fig. 1 fig. 2 fig. 3
1. Préparer l'inhalateur suivant les instructions du fabricant ou du médecin.
2. Détacher une ampoule monodose de l'ensemble (fig. 1).
3. Ouvrir l’ampoule monodose par torsion de la partie supérieure (fig. 2).
4. Vider le contenu dans le réservoir de l'inhalateur et ajouter le diluant (fig. 3).
5. Utiliser l'inhalateur suivant les instructions.
6. Après emploi, jeter les restes éventuels de solution et nettoyer l'appareil.
Comme l’ampoule ne contient pas de conservateur, afin d'éviter toute contamination microbienne, il est important d’utiliser la solution pour inhalation dès l’ouverture et d’ouvrir une nouvelle ampoule pour chaque nouvelle aérosolisation. Les ampoules partiellement utilisées, ouvertes ou endommagées doivent être éliminées.
Il est fortement recommandé de ne pas mélanger Combivent solution pour inhalation par nébuliseur à d’autres médicaments dans le même inhalateur.
4.3 Contre-indications
Combivent est contre-indiqué chez les patients souffrant de :
Cardiomyopathie obstructive hypertrophique, tachyarythmie.
Hypersensibilité au principe actif ou à l’un des excipients mentionnés à la rubrique 6.1.
4.8 Effets indésirables
Résumé du profil de sécurité
La plupart des effets indésirables peuvent être attribués aux propriétés anticholinergiques et β-adrénergiques de Combivent. Comme tout traitement topique, Combivent peut entraîner des irritations locales.
Les effets indésirables les plus fréquents rapportés lors des études cliniques sont: céphalées, irritation de la gorge, toux, bouche sèche, troubles de la motilité gastro-intestinale (incluant constipation, diarrhée et vomissements), nausées et étourdissements.
Résumé tabulé des effets indésirables
Les effets indésirables ont été classés en fonction de leur incidence en utilisant la classification suivante:
Très fréquent ( 1/10) ; fréquent ( 1/100, <1/10) ; peu fréquent ( 1/1.000, <1/100) ; rare ( 1/10.000, < 1/1.000) ; très rare (<1/10.000).
Affections du système immunitaire: | |
rare: | - réaction anaphylactique* |
Troubles du métabolisme et de la nutrition: | |
rare: | - hypokaliémie* |
Affections psychiatriques: | |
peu fréquent: | - nervosité |
rare: | - troubles psychiques* |
Affections du système nerveux: | |
peu fréquent: | - céphalées |
rare: | - sudation |
Affections oculaires: | |
rare: | - troubles d’accommodation |
Affections cardiaques: | |
peu fréquent: | - palpitations |
rare: | - fibrillation auriculaire |
Affections respiratoires, thoraciques et médiastinales: | |
peu fréquent : | - toux |
rare: | - sécheresse de la gorge |
Affections gastro-intestinales: | |
peu fréquent: | - sécheresse buccale |
rare: | - diarrhée |
Affections de la peau et du tissus sous-cutané: | |
peu fréquent: | - réactions cutanées |
rare: | - rash |
Affections musculo-squelettiques et systémiques: | |
rare: | - crampes musculaires |
Affections du rein et des voies urinaires: | |
rare: | - rétention urinaire |
Troubles généraux et anomalies au site d'administration: | |
rare: | - asthénie |
Investigations |
|
peu fréquent: | - augmentation de la tension artérielle (systolique) |
* Effet secondaire non observé dans aucun des essais cliniques sélectionnés sur Combivent. Une estimation de la fréquence de remplacement est accomplie selon la EU SmPC Guideline avec 3/3488=0.00086 qui se rapporte à « rare ».
Déclaration des effets indésirables suspectés:
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration:
Belgique
Agence fédérale des médicaments et des produits de santé - Division Vigilance
Boîte postale 97 - B-1000 Bruxelles Madou
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
Boehringer Ingelheim SComm
Avenue Arnaud Fraiteur 15-23
1050 Bruxelles
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
Belgium : BE187056
Luxembourg : 0632/01097766
- NN 0250701 : 1*20 ampoules
- NN 0306806 : 1*60 ampoules
- NN 0306823 : 2*60 ampoules
10. DATE DE MISE A JOUR DU TEXTE : 24/11/2023
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 1404920 | COMBIVENT VIAL MONODOSE 20X2,5ML | R03AL02 | € 12,36 | - | Oui | € 2,31 | € 1,39 |
| 1688951 | COMBIVENT MONODOSE VIAL 60X2,5ML | R03AL02 | € 22,08 | - | Oui | € 5,6 | € 3,36 |