![]() Ce médicament fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de la santé déclarent tout effet indésirable suspecté. Voir rubrique 4.8 pour les modalités de déclaration des effets indésirables.
Ce médicament fait l'objet d'une surveillance supplémentaire qui permettra l'identification rapide de nouvelles informations relatives à la sécurité. Les professionnels de la santé déclarent tout effet indésirable suspecté. Voir rubrique 4.8 pour les modalités de déclaration des effets indésirables.
1. DÉNOMINATION DU MÉDICAMENT
SOTYKTU 6 mg comprimés pelliculés
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque comprimé pelliculé contient 6 mg de deucravacitinib.
Excipient à effet notoire:
Chaque comprimé pelliculé contient 44 mg de lactose (voir rubrique 4.4).
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Comprimé pelliculé (comprimé)
Comprimé pelliculé rose, rond, biconvexe, de 8 mm de diamètre, portant les mentions « BMS 895 » et « 6 mg » gravées sur une face sur deux lignes, l’autre face étant lisse.
4. INFORMATIONS CLINIQUES
4.1 Indications thérapeutiques
SOTYKTU est indiqué dans le traitement du psoriasis en plaques modéré à sévère chez les adultes éligibles à un traitement systémique.
4.2 Posologie et mode d’administration
Le traitement doit être initié sous la conduite et la surveillance d'un médecin expérimenté dans le diagnostic et le traitement du psoriasis.
Posologie
La dose recommandée est de 6 mg par voie orale une fois par jour.
En l'absence de signes de bénéfice thérapeutique après 24 semaines, l’arrêt du traitement doit être envisagé. La réponse du patient au traitement doit être évaluée régulièrement.
Populations particulières
Personnes âgées
Aucune adaptation posologique n’est nécessaire chez les patients âgés de 65 ans et plus (voir rubrique 5.2). L’expérience clinique chez les patients de 75 ans ou plus est très limitée et le deucravacitinib doit être utilisé avec précaution dans ce groupe de patients.
Insuffisance rénale
Aucune adaptation posologique n’est nécessaire chez les patients insuffisants rénaux, y compris chez les patients dialysés présentant une insuffisance rénale terminale (voir rubrique 5.2).
Insuffisance hépatique
Aucune adaptation posologique n’est nécessaire chez les patients présentant une insuffisance hépatique légère à modérée. Il n’est pas recommandé d’utiliser deucravacitinib chez les patients présentant une insuffisance hépatique sévère (voir rubrique 5.2).
Population pédiatrique
La sécurité d’emploi et l’efficacité du deucravacitinib chez les enfants et les adolescents âgés de moins de 18 ans n’ont pas encore été établies. Aucune donnée n’est disponible.
Mode d’administration
Voie orale.
Les comprimés peuvent être pris pendant ou en dehors des repas. Les comprimés doivent être avalés entiers et ne doivent pas être écrasés, coupés ou mâchés.
4.3 Contre‑indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
Infections actives cliniquement importantes (par exemple : tuberculose active, voir rubrique 4.4).
4.8 Effets indésirables
Résumé du profil de sécurité
L’effet indésirable le plus fréquemment rapporté est les infections des voies aériennes supérieures (18,9 %), le plus souvent une rhinopharyngite. Le profil de sécurité du deucravacitinib à plus long terme était similaire et cohérent avec les études de développement.
Liste tabulée des effets indésirables
La liste des effets indésirables suivante pour deucravacitinib provient d'études cliniques sur le psoriasis en plaques (Tableau 1). Ces effets sont présentés par classe de systèmes d’organes MedDRA et par fréquence.
Les fréquences sont définies comme suit : très fréquent (≥ 1/10) ; fréquent (≥ 1/100, < 1/10) ; peu fréquent (≥ 1/1 000, < 1/100) ; rare (≥ 1/10 000, < 1/1 000) ; très rare (< 1/10 000) ; fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Tableau 1 : Liste des effets indésirables
Classe de systèmes d’organes | Fréquence | Effet indésirable |
Infections et infestations | Très fréquent | Infections des voies aériennes supérieuresa |
Fréquent | Infections par le virus de l’herpèsb | |
Peu fréquent | Zona | |
Affections gastro‑intestinales | Fréquent | Ulcères buccauxc |
Affections de la peau et du tissu sous‑cutané | Fréquent | Rash acnéiformed |
Investigations | Fréquent | Créatine phosphokinase sanguine augmentée |
a Les infections des voies aériennes supérieures comprennent la rhinopharyngite, l’infection des voies aériennes supérieures, l’infection virale des voies aériennes supérieures, la pharyngite, la sinusite, la sinusite aiguë, la rhinite, l'amygdalite, l’abcès périamygdalien, la laryngite, la trachéite et la rhinotrachéite. | ||
Description de certains effets indésirables
Infections
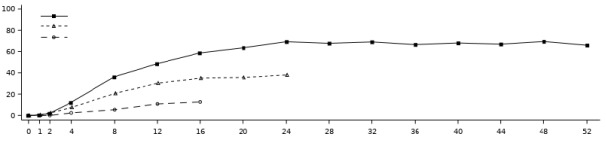
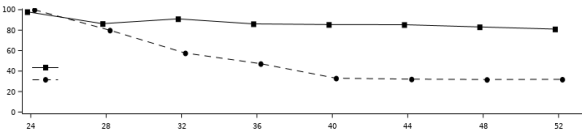
Dans les études POETYK PSO‑1 et POETYK PSO‑2 (voir rubrique 5.1), des infections sont survenues chez 29,1 % des patients traités par deucravacitinib (116,0 événements pour 100 personnes‑années) contre 21,5 % des patients traités par le placebo (83,7 événements pour 100 personnes‑années) au cours des 16 premières semaines. La majorité des infections étaient sans gravité, d’intensité légère à modérée et n’ont pas entraîné d’arrêt du traitement par deucravacitinib. L’incidence des infections graves chez les patients traités par deucravacitinib était de 0,6 % (2,0 événements pour 100 personnes‑années) et de 0,5 % chez les patients traités par le placebo (1,6 événement pour 100 personnes‑années).
Le taux d’infections chez les patients traités par deucravacitinib n’a pas augmenté jusqu’à la semaine 52 (95,4 événements pour 100 personnes‑années). Le taux d’infections graves chez les patients traités par deucravacitinib n’a pas augmenté jusqu’à la semaine 52 (1,7 événement pour 100 personnes‑années).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration – voir Annexe V.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHÉ
Bristol-Myers Squibb Pharma EEIG
Plaza 254
Blanchardstown Corporate Park 2
Dublin 15, D15 T867
Irlande
8. NUMÉRO(S) D’AUTORISATION DE MISE SUR LE MARCHÉ
EU/1/23/1718/001
EU/1/23/1718/002
EU/1/23/1718/003
EU/1/23/1718/004
EU/1/23/1718/005
EU/1/23/1718/006
EU/1/23/1718/007
EU/1/23/1718/008
10. DATE DE MISE À JOUR DU TEXTE
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’Agence européenne des médicaments http://www.ema.europa.eu.
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 4697421 | SOTYKTU 6 mg 28 comprimés pelliculés | € 723,51 | - | Oui | € 12,8 | € 8,5 |