ANNEXE I
RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
1. DÉNOMINATION DU MÉDICAMENT
Ilumetri 100 mg, solution injectable en seringue préremplie
Ilumetri 200 mg, solution injectable en seringue préremplie
Ilumetri 100 mg, solution injectable en stylo prérempli
Ilumetri 200 mg, solution injectable en stylo prérempli
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Ilumetri 100 mg, solution injectable en seringue préremplie
Chaque seringue préremplie contient 100 mg de tildrakizumab dans 1 mL.
Ilumetri 200 mg, solution injectable en seringue préremplie
Chaque seringue préremplie contient 200 mg de tildrakizumab dans 2 mL.
Ilumetri 100 mg, solution injectable en stylo prérempli
Chaque stylo prérempli contient 100 mg de tildrakizumab dans 1 mL.
Ilumetri 200 mg, solution injectable en stylo prérempli
Chaque stylo prérempli contient 200 mg de tildrakizumab dans 2 mL.
Le tildrakizumab est un anticorps monoclonal humanisé de classe IgG1/k produit par des cellules ovariennes de hamster chinois (CHO) par la technique de l'ADN recombinant.
Pour la liste complète des excipients, voir rubrique 6.1.
Excipient à effet notoire
Chaque seringue préremplie d’Ilumetri 100 mg solution injectable contient 0,5 mg de polysorbate 80 (E 433).
Chaque seringue préremplie d’Ilumetri 200 mg solution injectable contient 1 mg de polysorbate 80 (E 433).
Chaque stylo prérempli d’Ilumetri 100 mg solution injectable contient 0,5 mg de polysorbate 80 (E 433).
Chaque stylo prérempli d’Ilumetri 200 mg solution injectable contient 1 mg de polysorbate 80 (E 433)
3. FORME PHARMACEUTIQUE
Solution injectable
La solution est limpide à légèrement opalescente, incolore à jaune pâle. Le pH de la solution est compris entre 5,7 et 6,3 et son osmolalité se situe entre 258 et 311 mOsm/kg.
4. INFORMATIONS CLINIQUES
4.1 Indications thérapeutiques
Ilumetri est indiqué dans le traitement du psoriasis en plaques modéré à sévère chez l’adulte qui nécessite un traitement systémique.
4.2 Posologie et mode d’administration
Ce médicament est destiné à être utilisé sous la conduite et la surveillance d’un médecin expérimenté dans le diagnostic et le traitement du psoriasis en plaques.
Posologie
La dose recommandée est de 100 mg administrée par injection sous-cutanée, administrée aux semaines 0 et 4, puis toutes les 12 semaines.
À la discrétion du médecin, chez les patients présentant une charge de morbidité élevée ou chez ceux dont le poids corporel est supérieur à 90 kg, une dose de 200 mg d'Ilumetri peut apporter une plus grande efficacité.
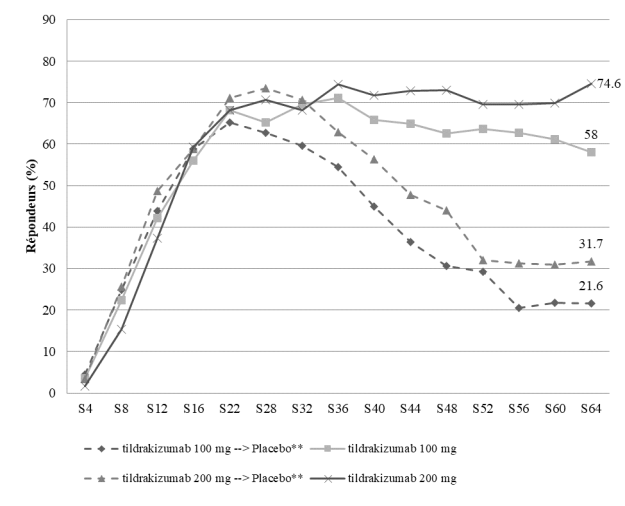
L’arrêt du traitement doit être envisagé chez les patients ne présentant pas de réponse après 28 semaines de traitement. Certains patients présentant une réponse partielle en début de traitement, peuvent obtenir une amélioration en poursuivant le traitement au-delà de 28 semaines.
Dose oubliée
En cas d’oubli d’une dose, celle-ci doit être administrée dès que possible. L’administration doit ensuite reprendre selon le schéma habituel prévu.
Populations particulières
Personnes âgées
Aucun ajustement posologique n’est nécessaire (voir rubrique 5.2).
Insuffisance rénale ou hépatique
Ilumetri n’a pas été étudié chez ces populations de patients. Aucune recommandation posologique ne peut être donnée. Pour plus d’informations sur l’élimination du tildrakizumab, voir rubrique 5.2.
Population pédiatrique
La sécurité et l’efficacité d’Ilumetri chez les enfants et les adolescents âgés de moins de 18 ans n’ont pas encore été établies. Aucune donnée n’est disponible.
Mode d’administration
Ce médicament est administré par injection sous-cutanée. Les sites d’injection doivent être alternés. Ilumetri ne doit pas être injecté dans des zones où la peau est atteinte de psoriasis en plaques ou est sensible au toucher, présente un hématome, est rouge, indurée, épaissie ou squameuse. La seringue ou le stylo ne doit pas être agité. Chaque seringue ou stylo est exclusivement à usage unique.
Après une formation adaptée à la technique d’injection sous-cutanée, les patients peuvent s’injecter eux-mêmes Ilumetri si un médecin estime cela approprié. Toutefois, le médecin doit assurer un suivi médical adéquat des patients. Les patients doivent être informés de la nécessité d’injecter la dose complète de tildrakizumab, conformément aux instructions figurant dans la notice. Des instructions détaillées concernant l’administration sont fournies dans la notice.
4.3 Contre-indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
Infection évolutive et cliniquement grave, par exemple, tuberculose active (voir rubrique 4.4).
4.8 Effets indésirables
Résumé du profil de sécurité
Les effets indésirables les plus fréquemment rapportés sont : infections des voies respiratoires supérieures (12,6 %), céphalées (4,0 %), diarrhée (1,6 %), gastroentérite (1,5 %), dorsalgie (1,5 %), nausées (1,3 %) et douleur au site d’injection (1,3 %).
Tableau récapitulatif des effets indésirables
Les effets indésirables des études cliniques (Tableau 1) sont présentés par classe de systèmes d’organes (SOC) selon la classification MedDRA et par fréquence, selon la convention suivante : très fréquent (≥ 1/10) ; fréquent (≥ 1/100, < 1/10) ; peu fréquent (≥ 1/1 000, < 1/100) ; rare (≥ 1/10 000, < 1/1 000) ; très rare (< 1/10 000) et fréquence indéterminée (ne peut être estimée sur la base des données disponibles). Dans chaque groupe de fréquence, les effets indésirables sont présentés par ordre décroissant de gravité.
Tableau 1. Liste des effets indésirables
Classe de systèmes d’organes MedDRA | Terme préconisé | Catégorie de fréquence |
Infections et infestations | Infections des voies respiratoires supérieuresa | Très fréquent |
Affections du système nerveux | Céphalées | Fréquent |
Affections gastro-intestinales | Gastroentérite | Fréquent |
Diarrhée | Fréquent | |
Nausées | Fréquent | |
Troubles généraux et anomalies au site d’administration | Dorsalgie | Fréquent |
Douleur au site d’injection | Fréquent |
a y compris rhinopharyngite
Sécurité d’emploi à long terme
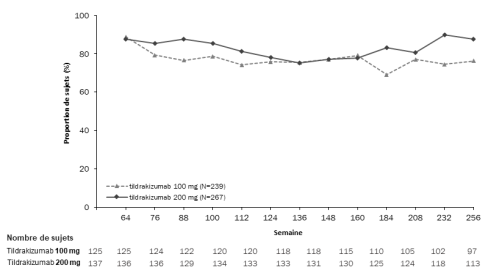
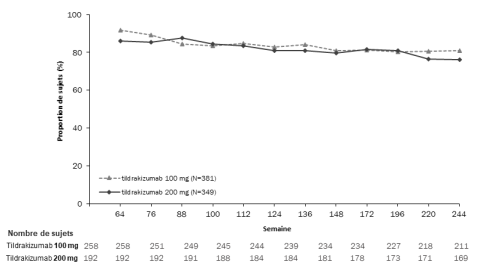
Le profil de sécurité du tildrakizumab observé pendant les périodes d’extension à long terme de reSURFACE 1 et reSURFACE 2 était cohérent avec celui des périodes en double aveugle.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via :
Belgique
l’Agence fédérale des médicaments et des produits de santé, www.afmps.be
Division Vigilance:
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHÉ
Almirall, S.A.
Ronda General Mitre, 151
08022 Barcelona
Espagne
8. NUMÉROS D’AUTORISATION DE MISE SUR LE MARCHÉ
EU/1/18/1323/001
EU/1/18/1323/002
EU/1/18/1323/003
EU/1/18/1323/004
EU/1/18/1323/005
10. DATE DE MISE À JOUR DU TEXTE
06/2024
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’Agence européenne des médicaments https://www.ema.europa.eu.
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 4166740 | ILUMETRI 100MG SOL INJ SERINGUE PREREMPLIE 1X1ML | L04AC17 | € 2817,11 | - | Oui | € 12,8 | € 8,5 |
| 4575163 | ILUMETRI 200MG SOL INJ SERINGUE PREREMPLIE 1X2ML | € 2817,11 | - | Oui | € 12,8 | € 8,5 | |
| 4800777 | ILUMETRI 100MG SOL INJ STYLO PREREMPLI 1X1ML | € 2817,11 | - | Oui | € 12,8 | € 8,5 |