RESUME DES CARACTERISTIQUES DU PRODUIT
1. DENOMINATION DU MEDICAMENT
ZOLADEX, 3,6 mg, implant
ZOLADEX Long Acting, 10,8 mg, implant
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
ZOLADEX contient de l’acétate de goséréline équivalent à 3,6 mg de peptide base.
ZOLADEX Long Acting contient de l’acétate de goséréline équivalent à 10,8 mg de peptide base.
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Implant.
4. DONNEES CLINIQUES
4.1 Indications thérapeutiques
ZOLADEX
1) Traitement hormonal palliatif du cancer avancé de la prostate (stades III et IV).
2) Diminution de la taille de la tumeur en vue d’une prostato-vésiculectomie totale radicale curative (stades T2N1-2M0 et T3N0-2M0 ou B2-C).
3) Traitement du cancer du sein avancé et traitement alternatif à une chimiothérapie adjuvante en cas de cancer du sein au stade précoce chez des femmes pré- et périménopausées susceptibles de bénéficier d’un traitement hormonal. On n’a pas encore démontré le bénéfice d’une castration induite par des analogues de la LHRH pendant ou après une chimiothérapie.
4) Traitement de l’endométriose. ZOLADEX permet de juguler les symptômes y compris la douleur. ZOLADEX réduit le nombre et les dimensions des foyers d’endométriose. La durée du traitement est de 6 mois maximum.
5) Traitement des fibromes utérins. ZOLADEX fait régresser la taille des tumeurs, favorise l’amélioration de l’état anémique et soulage les symptômes y compris la douleur. ZOLADEX peut être administré au cours de la période précédant une intervention chirurgicale ; ZOLADEX peut ainsi simplifier la technique opératoire et limiter les hémorragies. La durée du traitement est de 3 mois maximum.
6) Réduction de la taille de l’endomètre : en vue de la préparation d’une ablation de l’endomètre, ZOLADEX réduit celui-ci, ce qui augmenterait l’efficacité de la résection endométriale et faciliterait l’examen endoscopique. Néanmoins, le traitement peut accroître la résistance face à la dilatation du col. La prudence est donc de mise lors de la dilatation du col.
ZOLADEX Long Acting
1) Traitement hormonal palliatif du cancer avancé de la prostate (stades III et IV).
2) Diminution de la taille de la tumeur en vue d’une prostato-vésiculectomie totale radicale curative (stades T2N1-2M0 et T3N0-2M0 ou B2-C).
3) Traitement de l’endométriose. ZOLADEX Long Acting permet de juguler les symptômes y compris la douleur. ZOLADEX Long Acting réduit le nombre et les dimensions des foyers d’endométriose.
4) Traitement des fibromes utérins. ZOLADEX Long Acting fait régresser la taille des tumeurs, favorise l’amélioration de l’état anémique et soulage les symptômes y compris la douleur. ZOLADEX Long Acting peut être administré au cours de la période précédant une intervention chirurgicale ; ZOLADEX Long Acting peut ainsi simplifier la technique opératoire et limiter les hémorragies.
4.2 Posologie et mode d’administration
Il faut être prudent lors de l’injection de ZOLADEX/ZOLADEX Long Acting dans la paroi abdominale antérieure, du fait de la proximité de l’artère épigastrique inférieure sous-jacente et de ses branches.
Il faut redoubler de prudence lors de l’administration de ZOLADEX/ZOLADEX Long Acting chez les patients qui ont un IMC bas et/ou qui reçoivent un traitement anticoagulant complet (voir rubrique 4.4).
Afin d’utiliser correctement ZOLADEX/ZOLADEX Long Acting, veuillez consulter les instructions sur la pochette et à la fin de ce RCP.
A utiliser uniquement si l’emballage est intact. Administrer immédiatement après ouverture de l’emballage.
- Chez les patients présentant une insuffisance rénale ou hépatique, aucune adaptation de la posologie ne s’impose.
- Population pédiatrique
L’utilisation de ZOLADEX ou de ZOLADEX Long Acting chez l’enfant n’est pas indiquée.
- L’utilisation d’un anesthésique local est permise mais dans la plupart des cas, elle n’est pas nécessaire.
ZOLADEX (hommes et femmes)
Adultes (y compris les personnes âgées)
- Une injection sous-cutanée dans la paroi abdominale antérieure d’un implant de ZOLADEX tous les 28 jours.
Endométriose :
L'endométriose doit être traitée pendant une période de 6 mois seulement, puisqu’à l'heure actuelle il n'existe pas de données cliniques pour des périodes de traitement plus longs. Un traitement répété ne devrait pas être donné en raison des inquiétudes sur la perte de densité minérale osseuse. Chez les patients traités par la goséréline pour une endométriose, il a été montré que l'ajout d'une hormonothérapie substitutive (un agent œstrogènique quotidien et un agent progestatif) réduit la perte de densité minérale osseuse ainsi que les symptômes vasomoteurs.
Réduction endométriale :
- Dans l’indication de réduction endométriale, 2 implants de ZOLADEX doivent être administrés avec un intervalle de 28 jours. L’intervention chirurgicale doit avoir lieu dans les deux semaines suivant l’administration du deuxième implant de ZOLADEX.
- Traitement de quatre ou huit semaines. Un second implant peut être exigé pour une patiente avec un utérus large ou pour permettre un calendrier chirurgical flexible.
Fibromes utérins :
Pour les femmes qui sont anémiques à la suite de fibromes utérins : l’implant de ZOLADEX avec un supplément de fer peut être administré jusqu'à trois mois avant la chirurgie.
ZOLADEX Long Acting
Hommes adultes (y compris les hommes âgés)
Une injection sous-cutanée dans la paroi abdominale antérieure d’un implant de ZOLADEX Long Acting tous les 3 mois.
Femmes adultes (y compris les femmes âgées)
Une injection sous-cutanée dans la paroi abdominale antérieure d’un implant de ZOLADEX Long Acting toutes les 12 semaines.
4.3 Contre-indications
- Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
- Grossesse et allaitement (voir rubrique 4.6 Fertilité, grossesse et allaitement).
4.8 Effets indésirables
Les catégories de fréquences suivantes sont basées sur tous les effets indésirables provenant des études cliniques, des études après commercialisation et des rapports spontanés. Les effets indésirables les plus fréquemment observés incluent bouffées de chaleur, transpiration et réactions au site d’injection.
La convention suivante est utilisée pour la classification de la fréquence : très fréquent (≥ 1/10), fréquent (≥ 1/100 à < 1/10), peu fréquent (≥ 1/1 000 à < 1/100), rare (≥ 1/10 000 à < 1/1 000), et très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Tableau : Effets indésirables de ZOLADEX et ZOLADEX Long Acting présentés par classe de système d’organe MedDRA
Classe de système d’organe | Fréquence | Hommes | Femmes |
Tumeurs bénignes, malignes et non précisées (incl. kystes et polypes) | Très rare | Tumeur de l’hypophyse | Tumeur de l’hypophyse |
Fréquence indéterminée | ND | Dégénérescence des fibromes utérins (chez les femmes ayant des fibromes utérins) | |
Affections du système immunitaire | Peu fréquent | Hypersensibilité au produit | Hypersensibilité au produit |
Rare | Réaction anaphylactique | Réaction anaphylactique | |
Affections endocriniennes | Très rare | Hémorragie pituitaire | Hémorragie pituitaire |
Troubles du métabolisme et de la nutrition | Fréquent | Diminution de la tolérance au glucose a | ND |
| Peu fréquent | ND | Hypercalcémie (uniquement avec ZOLADEX) |
Affections psychiatriques | Très fréquent | Diminution de la libido b | Diminution de la libido b |
Fréquent | Modifications de l’humeur, dépression | Modifications de l’humeur, dépression | |
Très rare | Troubles psychotiques | Troubles psychotiques | |
Affections cardiaques | Fréquent | Insuffisance cardiaque f | ND |
Fréquence indéterminée | Allongement du QT (voir rubriques 4.4 et 4.5) | Allongement du QT (voir rubriques 4.4 et 4.5) | |
Affections du système nerveux | Fréquent | Paresthésies | Paresthésies |
Compression de la moelle épinière | ND | ||
ND | Céphalées | ||
Insomnies | Insomnies | ||
Affections vasculaires | Très fréquent | Bouffées de chaleur b | Bouffées de chaleur b |
Fréquent | Pression artérielle anormale c | Pression artérielle anormale c | |
Affections de la peau et du tissu sous-cutané | Très fréquent | Hyperhydrose b | Hyperhydrose b, acné i |
Fréquent | Rash d | Rash d, alopécie g | |
Fréquence indéterminée | Alopécie h | (voir fréquent) | |
Affections musculo-squelettiques et systémiques | Fréquent | Douleurs osseuses e | ND |
(voir peu fréquent) | Arthralgie | ||
Peu fréquent | Arthralgie | (voir fréquent) | |
Affections du rein et des voies urinaires | Peu fréquent | Obstruction de l’uretère | ND |
Affections des organes de reproduction et du sein | Très fréquent | Dysfonctionnement érectile | ND |
ND | Sécheresse vulvo-vaginale | ||
ND | Augmentation de la taille des seins | ||
Fréquent | Gynécomastie | ND | |
Peu fréquent | Sensibilité de la poitrine | ND | |
Rare | ND | Kyste ovarien | |
Fréquence indéterminée | ND | Hémorragie de privation (voir rubrique 4.4) | |
Troubles généraux et anomalies au site d’administration | Très fréquent | (voir fréquent) | Réactions sur le site d’injection |
Fréquent | Réactions sur le site d’injection | (voir très fréquent) | |
ND | Augmentation du volume tumoral (tumor flare), tumeur douloureuse | ||
Investigations | Fréquent | Diminution de la densité osseuse (voir rubrique 4.4), augmentation du poids | Diminution de la densité osseuse (voir rubrique 4.4), augmentation du poids |
a Une diminution de la tolérance au glucose a été observée chez les hommes recevant des agonistes de la LHRH. Elle peut se manifester sous la forme d’un diabète ou, chez les patients ayant déjà un diabète sucré, par une perte de la maîtrise de la glycémie.
b Ce sont des effets pharmacologiques qui ne nécessitent que rarement l’arrêt du traitement. Une hyperhydrose et des bouffées de chaleur peuvent se poursuivre après l’arrêt de ZOLADEX.
c Peuvent se manifester sous forme d’une hypotension ou d’une hypertension et ont parfois été observées chez les patients ayant reçu de la goséréline. Ces modifications sont habituellement transitoires, disparaissant pendant le traitement ou après l’arrêt du traitement par la goséréline. Dans de rares cas, ces modifications ont été suffisamment importantes pour nécessiter une intervention médicale, notamment l’arrêt du traitement par la goséréline.
d Généralement léger, régressant souvent sans nécessiter l’arrêt du traitement.
e Initialement, les patients atteints de cancer de la prostate pourront ressentir une augmentation temporaire des douleurs osseuses pouvant être prise en charge par un traitement symptomatique.
f Observé lors d’une étude pharmaco-épidémiologique des agonistes de la LHRH utilisés dans le traitement du cancer de la prostate. Le risque semble augmenter lorsqu’utilisé en association avec des anti-androgènes.
g Une chute de cheveux a été rapportée chez les femmes, y compris les patientes plus jeunes traitées pour des affections bénignes. Cela est généralement faible mais occasionnellement peut être grave.
h En particulier la perte de poils sur le corps, un effet attendu des taux d’androgènes diminués.
i Dans la plupart des cas, l’acné a été rapportée dans le mois qui suit le début du traitement avec ZOLADEX.
ND : Non déterminé
Expérience après commercialisation
Un petit nombre de cas de modification de la numération globulaire, de dysfonction hépatique, d’embolie pulmonaire et de pneumonie interstitielle ont été rapportés en relation avec l’administration de goséréline.
Rarement, certaines femmes entrent en ménopause pendant le traitement par les analogues de la LHRH et leurs règles ne reviennent pas à l’arrêt du traitement. On ne sait pas s’il s’agit d’un effet du traitement par la goséréline ou d’une conséquence de leurs troubles gynécologiques.
ZOLADEX
De plus, les réactions indésirables médicamenteuses suivantes ont été rapportées chez des femmes traitées pour des indications gynécologiques bénignes :
Acné, modification de la pilosité, sécheresse cutanée, prise de poids, augmentation du cholestérol sérique, syndrome d’hyperstimulation ovarienne (en cas d’utilisation concomitante avec des gonadotrophines), vaginite, écoulement vaginal, nervosité, troubles du sommeil, fatigue, œdème périphérique, myalgies, crampes dans les mollets, nausées, vomissements, diarrhées, constipation, douleurs abdominales, modifications de la voix.
Initialement, les patientes atteintes d’un cancer du sein pourront ressentir une intensification temporaire des signes et des symptômes pouvant être pris en charge par un traitement symptomatique.
Rarement, des patientes atteintes de cancer du sein métastasé ont développé une hypercalcémie lors de l’instauration du traitement. En présence de symptômes indiquant une hypercalcémie (par ex. soif), celle-ci devra être exclue.
ZOLADEX Long Acting
Un petit nombre de cas d’hypercalcémie ont été rapportés chez des femmes traitées pour une endométriose et/ou des fibromes. En présence de symptômes indiquant une hypercalcémie (par ex. soif), celle-ci devra être exclue.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration – voir détails ci-dessous.
Belgique
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance :
Site internet : www.notifieruneffetindesirable.be
e-mail : adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
AstraZeneca nv/sa
Alfons Gossetlaan 40 boîte 201
1702 Groot-Bijgaarden
Belgique
Tél. +32 (0)2/370 48 11
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
BE:
ZOLADEX: BE138731
ZOLADEX Long Acting: BE179277
LU :
ZOLADEX : 2007109481
ZOLADEX Long Acting : 2007109482
N° nationaux :
ZOLADEX :0141818
ZOLADEX Long Acting :0216841
10. DATE DE MISE A JOUR DU TEXTE
11-2024
Les informations suivantes sont destinées exclusivement aux professionnels de la santé:
ZOLADEX/ZOLADEX Long Acting est administré par injection sous-cutanée – Veuillez lire complètement et comprendre toutes les instructions avant l’administration
- Placez le patient dans une position confortable avec la partie supérieure du corps légèrement surélevée.
Préparez le site d’injection en suivant les directives et procédures locales.
REMARQUE : Il faut être prudent lors de l’injection de ZOLADEX/ZOLADEX Long Acting dans la paroi abdominale antérieure, du fait de la proximité de l’artère épigastrique inférieure sous-jacente et de ses branches ; le risque de lésions vasculaires est plus important chez les patients très minces.
- Examinez la pochette et la seringue afin de vérifier qu’elles ne soient pas endommagées. Retirez la seringue de la pochette ouverte et tenez la seringue légèrement inclinée en face de la lumière.
Vérifiez qu’au moins une partie de l’implant ZOLADEX/ZOLADEX Long Acting soit visible (Figure 1).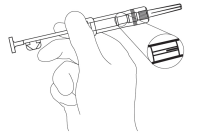 Figure 1
Figure 1
- Saisissez la languette de sécurité en plastique, détachez-la de la seringue, et jetez-la. (Figure 2). Enlevez le protège-aiguille. Contrairement aux injections de liquide, il n’est pas nécessaire d’éliminer les bulles d’air car des tentatives en ce sens risquent de déplacer l’implant de ZOLADEX/ZOLADEX Long Acting.
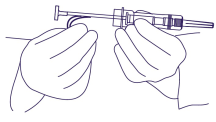 Figure 2
Figure 2
- Il faut tenir la seringue au niveau du manchon de protection en utilisant une technique aseptique, pincer la peau du patient et insérer l’aiguille selon une légère inclination (30 à 45 degrés) dans la peau. Introduisez l’aiguille le biseau tourné vers le haut dans le tissu sous-cutané de la paroi abdominale antérieure, sous la ligne ombilicale, jusqu’à ce que le manchon de protection entre en contact avec la peau du patient. (Figure 3).
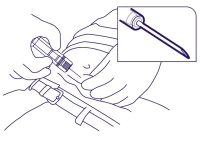 Figure 3
Figure 3
REMARQUE : la seringue de ZOLADEX/ZOLADEX Long Acting ne peut pas être utilisée pour l’aspiration. Si l’aiguille hypodermique pénètre dans un gros vaisseau, le sang sera immédiatement visible dans la chambre de la seringue. Si un vaisseau est percé, retirez l’aiguille et contrôlez immédiatement tout saignement, en surveillant tout signe ou symptôme d’hémorragie abdominale. Après s’être assuré que le patient soit hémodynamiquement stable, un autre implant de ZOLADEX/ZOLADEX Long Acting peut être injecté avec une nouvelle seringue à un autre endroit.
Il faut redoubler de prudence lors de l’administration de ZOLADEX/ZOLADEX Long Acting chez les patients ayant un faible IMC et/ou chez des patients recevant un traitement anticoagulant complet.
- N’enfoncez pas dans le muscle ou le péritoine. La figure ci-dessous représente une mauvaise manipulation (angle et prise de la seringue). (Figure 4)
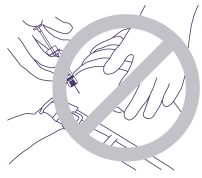 Figure 4
Figure 4
- Enfoncez complètement le piston, jusqu’à ce que vous ne puissiez plus aller plus loin, afin de libérer l’implant de ZOLADEX/ZOLADEX Long Acting et d’activer le mécanisme de protection. Vous pouvez entendre un “clic” et vous sentirez que le mécanisme de protection se déplace automatiquement pour couvrir l’aiguille. Si le piston n’est pas enfoncé complètement, le mécanisme de protection ne sera PAS activé.
REMARQUE : l’aiguille ne se rétracte pas.
- Tenez la seringue comme illustré sur la figure 5, retirez l’aiguille de telle sorte que le manchon de protection puisse glisser davantage sur l’aiguille. Eliminez la seringue dans un récipient adéquat pour objets tranchants.
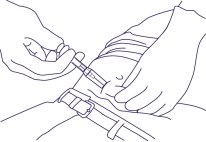 Figure 5
Figure 5
REMARQUE : dans l’éventualité peu probable de la nécessité de devoir retirer chirurgicalement un implant de ZOLADEX/ZOLADEX Long Acting, il peut être localisé par ultrasons.
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 0603159 | ZOLADEX SER INJ SC 1X3,6MG | L02AE03 | € 122,11 | - | Oui | € 2 | € 1 |
| 1278480 | ZOLADEX LONG ACTION SER 1X10,8 MG | L02AE03 | € 297,11 | - | Oui | € 2 | € 1 |