1. DENOMINATION DU MEDICAMENT
Levorichter 30, 30 microgrammes/150 microgrammes, comprimés enrobés.
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque comprimé contient 150 microgrammes de lévonorgestrel et 30 microgrammes d’éthinylestradiol.
Excipients à effet notoire : chaque comprimé contient 33 mg de lactose monohydraté et 22,46 mg de saccharose.
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Comprimé enrobé.
Comprimés ronds, biconvexes, blancs.
4. DONNEES CLINIQUES
4.1 Indications thérapeutiques
Contraception orale hormonale.
La décision de prescrire Levorichter 30 doit être prise en tenant compte des facteurs de risque de la patiente, notamment ses facteurs de risque de thrombo-embolie veineuse (TEV), ainsi que du risque de TEV associé à Levorichter 30 en comparaison aux autres CHCs (Contraceptifs Hormonaux Combinés) (voir rubriques 4.3 et 4.4).
4.2 Posologie et mode d’administration
Posologie
Comment prendre Levorichter 30?
Les comprimés doivent être pris par voie orale dans l’ordre indiqué sur la plaquette, à peu près à la même heure tous les jours, avec un peu de liquide si nécessaire.
Prendre un comprimé par jour pendant 21 jours consécutifs. Commencer chaque plaquette suivante après une période de 7 jours sans comprimés au cours de laquelle un saignement se produira généralement. Ce saignement débutera généralement le 2e ou le 3e jour après la prise du dernier comprimé et ne sera peut-être pas fini avant de commencer la plaquette suivante.
Comment débuter la prise de Levorichter 30?
Pas de prise antérieure d’un contraceptif hormonal (au cours du dernier mois)
La prise des comprimés commence le jour 1 du cycle naturel de la femme (= le premier jour de ses règles).
Relais d’un autre contraceptif hormonal de type combiné (contraceptifs oraux combinés (COC), anneau vaginal, dispositif transdermique)
Prendre le premier comprimé le jour suivant la dose du dernier comprimé actif du contraceptif précédent ou, au plus tard, le jour suivant la période habituelle d’arrêt de prise des comprimés.
En cas d’utilisation d’un anneau vaginal ou d’un dispositif transdermique, prendre le premier comprimé le jour même du retrait de l’anneau vaginal ou du patch transdermique, ou au plus tard le jour où la pose suivante était prévue.
Relais de produits contenant uniquement un progestatif (minipilule, injection, implant ou un dispositif intra-utérin libérant un progestatif (SIU))
Le passage d’une minipilule seule peut se faire à tout moment pendant le cycle et la prise du comprimé enrobé de Levorichter 30 doit commencer le jour suivant l’arrêt.
Le passage d’un implant ou d’un SIU doit se faire le jour du retrait du dispositif et, pour un contraceptif injectable, le jour prévu pour la nouvelle injection.
Dans tous les cas, l’utilisation d’une méthode contraceptive complémentaire est recommandée pendant les 7 premiers jours du traitement.
Après un avortement/fausse-couche au 1er trimestre
La femme peut commencer à prendre les comprimés immédiatement. Dans ce cas, il ne sera pas nécessaire de prendre des mesures contraceptives complémentaires.
Après un accouchement ou un avortement/fausse-couche au 2e trimestre
Il sera recommandé à la femme qui n’allaite pas de commencer entre 21 et 28 jours après un accouchement ou un avortement au 2e trimestre, compte tenu du risque accru de thromboembolie durant la période postpartum. Si elle commence plus tard, il lui sera recommandé d’utiliser simultanément une méthode contraceptive de type barrière pendant les 7 premiers jours de prise des comprimés. Cependant, si elle a déjà eu des rapports sexuels, une grossesse doit être exclue avant de commencer à prendre les comprimés ou bien elle devra attendre ses premières règles.
En cas d’allaitement
Voir rubrique 4.6.
Oubli de comprimés
L’efficacité contraceptive peut être réduite en cas d’oubli d’une dose, surtout si la dose est oubliée pendant >12 heures.
En cas d’oubli de prendre un comprimé pendant moins de 12 heures, l’efficacité contraceptive n’est pas réduite. La femme doit prendre le comprimé dès qu’elle y pense et les comprimés restants seront pris à l’heure habituelle.
En cas d’oubli de prendre un comprimé pendant plus de 12 heures, l’efficacité contraceptive peut être réduite. Les deux règles de base suivantes s’appliquent en cas d’oubli de comprimés :
- La prise des comprimés ne doit jamais être interrompue pendant plus de 7 jours.
- La prise ininterrompue de comprimés pendant 7 jours est requise pour maintenir une suppression suffisante de l’axe hypothalamo-hypophyso-ovarien.
Les conseils suivants seront donc donnés en pratique :
Semaine 1 :
La femme prendra le dernier comprimé oublié dès qu’elle y pense, même si cela veut dire qu’elle doit prendre 2 comprimés en même temps. Elle continuera ensuite à prendre les comprimés à l’heure habituelle.
Elle devra aussi utiliser simultanément une méthode contraceptive de type barrière (ex. un préservatif) pendant les 7 jours suivants. En cas de rapports sexuels au cours des 7 jours qui précèdent, la possibilité d’une grossesse doit être envisagée. Plus le nombre de comprimés oubliés est élevé et l’oubli proche de la période normale sans comprimés, plus le risque de grossesse sera élevé.
Semaine 2 :
La femme prendra le dernier comprimé oublié dès qu’elle y pense, même si cela veut dire qu’elle doit prendre 2 comprimés en même temps. Elle continuera ensuite à prendre les comprimés à l’heure habituelle.
Si les comprimés ont été pris correctement les 7 jours qui précèdent le comprimé oublié, il ne sera pas nécessaire de prendre des mesures contraceptives complémentaires. Toutefois, dans la négative ou si plusieurs comprimés sont oubliés, il sera recommandé à la femme d’utiliser une barrière mécanique supplémentaire (par ex. un préservatif) pendant 7 jours.
Semaine 3 :
Le risque de réduction de la fiabilité est imminent en raison de l’intervalle sans comprimés à venir. Toutefois il est possible d’empêcher la réduction de l’efficacité contraceptive en modulant la prise de comprimés. Il ne sera donc pas nécessaire de prendre des mesures contraceptives complémentaires si l’on suit l’une des alternatives ci-dessous, à condition que tous les comprimés aient été pris correctement pendant les 7 jours qui précèdent le comprimé oublié. Toutefois, dans la négative, il sera recommandé à la femme de suivre la première des deux alternatives et d’utiliser simultanément une méthode contraceptive de type barrière supplémentaire (par ex. un préservatif) pendant les 7 jours suivants.
- La femme prendra le dernier comprimé oublié dès qu’elle y pense, même si cela veut dire qu’elle doit prendre 2 comprimés en même temps. Elle continuera ensuite à prendre les comprimés à l’heure habituelle. Elle commencera la plaquette suivante immédiatement après avoir pris le dernier comprimé de la plaquette en cours, c-à-d qu’il n’y aura pas d’interruption entre les plaquettes. L’apparition d’hémorragies de privation avant la fin de la deuxième plaquette est peu probable mais un spotting ou des hémorragies utérines secondaires sont possibles les jours de prise des comprimés.
- Il pourra aussi être conseillé à la femme d’arrêter de prendre les comprimés de la plaquette en cours. Dans ce cas, elle devra observer une période sans comprimés de 7 jours maximum, y compris les jours où elle a oublié de prendre les comprimés, et continuer ensuite avec la plaquette suivante.
Si la femme a oublié des comprimés et n’a pas d’hémorragies de privation pendant la première période normale sans comprimés, la possibilité d’une grossesse devra être envisagée.
Précautions en cas de troubles gastro-intestinaux
En cas de symptômes gastro-intestinaux sévères (p.ex. vomissements, diarrhée), il est possible que les substances actives n’aient pas été complètement absorbées ; par conséquent, d’autres mesures contraceptives devront être utilisées.
Si des vomissements ou une diarrhée sévère se produisent dans les 3 à 4 heures suivant la prise d’un comprimé, un nouveau comprimé doit être pris en remplacement le plus rapidement possible. Le nouveau comprimé doit être pris, si possible, dans les 12 heures qui suivent l’heure de prise habituelle.
Si plus de 12 heures se sont écoulées, il conviendra de suivre les mêmes instructions que celles données pour l’oubli de comprimés (voir rubrique 4.2).
Si la femme ne veut pas changer sa prise de comprimés habituelle, elle devra prendre le ou les comprimés supplémentaires provenant d’une autre plaquette.
Comment retarder ou avancer les saignements menstruels :
Pour retarder les saignements menstruels, la femme doit continuer avec la plaquette de Levorichter 30 suivante après avoir pris le dernier comprimé de la plaquette actuelle, sans observer de période sans comprimés. Le retardement des règles peut continuer aussi longtemps que désiré jusqu’à la fin de la deuxième plaquette. Pendant cette période, la femme peut avoir des hémorragies secondaires utérines ou un spotting. La prise régulière de Levorichter 30 recommencera après la période habituelle de 7 jours sans comprimés.
Pour avancer ses saignements menstruels afin qu’ils apparaissent un jour de la semaine autre que celui auquel la femme est habituée, il peut lui être conseillé de réduire la période sans comprimés par le nombre de jours désiré. Plus l’arrêt est court, plus le risque est grand de ne pas avoir d’hémorragies de privation et de présenter des petites pertes sanglantes ou du spotting pendant la prise des comprimés de la deuxième plaquette (ce qui est également le cas pour un retardement des règles). Il est important de souligner qu’il ne faut pas prolonger la période sans comprimés.
Population pédiatrique
Il n’y a pas d’utilisation justifiée de Levorichter 30 dans la population avant l’âge pubertaire.
Mode d’administration
Pour administration orale.
4.3 Contre-indications
Les contraceptifs oraux de type combiné (COCs) ne doivent pas être utilisés dans l’une des conditions mentionnées ci-dessous. En cas d’apparition d’une des affections suivantes pour la première fois pendant la prise de COCs, leur utilisation doit cesser immédiatement.
- Présence ou risque de thrombo-embolie veineuse (TEV)
- Thrombo-embolie veineuse – présence de TEV (patient traité par des anticoagulants) ou antécédents de TEV (p. ex. thrombose veineuse profonde [TVP] ou embolie pulmonaire [EP])
- Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie veineuse, telle qu’une résistance à la protéine C activée (PCa) (y compris une mutation du facteur V de Leiden), un déficit en antithrombine III, un déficit en protéine C, un déficit en protéine S
- Intervention chirurgicale majeure avec immobilisation prolongée (voir rubrique 4.4)
- Risque élevé de thrombo-embolie veineuse dû à la présence de multiples facteurs de risque (voir rubrique 4.4)
- Présence ou risque de thrombo-embolie artérielle (TEA)
- Thrombo-embolie artérielle – présence ou antécédents de thrombo-embolie artérielle (p. ex. infarctus du myocarde) ou de prodromes (p. ex. angine de poitrine)
- Affection cérébrovasculaire – présence ou antécédents d’accident vasculaire cérébral (AVC) ou de prodromes (p. ex. accident ischémique transitoire [AIT])
- Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie artérielle, telle qu’une hyperhomocystéinémie ou la présence d’anticorps anti-phospholipides (anticorps anti-cardiolipine, anticoagulant lupique).
- Antécédents de migraine avec signes neurologiques focaux
- Risque élevé de thrombo-embolie artérielle dû à la présence de multiples facteurs de risque (voir rubrique 4.4) ou d’un facteur de risque sévère tel que :
- diabète avec symptômes vasculaires
- hypertension artérielle sévère
- dyslipoprotéinémie sévère
- Affection hépatique sévère, en cours ou passée, tant que les valeurs de la fonction hépatique ne sont pas redevenues normales
- Présence ou antécédents de tumeurs du foie (bénignes ou malignes)
- Tumeur maligne hormono-dépendante avérée ou suspectée (par ex., tumeur au niveau des organes génitaux ou du sein)
- Saignement vaginal non diagnostiqué
- Utilisation concomitante avec le millepertuis (voir rubrique 4.5)
- Hypersensibilité aux substances actives lévonorgestrel, éthinylestradiol ou à l’un des excipients mentionnés à la rubrique 6.1.
Levorichter 30 est contre-indiquée avec des médicaments concomitants contenant ombitasvir/paritaprévir/ritonavir, dasabuvir, glécaprevir/pibrentasvir et sofosbuvir/velpatasvir/voxilaprévir (voir rubriques 4.4 et 4.5).
4.8 Effets indésirables
Les effets indésirables suivants ont été observés pendant l’utilisation de l’éthinylestradiol/lévonorgestrel:
Classe de systèmes d'organes | Fréquent | Peu fréquent (≥1/1 000 à <1/100) | Rare (≥1/10 000 à <1/1 000) | Très rare (<1/10 000) | Fréquence indéterminée |
Néoplasmes bénins, malins et non spécifiés (y compris kystes et polypes) |
|
|
| Carcinomes hépatocellulaires, tumeurs bénignes du foie (par ex., hyperplasie nodulaire focale, adénome hépatique) |
|
Infections et infestations | Vaginite, y compris candidose vaginale |
|
|
|
|
Affections du système immunitaire |
|
| Réactions anaphylactiques, dont de rares cas d’urticaire, d’angio-œdème, de troubles circulatoires et respiratoires sévères | Exacerbation d’un lupus érythémateux disséminé | Exacerbation des symptômes de l’angiœdème héréditaire et acquis |
Troubles du métabolisme et de la nutrition |
| Modification de l’appétit (augmentation ou diminution) | Intolérance au glucose | Exacerbation d’une porphyrie |
|
Affections psychiatriques | Sautes d’humeur, y compris une dépression |
|
|
|
|
Affections du système nerveux | Nervosité, |
|
| Exacerbation d’une chorée |
|
Affections oculaires |
|
| Intolérance aux lentilles de contact | Névrite optique, |
|
Affections vasculaires |
| Hypertension | Thrombo-embolie veineuse et thrombo-embolie artérielle | Aggravation des veines variqueuses |
|
Affections gastro-intestinales | Nausées, | Crampes abdominales, ballonnements |
| Colite ischémique | Maladie inflammatoire de l'intestin (maladie de Crohn ou recto-colite hémorragique) |
Affections hépatobiliaires |
|
| Ictère cholestatique | Pancréatite, | état hépatocellulaire (par ex., hépatite, résultats anormaux aux tests de la fonction hépatique) |
Affections de la peau et du tissu sous-cutané | Acné | Éruption cutanée, | Érythème noueux | Érythème polymorphe |
|
Affections du rein et des voies urinaires |
|
|
| Syndrome hémolytique urémique |
|
Affections des organes de reproduction et du sein | Douleurs, tendresse des seins, gonflement et sécrétions mammaires, |
|
|
|
|
Troubles généraux et anomalies au site d’administration | Rétention de fluides/œdème, |
|
|
|
|
Investigations |
| Modification des lipides plasmatiques, y compris hypertriglycéridémie |
| Réduction des folates sériques |
|
Description de certains effets indésirables particuliers
Une augmentation du risque d'événement thrombotique et thrombo-embolique artériel et veineux, incluant l’infarctus du myocarde, l’accident vasculaire cérébral, les accidents ischémiques transitoires, la thrombose veineuse et l’embolie pulmonaire, a été observée chez les femmes utilisant des CHCs ; ceci est abordé plus en détail en rubrique 4.4.
Les événements indésirables sévères suivants ont été décrits par les utilisatrices de COCs et sont discutés à la rubrique 4.4 « Mises en garde spéciales et autres formes d’interactions ».
- Maladies thromboemboliques veineuses,
- Maladies thromboemboliques artérielles
- Hypertension
- Cancer du col de l’utérus
- Tumeurs hépatiques
- Affections de la peau et du tissu sous-cutané : chloasma, érythème noueux
- Maladie de Crohn, rectocolite hémorragique, porphyrie, lupus érythémateux disséminé, herpes gestationis, chorée de Sydenham, syndrome hémolytique et urémique, ictère cholestatique.
Le diagnostic du cancer du sein est légèrement accru chez les utilisatrices de COC. Etant donné que le cancer du sein est rare chez les femmes de moins de 40 ans, l’augmentation du nombre de cas est faible par comparaison au risque global de cancer du sein. Un lien de causalité avec les COC n’est pas connu. Pour un complément d’information, voir rubriques 4.3 et 4.4.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via :
Belgique :
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg :
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
Gedeon Richter Plc.
Gyömrői út 19-21
H-1103 Budapest
Hongrie
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
BE : BE285232
LU : 2003030013
• 0409977 : 3 x 21 comprimés enrobés
• 0801659 : 6 x 21 comprimés enrobés
• 0801662 : 13 x 21 comprimés enrobés
10. DATE DE MISE A JOUR DU TEXTE
02/2025
1
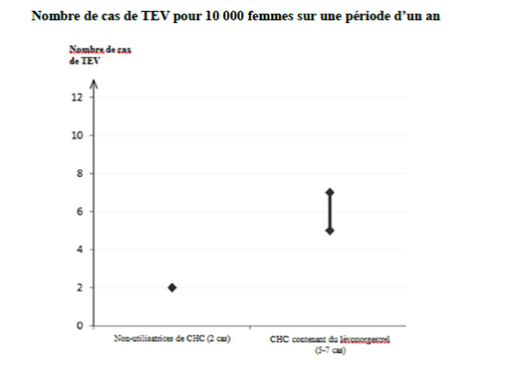
[1] Point central de l’intervalle de 5-7 pour 10 000 années-femmes sur la base d’un risque relatif, pour les CHC contenant du lévonorgestrel par rapport à la non-utilisation d’un CHC, d’environ 2,3 à 3,6
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 1625516 | LEVORICHTER 30 COMP ENROBES 3 X 21 | G03AA07 | € 6,66 | - | Oui | - | - |
| 2383107 | LEVORICHTER 30 COMP ENROBES 13 X 21 | G03AA07 | € 20,08 | - | Oui | - | - |
| 2383115 | LEVORICHTER 30 COMP ENROBES 6 X 21 | G03AA07 | € 12,67 | - | Oui | - | - |