1. DÉNOMINATION DU MÉDICAMENT
Drosana 20 0,02 mg/3 mg comprimés pelliculés
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque comprimé pelliculé contient 0,02 mg d’éthinylestradiol et 3 mg de drospirénone.
Excipients à effet notoire :
Chaque comprimé pelliculé contient 48,53 mg de lactose monohydraté et 0,070 mg de lécithine de soja.
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Comprimé pelliculé.
Comprimé pelliculé blanc à presque blanc, rond, biconvexe, d’environ 6 mm de diamètre. Une face porte l’inscription : « G73 ». L’autre face ne comporte pas d’inscription.
4. DONNÉES CLINIQUES
4.1 Indications thérapeutiques
Contraception orale.
La décision de prescrire Drosana 20 doit être prise en tenant compte des facteurs de risque de la patiente, notamment ses facteurs de risque de thrombo-embolie veineuse (TEV), ainsi que du risque de TEV associé à Drosana 20 en comparaison aux autres CHC (Contraceptifs Hormonaux Combinés) (voir rubriques 4.3 et 4.4).
4.2 Posologie et mode d’administration
Mode d’administration : voie orale
Posologie
Comment prendre Drosana 20
Les comprimés doivent être pris chaque jour, à peu près au même moment, éventuellement avec un peu de liquide, en respectant l’ordre indiqué sur la plaquette. Prendre un comprimé par jour pendant 21 jours consécutifs. Chaque plaquette suivante doit être commencée après une interruption de 7 jours sans prise de comprimés pendant laquelle se produit habituellement une hémorragie de privation. Celle-ci débute habituellement 2 ou 3 jours après la prise du dernier comprimé. Il se peut que cette hémorragie de privation ne soit pas terminée au moment d’entamer la plaquette suivante.
Comment commencer à utiliser Drosana 20
- Absence de contraception hormonale antérieure (au cours du mois précédent)
La prise des comprimés doit commencer le 1er jour du cycle menstruel normal de l’utilisatrice (c.-à-d. le premier jour de ses règles).
- Relais d’une autre contraception hormonale combinée (contraceptif oral combiné (COC), anneau vaginal ou patch transdermique)
Il est préférable de commencer Drosana 20 le jour qui suit la prise du dernier comprimé actif (le dernier comprimé contenant les substances actives) du COC précédent mais au plus tard le jour qui suit la période habituelle d’interruption de prise des comprimés ou après la prise du dernier comprimé placebo du COC précédent. En cas de relais d’un anneau vaginal ou d’un patch transdermique, il conviendra de commencer Drosana 20 de préférence le jour du retrait mais au plus tard le jour prévu pour la pose suivante.
- Relais d’un produit contenant uniquement un progestatif (pilule progestative seule, injection, implant) ou d’un dispositif intra-utérin (DIU) libérant un progestatif
L’utilisatrice peut passer à Drosana 20 à tout moment du cycle s’il s’agit d’une pilule progestative seule (le jour du retrait pour l’implant ou le DIU, ou le jour prévu pour l’injection suivante s’il s’agit d’une forme injectable) mais dans tous les cas, il est recommandé d’utiliser une méthode contraceptive de barrière pendant les 7 premiers jours de prise de comprimés.
- Après une interruption de grossesse au cours du premier trimestre
L’utilisatrice peut commencer Drosana 20 immédiatement. Dans ce cas, aucune autre méthode contraceptive n’est nécessaire.
- Après un accouchement ou une interruption de grossesse au cours du deuxième trimestre
Il sera conseillé aux femmes de commencer Drosana 20 21 à 28 jours après un accouchement ou un avortement au cours du deuxième trimestre. Si cette contraception est démarrée plus tardivement, il leur sera recommandé d’utiliser en plus une méthode contraceptive de barrière pendant les 7 premiers jours de traitement. Cependant, si des rapports sexuels ont déjà eu lieu, il convient d’exclure une éventuelle grossesse avant le début effectif de la prise du COC ou l’utilisatrice devra attendre ses premières règles.
En cas d’allaitement, voir rubrique 4.6.
Conduite à tenir en cas de comprimés oubliés
Si l’oubli du comprimé est constaté moins de 12 heures après l’heure habituelle de la prise, la protection contraceptive n’est pas diminuée. La femme devra prendre le comprimé oublié dès qu’elle constate l’oubli et prendre les comprimés suivants comme d’habitude.
Si l’oubli du comprimé est constaté plus de 12 heures après l’heure habituelle de la prise, la protection contraceptive peut être diminuée. La conduite à tenir en cas d’oubli de comprimé sera guidée par les deux règles de base suivantes :
- la prise de comprimés ne doit jamais être interrompue pendant plus de 7 jours
- 7 jours de prise ininterrompue du traitement sont nécessaires pour obtenir une inhibition correcte de l’axe hypothalamo-hypophyso-ovarien.
Par conséquent, les conseils suivants pourront être donnés pour la prise quotidienne :
- Semaine 1
La femme devra prendre le dernier comprimé oublié dès que l’oubli est constaté, même si cela implique la prise de deux comprimés en même temps. Les comprimés suivants devront être pris à l’heure habituelle. En outre, une méthode contraceptive de barrière (par exemple un préservatif) devra être utilisée pendant les 7 jours suivants. Si des rapports sexuels ont eu lieu au cours des 7 jours précédents, la possibilité d’une grossesse devra être envisagée. Plus le nombre de comprimés oubliés est important et plus l’oubli est proche de la période d’interruption de la prise, plus le risque de grossesse est élevé.
- Semaine 2
La femme devra prendre le dernier comprimé oublié dès que l’oubli est constaté, même si cela implique la prise de deux comprimés en même temps. Les comprimés suivants devront être pris à l’heure habituelle. Si les comprimés ont été pris correctement les 7 jours précédant le premier comprimé oublié, aucune mesure contraceptive complémentaire n’est nécessaire. Cependant, en cas d’oubli de plusieurs comprimés, il conviendra de recommander à l’utilisatrice de prendre des précautions complémentaires pendant 7 jours.
- Semaine 3
Le risque de diminution de la fiabilité est imminent en raison de la proximité de l’interruption de 7 jours sans comprimés. Toutefois, il est toujours possible d’empêcher la diminution de l’efficacité contraceptive en ajustant le calendrier de prise des comprimés. Par conséquent, il n’est pas nécessaire d’avoir recours à un moyen de contraception complémentaire si l’une des deux règles ci-dessous est respectée, tant que tous les comprimés ont été pris correctement au cours des 7 jours précédant le premier comprimé oublié. Si ce n’est pas le cas, l’utilisatrice devra suivre la première de ces deux options et utiliser en même temps un autre moyen de contraception au cours des 7 jours suivants.
- La femme devra prendre le dernier comprimé oublié dès que l’oubli est constaté, même si cela implique la prise de deux comprimés en même temps. Les comprimés suivants devront être pris à l’heure habituelle. La plaquette suivante doit être commencée dès la fin de la plaquette actuelle, c’est-à-dire sans arrêt entre les deux plaquettes. Il est peu probable que la femme ait des règles avant la fin de la seconde plaquette mais elle peut avoir des « spottings » ou des métrorragies les jours de prise de comprimés.
- Il est également possible de conseiller à l’utilisatrice d’arrêter de prendre les comprimés de la plaquette actuelle. Dans ce cas, elle gardera une période d’interruption de 7 jours maximum sans prise de comprimés, incluant le nombre de jours où des comprimés ont été oubliés, et commencera ensuite la nouvelle plaquette.
Si la femme a oublié plusieurs comprimés et que ses règles ne surviennent pas au cours de la première période normale d’interruption sans comprimés, la possibilité d’une grossesse devra être envisagée.
Conduite à tenir en cas de troubles gastro-intestinaux
En cas de troubles gastro-intestinaux sévères (par exemple des vomissements ou une diarrhée), l’absorption d’un comprimé peut ne pas être complète ; des mesures contraceptives complémentaires doivent donc être prises.
Si des vomissements surviennent dans les 3 ou 4 heures suivant la prise du comprimé, un nouveau comprimé (de remplacement) devra être pris dès que possible. Le nouveau comprimé devra si possible être pris dans les 12 heures qui suivent l’heure habituelle de prise du comprimé. Si plus de 12 heures se sont écoulées, les mêmes consignes que celles données pour les oublis de comprimés à la rubrique 4.2 « Conduite à tenir en cas de comprimés oubliés », doivent s’appliquer. Si l’utilisatrice ne veut pas modifier son calendrier normal de prise des comprimés, elle devra prendre le ou les autre(s) comprimé(s) dans une autre plaquette.
Comment retarder une hémorragie de privation
Pour retarder ses règles, l’utilisatrice doit commencer une nouvelle plaquette de Drosana 20 sans période d’interruption sans comprimés. Le report peut être prolongé aussi longtemps que désiré jusqu’à la fin de la seconde plaquette. Au cours de ce report, des spottings ou métrorragies peuvent survenir. La prise régulière de Drosana 20 reprend ensuite après l’interruption habituelle de 7 jours sans comprimés.
Pour décaler ses règles à un autre jour de la semaine que celui auquel elle est habituée avec son schéma en cours, il convient de lui conseiller de raccourcir la durée de la période d’interruption suivante d’autant de jours qu’elle le désire. Plus l’interruption sera courte, plus il y aura de risque qu’elle n’ait pas d’hémorragie de privation mais qu’elle présente des spottings ou des métrorragies au cours de la plaquette suivante (comme lors du report des règles).
4.3 Contre-indications
Les contraceptifs hormonaux combinés (CHC) ne doivent pas être utilisés dans les situations suivantes. Si l’une de ces affections survient pour la première fois au cours de l’utilisation d’un CHC, le traitement devra être immédiatement interrompu.
- Présence ou risque de thrombo-embolie veineuse (TEV)
- Thrombo-embolie veineuse – présence de TEV (patient traité par des anticoagulants) ou antécédents de TEV (p. ex. thrombose veineuse profonde [TVP] ou embolie pulmonaire [EP])
- Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie veineuse, telle qu’une résistance à la protéine C activée (PCa) (y compris une mutation du facteur V de Leiden), un déficit en antithrombine III, un déficit en protéine C, un déficit en protéine S
- Intervention chirurgicale majeure avec immobilisation prolongée (voir rubrique 4.4)
- Risque élevé de thrombo-embolie veineuse dû à la présence de multiples facteurs de risque (voir rubrique 4.4)
- Présence ou risque de thrombo-embolie artérielle (TEA)
- Thrombo-embolie artérielle – présence ou antécédents de thrombo-embolie artérielle (p. ex. infarctus du myocarde [IM]) ou de prodromes (p. ex. angine de poitrine)
- Affection cérébrovasculaire – présence ou antécédents d’accident vasculaire cérébral (AVC) ou de prodromes (p. ex. accident ischémique transitoire [AIT])
- Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie artérielle, telle qu’une hyperhomocystéinémie ou la présence d’anticorps anti-phospholipides (anticorps anti-cardiolipine, anticoagulant lupique).
- Antécédents de migraine avec signes neurologiques focaux
- Risque élevé de thrombo-embolie artérielle dû à la présence de multiples facteurs de risque (voir rubrique 4.4) ou d’un facteur de risque sévère tel que :
- diabète avec symptômes vasculaires
- hypertension artérielle sévère
- dyslipoprotéinémie sévère
- Présence ou antécédent d’affection hépatique sévère tant que les valeurs de la fonction hépatique ne se sont pas normalisées.
- Insuffisance rénale sévère ou aiguë
- Présence ou antécédent de tumeurs hépatiques (bénignes ou malignes)
- Diagnostic ou suspicion de malignités dépendantes des stéroïdes sexuels (par exemple des organes génitaux ou des seins)
- Saignements vaginaux sans diagnostic établi
- Hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1
- Hypersensibilité aux cacahuètes ou au soja
L’utilisation concomitante de Drosana 20 et d’autres médicaments contenant de l’ombitasvir/du paritaprévir/du ritonavir, du dasabuvir, des médicaments contenant du glécaprévir/du pibrentasvir ou du sofosbuvir/du velpatasvir/du voxilaprévir est contre-indiquée (voir rubrique 4.5).
4.8 Effets indésirables
Pour les effets indésirables graves chez les utilisatrices de COC, voir la rubrique 4.4.
Les effets indésirables suivants ont été rapportés lors de l’utilisation de drospirénone/éthinylestradiol :
Le tableau suivant mentionne les effets indésirables par classe de systèmes d’organes MedDRA. Les fréquences sont basées sur les données issues d’essais cliniques.
Classe de systèmes d’organes | Fréquence des effets indésirables | |||
MedDRA | Fréquent | Peu fréquent | Rare | Non connu (ne peut être estimé à partir des données disponibles)
|
Infections et infestations | | Candidose |
|
|
Affections du système immunitaire | | Réaction allergique | Asthme | Exacerbation des symptômes de l'angiœdème héréditaire et acquis |
Troubles du métabolisme et de la nutrition | | Augmentation de l’appétit |
|
|
Affections psychiatriques | Labilité émotionnelle | Dépression |
|
|
Affections du système nerveux | Céphalées | Paresthésie |
|
|
Affections de l’oreille et du labyrinthe |
|
| Hypo-acousie |
|
Affections oculaires | | Troubles de la vision |
|
|
Affections cardiaques | | Extrasystoles |
|
|
Affections vasculaires | | Embolie pulmonaire | Accidents thromboemboliques veineux (TEV) |
|
Affections respiratoires, thoraciques et médiastinales | | Pharyngite |
|
|
Affections gastro-intestinales | Douleurs abdominales | Nausées |
|
|
Affections de la peau et du tissu sous-cutané | Acné | Angiœdème | Erythème noueux |
|
Affections musculo-squelettiques et systémiques | | Douleur du cou |
|
|
Affections du rein et des voies urinaires | | Cystite |
|
|
Affections des organes de reproduction et du sein | Douleurs mammaires | Cancer du sein |
|
|
Troubles généraux et anomalies au site d’administration | | Œdème |
|
|
Investigations | Prise de poids | Perte de poids |
|
|
Description de certains effets indésirables particuliers
Une augmentation du risque d'événement thrombotique et thrombo-embolique artériel et veineux, incluant l’infarctus du myocarde, l’AVC, les accidents ischémiques transitoires, la thrombose veineuse et l’embolie pulmonaire, a été observée chez les femmes utilisant des CHC ; ceci est abordé plus en détails en rubrique 4.4.
Les effets indésirables graves suivants ont été rapportés chez des femmes utilisant des COC et sont également évoqués à la rubrique 4.4 « Mises en garde spéciales et précautions d’emploi » :
- troubles thromboemboliques veineux
- troubles thromboemboliques artériels
- hypertension
- tumeurs hépatiques
- survenue ou aggravation d’affections dont l’association avec les COC n’est pas certaine : maladie de Crohn, rectocolite hémorragique, épilepsie, myome utérin, porphyrie, lupus érythémateux disséminé, herpès gravidique, chorée de Sydenham, syndrome hémolytique et urémique, ictère cholestatique
- chloasma
- troubles aigus ou chroniques de la fonction hépatique pouvant nécessiter l’arrêt des COC jusqu’à la normalisation des marqueurs de la fonction hépatique
- les œstrogènes exogènes peuvent provoquer ou exacerber les symptômes de l'angiœdème héréditaire et acquis.
La fréquence de diagnostic de cancer du sein est très légèrement augmentée chez les utilisatrices de contraceptifs oraux. Le cancer du sein étant rare chez les femmes de moins de 40 ans, le nombre plus élevé de cancers du sein est faible par rapport au risque global de cancer du sein. La relation de causalité avec l’utilisation de COC est inconnue. Pour plus d’informations, se reporter aux rubriques 4.3 et 4.4.
Interactions
Des métrorragies et/ou un échec de la contraception peuvent être la conséquence d’interactions entre d’autres médicaments (inducteurs enzymatiques) et les contraceptifs oraux (voir rubrique 4.5).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via:
Belgique:
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance:
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg:
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHÉ
Gedeon Richter Plc.
Gyömrői út 19-21
1103 Budapest
Hongrie
8. NUMÉRO D’AUTORISATION DE MISE SUR LE MARCHÉ
BE : BE398745
LU : 2011060037
- 0839253: 1 × 21 comprimés pelliculés
- 0839284: 3 × 21 comprimés pelliculés
- 0839267: 6 × 21 comprimés pelliculés
- 0839271: 13 × 21 comprimés pelliculés
10. DATE DE MISE À JOUR DU TEXTE
01/2025
Date d’approbation : 02/2025
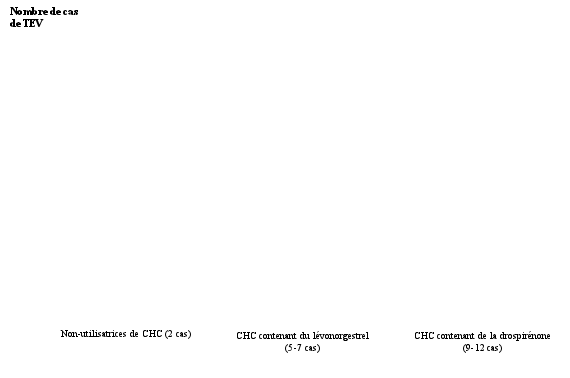
[1] Ces incidences ont été estimées à partir de l’ensemble des données des études épidémiologiques, en s’appuyant sur les risques relatifs liés aux différents CHC en comparaison aux CHC contenant du lévonorgestrel.
[2] Point central de l’intervalle de 5-7 pour 10 000 années-femmes sur la base d’un risque relatif, pour les CHC contenant du lévonorgestrel par rapport à la non-utilisation d’un CHC, d’environ 2,3 à 3,6.
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 3562279 | DROSANA 20 0,02MG/3MG COMP PELL 6 X 21 | G03AA12 | € 41,86 | - | Oui | € 23,86 | € 23,86 |
| 3562287 | DROSANA 20 0,02MG/3MG COMP PELL 3 X 21 | G03AA12 | € 26,16 | - | Oui | € 17,16 | € 17,16 |
| 3562295 | DROSANA 20 0,02MG/3MG COMP PELL 13 X 21 | G03AA12 | € 76,4 | - | Oui | € 37,4 | € 37,4 |