RESUME DES CARACTERISTIQUES DU PRODUIT
(12/2024)
1. DENOMINATION DU MEDICAMENT
Spiolto® Respimat® 2,5 microgrammes/2,5 microgrammes/inhalation, solution à inhaler
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
La dose délivrée est de 2,5 microgrammes de tiotropium (sous forme de bromure monohydraté) et de 2,5 microgrammes d’olodaterol (sous forme de chlorhydrate) par bouffée.
La dose délivrée est la quantité disponible pour le patient après le passage à travers l’embout buccal.
Excipient à effet notoire : ce médicament contient 0,0011 mg de chlorure de benzalkonium par bouffée.
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Solution à inhaler.
Solution à inhaler limpide et incolore.
4. DONNEES CLINIQUES
4.1 Indications thérapeutiques
Spiolto Respimat est indiqué en traitement bronchodilatateur continu destiné à soulager les symptômes des patients adultes présentant une bronchopneumopathie chronique obstructive (BPCO).
4.2 Posologie et mode d'administration
Posologie
Le médicament est destiné à la voie inhalée exclusivement. La cartouche ne peut être utilisée qu’avec l’inhalateur Respimat.
Une dose médicamenteuse correspond à 2 bouffées consécutives administrées à l’aide de l’inhalateur Respimat.
Adultes
La posologie recommandée chez l’adulte est de 5 microgrammes de tiotropium et de 5 microgrammes d’olodatérol, soit deux bouffées consécutives administrées à l’aide de l’inhalateur Respimat une fois par jour, à heure fixe.
Ne pas dépasser la posologie recommandée.
Sujets âgés
Spiolto Respimat peut être utilisé chez les sujets âgés sans adaptation de la posologie.
Insuffisance hépatique et insuffisance rénale
Spiolto Respimat contient du tiotropium qui est éliminé majoritairement par voie rénale et de l’olodatérol qui est métabolisé majoritairement par le foie.
Insuffisance hépatique
En cas d’insuffisance hépatique légère à modérée, Spiolto Respimat peut être utilisé sans adaptation de la posologie.
Il n’existe pas de données concernant l’administration d’olodaterol chez les patients atteints d’insuffisance hépatique sévère.
Insuffisance rénale
En cas d’insuffisance rénale, Spiolto Respimat peut être utilisé sans adaptation de la posologie.
Pour les patients atteints d’insuffisance rénale modérée à sévère (clairance de la créatinine ≤ 50 ml/min) voir les rubriques 4.4 et 5.2.
Spiolto Respimat contient de l’olodatérol. Les données relatives à l'utilisation de l’olodatérol chez les patients atteints d’insuffisance rénale sévère sont limitées.
Population pédiatrique
Il n’y a pas d'utilisation justifiée de Spiolto Respimat dans la population pédiatrique (moins de 18 ans).
Mode d’administration
Ce médicament est destiné à être utilisé par inhalation uniquement. La cartouche ne peut être insérée et utilisée que dans l'inhalateur Respimat réutilisable. Respimat est un dispositif d'inhalation qui génère une pulvérisation pour inhalation. Il est destiné à être utilisé par un seul patient et à délivrer plusieurs doses à l'aide d'une seule cartouche.
L'inhalateur Respimat réutilisable permet de remplacer la cartouche et peut être utilisé avec un maximum de 6 cartouches.
Les patients doivent lire le mode d'emploi de l'inhalateur Respimat réutilisable avant de commencer à utiliser Spiolto Respimat.
Pour une administration correcte du médicament, le médecin ou un autre professionnel de santé devra montrer au patient comment utiliser l’inhalateur.
Mode d’emploi pour la manipulation et l’utilisation de l’inhalateur Respimat réutilisable
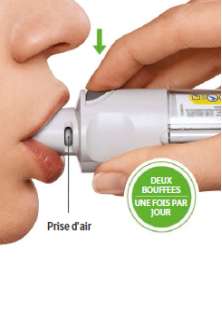
Le patient aura à utiliser cet inhalateur UNE SEULE FOIS PAR JOUR. À chaque utilisation, il prendra DEUX BOUFFEES.

- Si vous n’avez pas utilisé le Spiolto Respimat depuis plus de 7 jours, libérez une bouffée vers le sol.
- Si vous n’avez pas utilisé le Spiolto Respimat depuis plus de 21 jours, répétez les étapes 4 à 6 «Préparation pour l’utilisation» jusqu'à ce qu'un nuage soit visible. Ensuite, répétez les étapes 4 à 6 trois autres fois.
Comment entretenir l’inhalateur Respimat réutilisable
Nettoyer l’embout buccal au moins une fois par semaine, y compris la partie métallique à l’intérieur de l’embout buccal en utilisant uniquement un linge ou un tissu humide.
Une décoloration mineure de l’embout buccal n’affecte pas les performances de l’inhalateur Respimat réutilisable.
Si nécessaire, essuyer l'extérieur de l’inhalateur Respimat réutilisable avec un chiffon humide.
Quand se procurer un nouvel inhalateur
Lorsque le patient a utilisé l’inhalateur avec 6 cartouches, il doit se procurer une nouvelle boîte de Spiolto Respimat contenant un inhalateur. N’utilisez pas l'inhalateur Respimat réutilisable pendant plus d'un an après avoir inséré la première cartouche.


Préparation pour l’utilisation
|
|
|
|
|
|
|
|
|
|
|
|
Utilisation quotidienne
TOURNER
|
|
OUVRIR
|
|
PRESSER
|
|
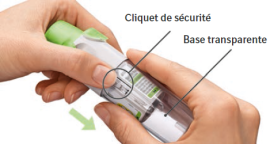
Quand remplacer la cartouche de Spiolto Respimat
L’indicateur de dose montre le nombre de bouffées restantes dans la cartouche.
| |
| |
| La cartouche est vide. Tourner la base transparente afin de la retirer. L’inhalateur est maintenant en position verrouillée. Retirer la cartouche de l’inhalateur. Insérer une nouvelle cartouche jusqu’à entendre un déclic (se référer à l’étape 2). La nouvelle cartouche dépassera davantage que la toute première cartouche (continuer avec l'étape 3). Ne pas oublier pas de remettre la base transparente pour déverrouiller l'inhalateur. |
4.3 Contre-indications
Hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1.
Antécédent d’hypersensibilité à l'atropine ou à ses dérivés, par exemple l'ipratropium ou l'oxitropium.
4.8 Effets indésirables
- Résumé du profil de sécurité
Un grand nombre des effets indésirables rapportés peuvent être attribués aux propriétés anticholinergiques du bromure de tiotropium ou aux propriétés β2-adrénergiques de l’olodatérol, les substances de Spiolto Respimat.
- Tableau résumé des effets indésirables
Les fréquences des effets indésirables présentées ci-dessous sont basées sur l'incidence des effets indésirables (c'est-à-dire les événements imputables à Spiolto Respimat) observés dans le groupe tiotropium 5 microgrammes/olodatérol 5 microgrammes (5 646 patients), regroupés à partir de 8 études cliniques conduites en groupes parallèles contrôlées contre comparateur actif ou placebo, incluant des patients présentant une BPCO, dont les durées de traitement étaient comprises entre 4 et 52 semaines.
Les effets indésirables rapportés dans tous les essais cliniques avec Spiolto Respimat sont présentés ci-dessous par classes de systèmes d’organes.
Tous les effets indésirables rapportés antérieurement avec une des substances sont également inclus.
La fréquence est définie selon la classification conventionnelle:
Très fréquent (≥1/10) ; fréquent (≥1/100 à <1/10) ; peu fréquent (≥1/1000 à <1/100) ; rare (≥1/10 000 à <1/1000) ; très rare (<1/10 000) ; fréquence indéterminé (ne peut être estimée sur la base des données disponibles).
Classe de systèmes d’organes | Effet indésirable | Fréquence |
Infections et infestations | Rhinopharyngite | Fréquence indéterminée |
Troubles du métabolisme et de la nutrition | Déshydratation | Fréquence indéterminée |
Affections du système nerveux | Sensations de vertige | Peu fréquent |
Insomnie | Rare | |
Céphalées | Peu fréquent | |
Affections oculaires | Vision trouble | Rare |
Glaucome | Fréquence indéterminée | |
Augmentation de la pression intraoculaire | Fréquence indéterminée | |
Affections cardiaques | Fibrillation auriculaire | Rare |
Tachycardie | Peu fréquent | |
Palpitations | Rare | |
Tachycardie supraventriculaire | Rare | |
Affections vasculaires | Hypertension | Rare |
Affections respiratoires, thoraciques et médiastinales | Toux | Peu fréquent |
Dysphonie | Peu fréquent | |
Laryngite | Rare | |
Pharyngite | Rare | |
Epistaxis | Rare | |
Bronchospasme | Rare | |
Sinusite | Fréquence indéterminée | |
Affections gastro-intestinales | Sécheresse buccale | Peu fréquent |
Constipation | Rare | |
Candidose oropharyngée | Rare | |
Gingivite | Rare | |
Nausées | Rare | |
Occlusion intestinale | Fréquence indéterminée | |
Dysphagie | Fréquence indéterminée | |
Reflux gastro-œsophagien | Fréquence indéterminée | |
Glossite | Fréquence indéterminée | |
Stomatite | Rare | |
Caries dentaires | Fréquence indéterminée | |
Affections de la peau et du tissu sous-cutané, Affections du système immunitaire | Hypersensibilité | Rare |
Angio-œdème (œdème de Quicke) | Rare | |
Urticaire | Rare | |
Prurit | Rare | |
Réaction anaphylactique | Fréquence indéterminée | |
Eruption cutanée | Rare | |
Infection cutanée/ulcération cutanée | Fréquence indéterminée | |
Sécheresse cutanée | Fréquence indéterminée | |
Affections musculo-squelettiques et systémiques | Arthralgie | Rare |
Douleurs dorsales1 | Rare | |
Gonflement articulaire | Rare | |
Affections du rein et des voies urinaires | Rétention urinaire | Rare |
Infection urinaire | Rare | |
Dysurie | Rare |
1 Effet indésirable rapporté avec Spiolto Respimat mais pas avec les substances prises séparément.
- Description d’effets indésirables sélectionnés
Spiolto Respimat associe les propriétés anticholinergiques et ß2-adrénergiques de ses composants le tiotropium et l’olodatérol.
Profil d’effets indésirables des anticholinergiques
Dans les études cliniques à long terme de 52 semaines avec Spiolto Respimat, l’effet indésirable lié aux effets anticholinergiques le plus fréquemment observé était la sécheresse buccale avec environ 1,3% des patients traités par Spiolto Respimat et respectivement 2,7% et 1% des patients dans les groupes tiotropium 5 microgrammes et olodatérol 5 microgrammes. La sécheresse buccale a entraîné l’arrêt du traitement chez 2 patients sur 4 968 (0,04%) traités par Spiolto Respimat.
Les effets indésirables graves liés aux effets anticholinergiques incluent : glaucome, constipation, occlusion intestinale y compris iléus paralytique et rétention urinaire.
Profil d’effets indésirables des agonistes ß-adrénergiques
Olodatérol, une des substances de Spiolto Respimat appartient à la classe thérapeutique des agonistes β2-adrénergiques de longue durée d'action. De ce fait, l'apparition d'autres effets indésirables liés à la classe des agonistes β-adrénergiques non listés ci-dessus doit être prise en compte, par exemple, arythmie, ischémie myocardique, angine de poitrine, hypotension, tremblement, nervosité, spasmes musculaires, fatigue, malaise, hypokaliémie, hyperglycémie et acidose métabolique.
- Autres populations particulières
L’incidence des effets anticholinergiques peut augmenter avec l’âge.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via:
Belgique
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance:
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L'AUTORISATION DE MISE SUR LE MARCHE
Boehringer Ingelheim International GmbH
Binger Strasse 173
55216 Ingelheim am Rhein
Allemagne
8. NUMERO(S) D'AUTORISATION DE MISE SUR LE MARCHE
Belgique : BE475093
Luxembourg : 2015120248
- 0799984: 1 inhalateur Respimat réutilisable et 1 cartouche
- 0800004: 1 inhalateur Respimat réutilisable et 3 cartouches
- 0874056: 1 cartouche
- 0874073: 3 cartouches
10. DATE DE MISE A JOUR DU TEXTE 12/2024
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 3264785 | SPIOLTO RESPIMAT 2,5/2,5 SOL INH.CART.3X60D+1INHAL | R03AL06 | € 128,77 | - | Oui | € 12,5 | € 8,3 |
| 3264793 | SPIOLTO RESPIMAT 2,5/2,5 SOL INH.CART.1X60D+1INHAL | R03AL06 | € 49,68 | - | Oui | € 12,4 | € 7,36 |