1. DÉNOMINATION DU MÉDICAMENT
Ultibro Breezhaler 85 microgrammes/43 microgrammes poudre pour inhalation en gélules
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque gélule contient 143 microgrammes de maléate d’indacatérol équivalant à 110 microgrammes d’indacatérol et 63 microgrammes de bromure de glycopyrronium équivalant à 50 microgrammes de glycopyrronium.
Chaque dose délivrée au travers de l’embout buccal de l’inhalateur contient 110 microgrammes de maléate d’indacatérol équivalant à 85 microgrammes d’indacatérol, et 54 microgrammes de bromure de glycopyrronium équivalant à 43 microgrammes de glycopyrronium.
Excipient(s) à effet notoire
Chaque gélule contient 23,5 mg de lactose (sous forme de monohydrate).
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Poudre pour inhalation en gélule (poudre pour inhalation).
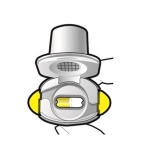
Gélules avec une coiffe jaune transparente et un corps naturel transparent contenant une poudre blanche à presque blanche et portant le code produit « IGP110.50 » imprimé en bleu sous deux lignes bleues sur le corps de la gélule et le logo de la société (![]() ) imprimé en noir sur la coiffe.
) imprimé en noir sur la coiffe.
4. INFORMATIONS CLINIQUES
4.1 Indications thérapeutiques
Ultibro Breezhaler est indiqué en traitement bronchodilatateur continu pour soulager les symptômes chez les patients adultes atteints de broncho-pneumopathie chronique obstructive (BPCO).
4.2 Posologie et mode d’administration
Posologie
La dose recommandée est l’inhalation du contenu d’une gélule une fois par jour à l’aide de l’inhalateur Ultibro Breezhaler.
Il est recommandé d’administrer Ultibro Breezhaler à la même heure chaque jour. En cas d’omission d’une dose, celle-ci doit être prise dès que possible le même jour. Les patients seront avertis qu’ils ne doivent pas prendre plus d’une dose par jour.
Populations particulières
Sujets âgés
Ultibro Breezhaler peut être utilisé à la dose recommandée chez les sujets âgés (75 ans et plus).
Insuffisance rénale
Ultibro Breezhaler peut être utilisé à la dose recommandée chez les patients atteints d’insuffisance rénale légère à modérée. En cas d’insuffisance rénale sévère ou en phase terminale nécessitant une dialyse, il ne doit être utilisé que si le bénéfice attendu pour le patient est supérieur au risque potentiel (voir rubriques 4.4 et 5.2).
Insuffisance hépatique
Ultibro Breezhaler peut être utilisé à la dose recommandée chez les patients présentant une insuffisance hépatique légère ou modérée. Il n’existe pas de données concernant l’administration d’Ultibro Breezhaler chez les patients atteints d’insuffisance hépatique sévère, il conviendra donc d'être prudent chez ces patients (voir rubrique 5.2).
Population pédiatrique
Il n’existe pas d’utilisation justifiée d’Ultibro Breezhaler dans la population pédiatrique (en dessous de 18 ans) dans l’indication de la BPCO. La sécurité et l’efficacité d’Ultibro Breezhaler chez les enfants n’ont pas été établies. Aucune donnée n’est disponible.
Mode d’administration
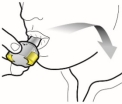
Voie inhalée. Les gélules ne doivent pas être avalées.
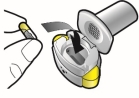
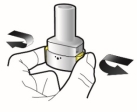
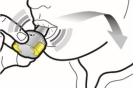
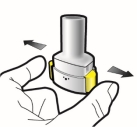
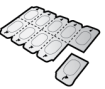
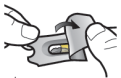
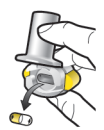
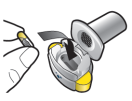
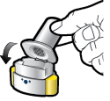
Les gélules doivent être exclusivement administrées à l’aide de l’inhalateur Ultibro Breezhaler fourni dans chacune des boites délivrées (voir rubrique 6.6).
Les patients doivent recevoir les instructions adaptées pour une utilisation correcte du dispositif d’inhalation et l’administration du médicament. En l’absence d’amélioration des symptômes respiratoires, il convient de vérifier que le patient inhale correctement le médicament.
Pour les instructions concernant l’utilisation du médicament avant administration, voir la rubrique 6.6.
4.3 Contre-indications
Hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1.
4.8 Effets indésirables
La présentation du profil de sécurité est basée sur l’expérience acquise avec Ultibro Breezhaler et ses principes actifs individuels.
Synthèse du profil de sécurité
L’expérience en matière de sécurité d’emploi d’Ultibro Breezhaler repose sur une exposition allant jusqu’à 15 mois à la dose thérapeutique recommandée.
Ultibro Breezhaler a entraîné des effets indésirables similaires à ceux observés avec les composants individuels de l’association. Comme il contient de l’indacatérol et du glycopyrronium, les effets indésirables du même type et de la même sévérité que ceux associés à chacun des composants peuvent être attendus avec l’association.
Le profil de sécurité est caractérisé par des symptômes anticholinergiques et bêta‑2‑adrénergiques caractéristiques des composants individuels de l’association. Les autres effets indésirables (EI) les plus fréquents liés au médicament (chez au moins 3 % des patients avec Ultibro Breezhaler et également plus souvent qu’avec le placebo) ont été la toux, la rhinopharyngite et les céphalées.
Résumé tabulé des effets indésirables
Les effets indésirables observés pendant les essais cliniques et à partir des données recueillies depuis la commercialisation sont présentés par classe de système d’organes MedDRA (Tableau 1). Dans chaque classe de système d’organe, les effets indésirables sont présentés suivant un ordre décroissant de fréquence. Dans chaque groupe de fréquence, les effets indésirables sont présentés suivant un ordre décroissant de gravité. De plus, pour chaque effet indésirable, la fréquence de survenue correspondante est présentée selon la convention suivante : très fréquent (≥ 1/10) ; fréquent (≥ 1/100, < 1/10) ; peu fréquent (≥ 1/1 000, < 1/100) ; rare (≥ 1/10 000, < 1/1 000) ; très rare (< 1/10 000) ; fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Tableau 1 Effets indésirables
Effets indésirables | Catégorie de fréquence de survenue |
Infections et infestations | |
Infection respiratoire haute | Très fréquent |
Rhinopharyngite | Fréquent |
Infection urinaire | Fréquent |
Sinusite | Fréquent |
Rhinite | Fréquent |
Affections du système immunitaire | |
Hypersensibilité | Fréquent |
Angiœdème2 | Peu fréquent |
Troubles du métabolisme et de la nutrition | |
Hyperglycémie et diabète | Fréquent |
Affections psychiatriques | |
Insomnie | Peu fréquent |
Affections du système nerveux | |
Vertiges | Fréquent |
Céphalée | Fréquent |
Paresthésies | Rare |
Affections oculaires | |
Glaucome1 | Peu fréquent |
Affections cardiaques | |
Cardiopathie ischémique | Peu fréquent |
Fibrillation auriculaire | Peu fréquent |
Tachycardie | Peu fréquent |
Palpitations | Peu fréquent |
Affections respiratoires, thoraciques et médiastinales | |
Toux | Fréquent |
Douleur oropharyngée incluant irritation de la gorge | Fréquent |
Bronchospasme paradoxal | Peu fréquent |
Dysphonie2 | Peu fréquent |
Epistaxis | Peu fréquent |
Affections gastro-intestinales | |
Dyspepsie | Fréquent |
Caries dentaires | Fréquent |
Gastro-entérite | Peu fréquent |
Sécheresse buccale | Peu fréquent |
Affections de la peau et du tissu sous-cutané | |
Prurit/éruption cutanée | Peu fréquent |
Affections musculo‑squelettiques et systémiques | |
Douleur musculo-squelettique | Peu fréquent |
Contractions musculaires | Peu fréquent |
Myalgie | Peu fréquent |
Douleurs des extrémités | Peu fréquent |
Affections du rein et des voies urinaires | |
Obstruction vésicale et rétention urinaire | Fréquent |
Troubles généraux et anomalies au site d’administration | |
Fièvre1 | Fréquent |
Douleur thoracique | Fréquent |
Œdème périphérique | Peu fréquent |
Sensation de fatigue | Peu fréquent |
1 Effet indésirable rapporté avec l'association Ultibro Breezhaler mais pas avec chacun des composants administrés individuellement.
2 Cas rapportés à partir des données recueillies depuis la commercialisation, mais la fréquence est calculée à partir des données issues des essais cliniques.
Description spécifique des effets indésirables
La toux est fréquente, mais habituellement d’intensité légère.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via:
Belgique
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance:
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy
ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet: www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHÉ
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Irlande
8. NUMÉRO(S) D’AUTORISATION DE MISE SUR LE MARCHÉ
EU/1/13/862/001-008
10. DATE DE MISE À JOUR DU TEXTE
24.07.2025
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’Agence européenne des médicaments http://www.ema.europa.eu/.
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 3085636 | ULTIBRO BREEZHALER 85MCG/43MCG PULV INHAL CAPS 90 | R03AL04 | € 129,09 | - | Oui | € 15,9 | € 10,5 |
| 3085644 | ULTIBRO BREEZHALER 85MCG/43MCG PULV INHAL CAPS 30 | R03AL04 | € 42,28 | - | Oui | € 10,6 | € 6,3 |