RESUME DES CARACTERISTIQUES DU PRODUIT
1. DENOMINATION DU MEDICAMENT
Dalacin Vaginal 100 mg/5 g crème vaginale
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
La substance active est le phosphate de clindamycine à une concentration de 2,38 %, équivalant à 2 % de clindamycine base.
Dalacin Vaginal est conditionné en tube de 20 g, auquel sont joints 3 applicateurs à usage unique, ou en tube de 40 g, auquel sont joints 7 applicateurs à usage unique. Chaque applicateur rempli de crème (= une dose) contient environ 5 g de crème (100 mg de clindamycine).
Excipients à effet notoire:
Dalacin Vaginal contient 250 mg de propylène glycol par 5 grammes de crème par applicateur, équivalent à 50 mg/g de propylène glycol.
Dalacin Vaginal contient 160,5 mg d’alcool cetostéarylique par 5 grammes de crème par applicateur, équivalent à 32,1 mg/g d’alcool cetostéarylique.
Dalacin Vaginal contient 50 mg d’alcool benzylique par 5 grammes de crème par applicateur, équivalent à 10 mg/g d’alcool benzylique.
Dalacin Vaginal contient 250 mg de polysorbate 60 par 5 grammes de crème par applicateur, équivalent à 50 mg/g de polysorbate 60.
Voir rubrique 4.4.Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Crème vaginale.
4. DONNEES CLINIQUES
4.1 Indications thérapeutiques
Traitement de la vaginose bactérienne (connue auparavant sous le nom de vaginite à Haemophilus, vaginite à Gardnerella, vaginite non spécifique, vaginite à Corynebacterium ou vaginite anaérobie).
Il convient tout d’abord d’exclure, par un examen de laboratoire approprié, les autres germes pathogènes qui sont souvent cause de vulvovaginite, Trichomonas vaginalis et Candida albicans, ainsi que des infections par Chlamydia trachomatis et des infections gonococciques.
A l'instar des autres antibiotiques, les informations concernant la prévention de la résistance locale ainsi que les recommandations officielles en matière de prescription d'antibiotiques doivent être consultées avant de prescrire de la clindamycine.
4.2 Posologie et mode d’administration
Posologie
Introduire dans le vagin un applicateur rempli de crème (environ 5 g) par jour pendant 7 jours consécutifs, avant le coucher.
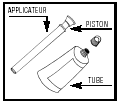
Ouvrir le tube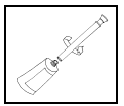
Visser un applicateur en plastique sur le tube.
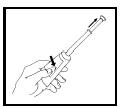
Comprimer doucement la partie inférieure du tube pour remplir l’applicateur de crème jusqu’à ce qu’une résistance soit perçue ; à ce moment, le piston est en grande partie ressorti de l’applicateur ; dévisser l’applicateur ; refermer le tube.
Mode d’administration
La patiente étant en décubitus dorsal, introduire l’applicateur profondément dans le vagin et injecter la crème. Jeter l’applicateur après utilisation.
4.3 Contre-indications
Hypersensibilité à la substance active, la clindamycine, à la lincomycine, à un produit apparenté ou à l’un des excipients mentionnés à la rubrique 6.1.
La clindamycine est également contre-indiquée chez les personnes ayant des antécédents de colite associée aux antibiotiques.
4.8 Effets indésirables
Le tableau ci-dessous reprend les réactions indésirables identifiées lors des essais cliniques et lors de la surveillance après la mise sur le marché ; elles sont classées par classe de systèmes d’organes et par fréquence. Les réactions indésirables identifiées après la mise sur le marché sont mentionnées en caractères italiques. Les fréquences sont regroupées selon les conventions suivantes : très fréquent (≥ 1/10) ; fréquent (≥ 1/100, < 1/10) ; peu fréquent (≥ 1/1 000, < 1/100) ; rare (≥ 1/10 000, < 1/1 000) ; très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles). Dans chaque groupe de fréquence, les effets indésirables sont présentés par ordre décroissant de gravité.
La sécurité de la crème vaginale à la clindamycine a été évaluée chez des patientes qui n’étaient pas enceintes et chez des patientes au cours du second et du troisième trimestre de grossesse. La majorité des effets indésirables sont de sévérité faible à modérée. L’effet indésirable le plus souvent rapporté est la candidose vulvo-vaginale.
Classe de systèmes d’organes | Très fréquent | Fréquent | Peu fréquent | Fréquence indéterminée |
Infections et infestations |
| Infection fongique, | Infection bactérienne | Candida cutané |
Affections du système immunitaire |
|
| Hypersensibilité |
|
Affections endocriniennes |
|
|
| Hyperthyroïdie |
Affections du système nerveux |
| Céphalée, |
|
|
Affections de l’oreille et du labyrinthe |
|
| Vertiges |
|
Affections respiratoires, thoraciques et médiastinales |
| Infection des voies respiratoires supérieures | Epistaxis |
|
Affections gastro-intestinales |
| Douleur abdominale, | Distension abdominale, | Colite pseudomembraneuse (voir rubrique 4.4) |
Affections de la peau et du tissu sous-cutané |
| Prurit (hors site d'administration), | Urticaire, | Rash maculopapulaire |
Affections musculo-squelettiques et systémiques |
| Dorsalgie |
|
|
Affections du rein et des voies urinaires |
| Infection des voies urinaires, | Dysurie |
|
Affections gravidiques, puerpérales et périnatales |
| Travail anormal* |
|
|
Affections des organes de reproduction et du sein | Candidose vulvo-vaginale | Vulvovaginite, | Vulvovaginite à Trichomonas, | Endométriose |
Troubles généraux et anomalies au site d’administration |
|
|
| Inflammation, |
Investigations |
|
| Analyse microbiologique anormale |
|
* Les effets indésirables de « travail anormal » et de « glycosurie » ne sont d’application que chez les femmes enceintes.
Une colite pseudomembraneuse peut survenir lors du traitement (voir rubrique 4.4).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via :
Belgique : l’Agence fédérale des médicaments et des produits de santé
www.afmps.be - Division Vigilance:,
Site internet: www.notifieruneffetindesirable.be
e mail: adr@fagg-afmps.be
Luxembourg : Centre Régional de Pharmacovigilance de Nancy ou Division de la pharmacie et des médicaments de la Direction de la santé.
Site internet : www.guichet.lu/pharmacovigilance.7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
Pfizer NV/SA, 17 Boulevard de la Plaine, 1050 Bruxelles, Belgique.
8. NUMERO D’AUTORISATION DE MISE SUR LE MARCHE
BE165584
10. DATE DE MISE A JOUR DU TEXTE
11/25
25J13
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 1102714 | DALACIN VAGINAL CREME 40G | G01AA10 | € 25,97 | - | Oui | - | - |