1. DÉNOMINATION DU MEDICAMENT
Onbrez Breezhaler 150 microgrammes, poudre pour inhalation en gélules
Onbrez Breezhaler 300 microgrammes, poudre pour inhalation en gélules
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Onbrez Breezhaler 150 microgrammes, poudre pour inhalation en gélules
Chaque gélule contient 150 microgrammes d’indacatérol sous forme de maléate d’indacatérol.
La dose délivrée par l’embout buccal de l’inhalateur est de 120 microgrammes d’indacatérol sous forme de maléate d’indacatérol.
Excipient à effet notoire :
Chaque gélule contient 24,8 mg de lactose (sous forme de monohydrate).
Onbrez Breezhaler 300 microgrammes, poudre pour inhalation en gélules
Chaque gélule contient 300 microgrammes d’indacatérol sous forme de maléate d’indacatérol.
La dose délivrée par l’embout buccal de l’inhalateur est de 240 microgrammes d’indacatérol sous forme de maléate d’indacatérol.
Excipient à effet notoire :
Chaque gélule contient 24,6 mg de lactose (sous forme de monohydrate).
Pour la liste complète des excipients, voir rubrique 6.1.
3. FORME PHARMACEUTIQUE
Poudre pour inhalation en gélule
Onbrez Breezhaler 150 microgrammes, poudre pour inhalation en gélules
Gélules transparentes (incolores) contenant une poudre blanche et portant la mention « IDL 150 » imprimée en noir au‑dessus d’une ligne noire et le logo de la société imprimé en noir sous la ligne.
Onbrez Breezhaler 300 microgrammes, poudre pour inhalation en gélules
Gélules transparentes (incolores) contenant une poudre blanche et portant la mention « IDL 300 » imprimée en bleu au‑dessus d’une ligne bleue et le logo de la société imprimé en bleu sous la ligne.
4. INFORMATIONS CLINIQUES
4.1 Indications thérapeutiques
Onbrez Breezhaler est indiqué en traitement bronchodilatateur continu de l’obstruction des voies respiratoires chez les patients adultes atteints de broncho‑pneumopathie chronique obstructive (BPCO).
4.2 Posologie et mode d’administration
Posologie
La dose recommandée est l’inhalation du contenu d’une gélule de 150 microgrammes une fois par jour à l’aide de l’inhalateur Onbrez Breezhaler. La posologie ne doit être augmentée que sur avis médical.
L’inhalation du contenu d’une gélule de 300 microgrammes une fois par jour à l’aide de l’inhalateur Onbrez Breezhaler peut apporter un bénéfice clinique supplémentaire pour diminuer l’essoufflement, en particulier chez les patients atteints de BPCO sévère. La dose maximale préconisée est de 300 microgrammes une fois par jour.
Onbrez Breezhaler doit être administré quotidiennement à heure fixe dans la journée.
En cas d’omission d’une dose, la dose suivante doit être prise à l’heure habituelle le lendemain.
Populations spécifiques :
Sujets âgés
La concentration plasmatique maximale et l’exposition systémique totale augmentent avec l’âge mais il n’est pas nécessaire d’adapter la posologie chez les patients âgés (65 ans et plus).
Insuffisance hépatique
Il n’est pas nécessaire d’adapter la posologie chez les patients présentant une insuffisance hépatique légère à modérée. Il n’existe pas de données concernant l’administration d’Onbrez Breezhaler chez les patients atteints d’insuffisance hépatique sévère.
Insuffisance rénale
Il n’est pas nécessaire d’adapter la posologie chez les patients présentant une insuffisance rénale.
Population pédiatrique
Il n’existe pas d’utilisation justifiée d’Onbrez Breezhaler dans la population pédiatrique (moins de 18 ans).
Mode d’administration
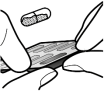
Voie inhalée exclusivement. Les gélules Onbrez Breezhaler ne doivent pas être avalées.
Les gélules ne doivent être extraites de la plaquette qu’au moment de leur utilisation.
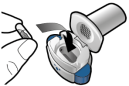
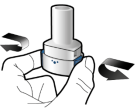
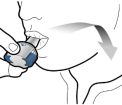
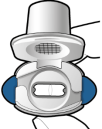
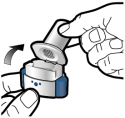
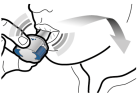
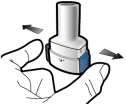
Les gélules doivent être administrées en utilisant uniquement l’inhalateur Onbrez Breezhaler (voir rubrique 6.6). Il convient d’utiliser l’inhalateur Onbrez Breezhaler fourni à chaque nouvelle prescription.
Les patients doivent recevoir les instructions adaptées pour une administration correcte du produit. En cas de non amélioration des symptômes respiratoires par le traitement, il convient de vérifier que le patient n'avale pas la gélule au lieu de l'utiliser en inhalation à l'aide du dispositif.
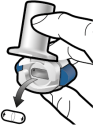
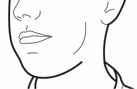
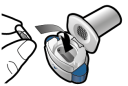
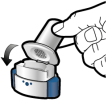
Pour les instructions concernant l’utilisation du médicament avant administration, voir la rubrique 6.6.
4.3 Contre‑indications
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
4.8 Effets indésirables
Synthèse du profil de sécurité d'emploi
Les effets indésirables les plus fréquents aux doses recommandées ont été : rhinopharyngite (14,3%), infections respiratoires hautes (14,2 %), toux (8,2 %), céphalées (3,7 %) et contractions musculaires (3,5 %). Dans la plupart des cas, ils ont été d’intensité légère ou modérée et leur fréquence diminuait avec la poursuite du traitement.
Aux doses recommandées, le profil d’effets indésirables d’Onbrez Breezhaler chez les patients atteints de BPCO montre des effets systémiques sans répercussions cliniques significatives de la stimulation des récepteurs bêta‑2‑adrénergiques. Les modifications de la fréquence cardiaque ont été en moyenne inférieures à une pulsation par minute et les cas de tachycardie ont été peu fréquents et rapportés à une incidence comparable à celle observée avec le placebo. Il n’a pas été détecté d’allongements significatifs de l’intervalle QTcF par rapport au placebo. La fréquence d’intervalle QTcF notable [soit > 450 ms chez les hommes et > 470 ms chez les femmes] et les cas d’hypokaliémie ont été comparables à ceux observés sous placebo. Les variations maximales de la glycémie ont été en moyenne comparables avec Onbrez Breezhaler par rapport au placebo.
Tableau de synthèse des effets indésirables
Le programme de développement clinique de phase III d’Onbrez Breezhaler a été mené chez des patients ayant un diagnostic clinique de BPCO modérée à sévère. Au total, 4 746 patients ont été exposés à l’indacatérol pendant des durées allant jusqu’à un an à des doses représentant jusqu’à deux fois la dose maximale recommandée. Chez ces patients, 2 611 ont été traités avec 150 microgrammes une fois par jour et 1 157 avec 300 microgrammes une fois par jour. Environ 41 % des patients présentaient une BPCO sévère. L’âge moyen des patients était de 64 ans, 48 % d’entre eux étant âgés de 65 ans ou plus, et les patients étaient majoritairement caucasiens (80 %).
Les effets indésirables sont présentés dans le tableau 1 selon la classification par classes d’organes MedDRA dans la base de données de sécurité d'emploi dans la BPCO. Au sein de chaque classe d’organes, les effets indésirables sont classés par fréquence en ordre décroissant selon la convention suivante : Très fréquent (≥ 1/10) ; fréquent (≥ 1/100, < 1/10) ; peu fréquent (≥ 1/1 000, < 1/100) ; rare (≥ 1/10 000, < 1/1 000) ; très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Tableau 1. Effets indésirables
Effets indésirables | Catégorie de fréquence |
Infections et infestations | |
Rhinopharyngite | Très fréquent |
Infection respiratoire haute | Très fréquent |
Sinusite | Fréquent |
Affections du système immunitaire | |
Hypersensibilité1 | Peu fréquent |
Troubles du métabolisme et de la nutrition | |
Diabète et hyperglycémie | Fréquent |
Affections du système nerveux | |
Céphalées | Fréquent |
Vertiges | Fréquent |
Paresthésies | Peu fréquent |
Affections cardiaques | |
Cardiopathie ischémique | Fréquent |
Palpitations | Fréquent |
Fibrillation auriculaire | Peu fréquent |
Tachycardie | Peu fréquent |
Affections respiratoires, thoraciques et médiastinales | |
Toux | Fréquent |
Douleur oropharyngée incluant irritation de la gorge | Fréquent |
Rhinorrhée | Fréquent |
Bronchospasme paradoxal | Peu fréquent |
Affections de la peau et du tissu sous-cutané | |
Prurit/éruption cutanée | Fréquent |
Affections musculo‑squelettiques et systémiques | |
Contractions musculaires | Fréquent |
Douleur musculo-squelettique | Fréquent |
Myalgie | Peu fréquent |
Troubles généraux et anomalies au site d’administration | |
Douleur thoracique | Fréquent |
Œdème périphérique | Fréquent |
1 Des cas d’hypersensibilité ont été observés depuis la commercialisation d’Onbrez Breezhaler. Ces cas sont issus de notifications spontanées sans information sur la population totale exposée ce qui rend impossible d’estimer avec précision la fréquence de survenue de cet effet indésirable ou d’établir une relation de causalité avec le médicament. Ainsi, la fréquence de survenue présentée est calculée à partir des données des essais cliniques. | |
Globalement, le profil de sécurité d'emploi d’Onbrez Breezhaler administré à raison de 600 microgrammes une fois par jour a été comparable à celui rapporté lors de l’administration des doses recommandées. Un effet indésirable supplémentaire a été des tremblements (fréquents).
Description des effets indésirables sélectionnés
Dans les études cliniques de phase III, les professionnels de santé ont observé lors des visites cliniques que 17 à 20 % des patients en moyenne présentaient une toux sporadique qui survenait habituellement dans les 15 secondes suivant l’inhalation et qui durait généralement 5 secondes (environ 10 secondes chez les fumeurs). Sa fréquence était plus élevée chez les femmes que chez les hommes et chez les fumeurs que chez les anciens fumeurs. Cette toux suivant l’inhalation n’a entraîné la sortie prématurée d’aucun patient des études menées aux doses recommandées (la toux est un symptôme de la BPCO et 8,2% seulement des patients ont rapporté une toux en tant qu’événement indésirable). Il n’existe pas de données indiquant que la toux survenant après l’inhalation soit associée à un bronchospasme, à des exacerbations, à une aggravation de la maladie ou à un manque d’efficacité.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via :
Belgique
Agence fédérale des médicaments et des produits de santé
www.afmps.be
Division Vigilance:
Site internet: www.notifieruneffetindesirable.be
e-mail: adr@fagg-afmps.be
Luxembourg
Centre Régional de Pharmacovigilance de Nancy
ou Division de la pharmacie et des médicaments de la Direction de la santé
Site internet : www.guichet.lu/pharmacovigilance
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHÉ
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Irlande
8. NUMÉRO(S) D’AUTORISATION DE MISE SUR LE MARCHÉ
Onbrez Breezhaler 150 microgrammes, poudre pour inhalation en gélules
EU/1/09/593/001-005
Onbrez Breezhaler 300 microgrammes, poudre pour inhalation en gélules
EU/1/09/593/006-010
10. DATE DE MISE À JOUR DU TEXTE
18.11.2025
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’Agence européenne des médicaments https://www.ema.europa.eu
PRIX
| Code CNK | Emballage | Code ATC5 | Prix | Prix ex-usine | Sur prescription | Ticket modérateur intervention régulière | Ticket modérateur intervention majorée |
|---|---|---|---|---|---|---|---|
| 2681286 | ONBREZ BREEZHALER 150 MCG PULV INHAL CAPS 30 | R03AC18 | € 36,25 | - | Oui | € 9,18 | € 5,46 |
| 2681310 | ONBREZ BREEZHALER 150 MCG PULV INHAL CAPS 3X30 | R03AC18 | € 84,97 | - | Oui | € 15,9 | € 10,5 |
| 2681328 | ONBREZ BREEZHALER 300 MCG PULV INHAL CAPS 3X30 | R03AC18 | € 86,93 | - | Oui | € 15,9 | € 10,5 |